Clear Sky Science · es
Estructura proteica transitoria guía las vías de difusión superficial para el transporte de electrones en supercomplejos de membrana
Cómo las células protegen sus líneas de energía
Cada segundo, las células de tu cuerpo mueven miles de millones de electrones para producir la molécula energética ATP. Si aunque sea una pequeña fracción de esos electrones se pierde, pueden formarse especies reactivas peligrosas que dañan el ADN, las proteínas y los lípidos. Este estudio explora cómo unas pequeñas “líneas de energía” proteicas en la membrana interna de las mitocondrias guían esos electrones de forma segura y eficiente de una estación a otra, revelando un papel sorprendente para fragmentos de proteína flexibles y aparentemente desordenados y para lípidos especiales de la membrana.
La ocupada red eléctrica dentro de las mitocondrias
Dentro de las mitocondrias, la producción de energía se realiza mediante una cadena de grandes máquinas proteicas incrustadas en una membrana. Dos estaciones clave, conocidas como Complejo III y Complejo IV, transfieren electrones usando una pequeña proteína portadora llamada citocromo c. Tradicionalmente, los científicos imaginaban al citocromo c moviéndose en tres dimensiones por el interior acuoso hasta chocar con cada complejo. Pero muchos organismos también organizan estos complejos en agrupaciones llamadas supercomplejos, lo que plantea la cuestión de si formar tales agrupaciones realmente mejora la eficiencia del transporte de electrones o simplemente mantiene la maquinaria ordenada y reduce pérdidas accidentales.
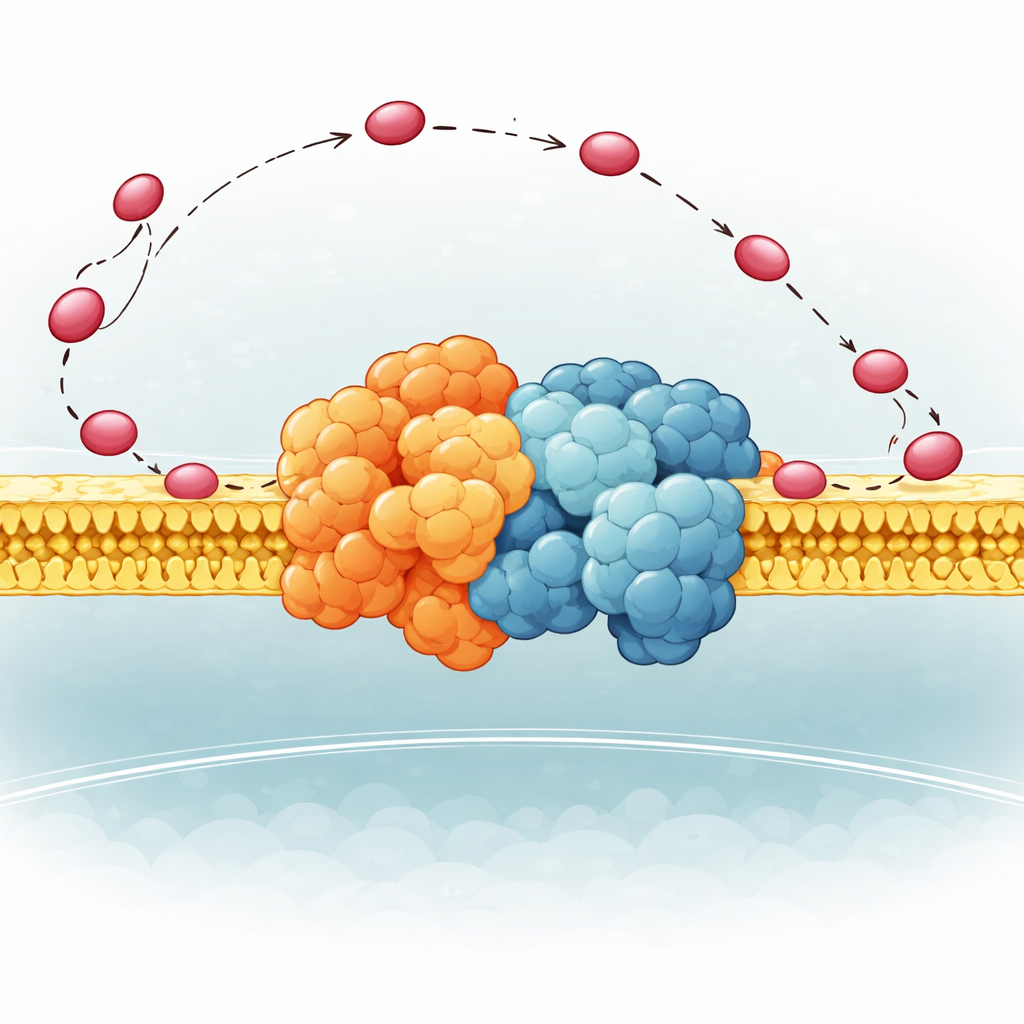
Una bisagra flexible que dirige al portador
Los autores se centraron en una pequeña parte del Complejo III en levadura llamada QCR6, que tiene un largo segmento “bisagra” cargado negativamente cuya estructura era demasiado flexible para captarse con claridad hasta ahora. Empleando una combinación de métodos computacionales avanzados —algoritmos de plegamiento proteico, dinámica molecular y criomicroscopía electrónica— generaron un conjunto de formas realistas que esta bisagra puede adoptar mientras está unida a un supercomplejo Complejo III–Complejo IV completo en una membrana. Encontraron que QCR6 no permanece inmóvil: cuando el citocromo c se acerca, partes de la bisagra se pliegan en hélices temporales y agarran al portador; cuando el citocromo c se mueve del Complejo III hacia el Complejo IV, la bisagra puede estirarse y desplegarse parcialmente, siguiéndolo y guiándolo a lo largo de la superficie de la membrana en lugar de permitir que se disperse en el fluido circundante.
Los lípidos de la membrana como guías invisibles
La propia membrana también desempeña un papel activo. El equipo sustituyó los lípidos genéricos en sus modelos por cardiolipina, un lípido cargado negativamente conocido por ser importante para la salud mitocondrial y que con frecuencia se altera en enfermedades cardíacas y neurodegenerativas. Las simulaciones mostraron que regiones cargadas positivamente en QCR6 se enganchan a las cabezas de cardiolipina, anclando efectivamente la bisagra a la membrana mientras escolta al citocromo c. Este acoplamiento hace que resulte energéticamente más barato para el portador deslizarse desde el Complejo III al Complejo IV a lo largo de la superficie, en lugar de saltar aleatoriamente en tres dimensiones. Cuando se eliminó la cardiolipina, el coste energético de este trayecto aumentó considerablemente, más citocromo c derivó hacia la solución en bloque y su posición dejó de estar sesgada claramente hacia el sitio aceptador de electrones.
De la deriva aleatoria al surf guiado
Mediante simulaciones a gran escala de dinámica browniana, los investigadores rastrearon dónde tiende a permanecer el citocromo c alrededor del supercomplejo. Con una bisagra QCR6 intacta y lípidos aniónicos presentes, la mayoría de las moléculas de citocromo c permanecen cerca de la membrana y pasan más tiempo junto a los sitios de contacto productivos en el Complejo III y el Complejo IV. A medida que la bisagra se extiende, la nube preferida de posiciones del citocromo c se desplaza del lado donador al lado aceptador, efectivamente “surfeando” a lo largo de la superficie del complejo. Esta difusión superficial guiada mejora la rapidez con que se pueden transferir los electrones sin convertir al citocromo c en una parte permanentemente adherida de la maquinaria; los portadores pueden seguir intercambiándose libremente con el reservorio circundante.
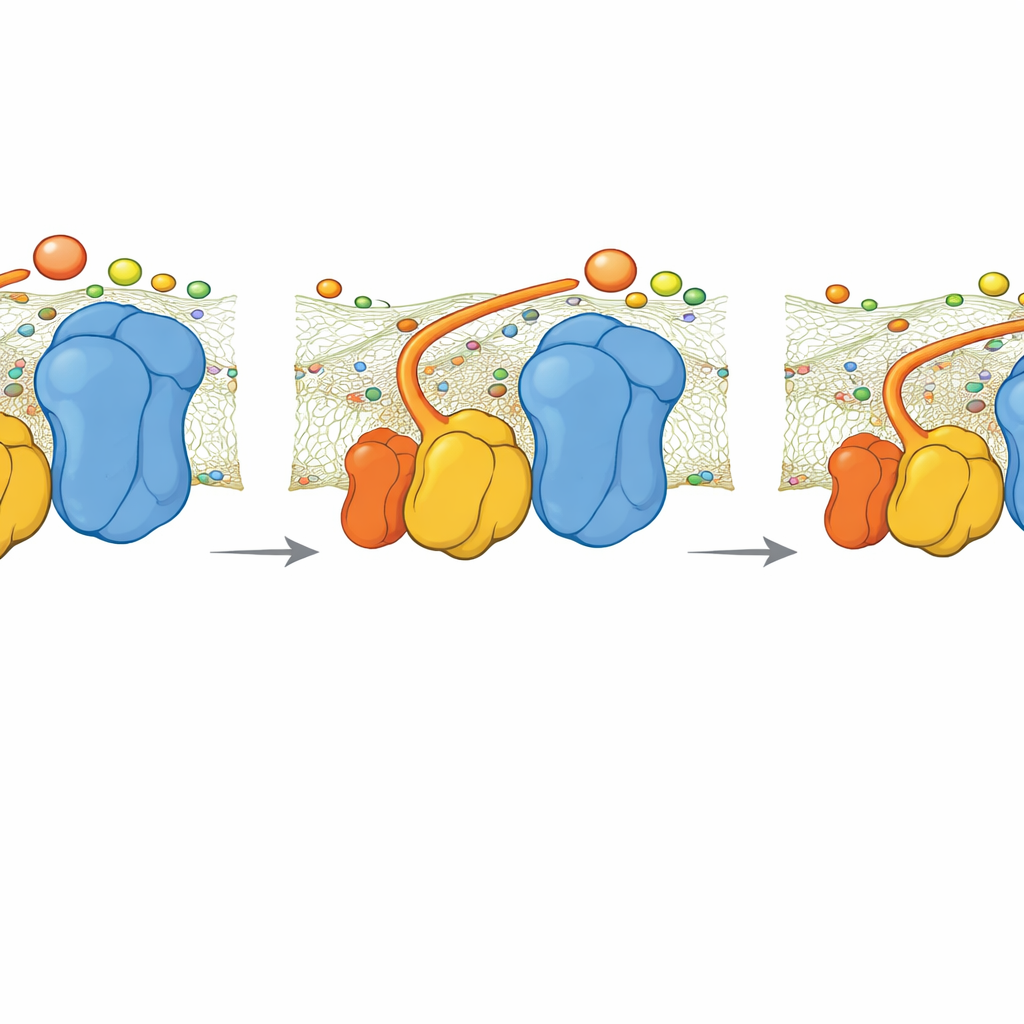
Qué ocurre cuando falta la bisagra
El equipo también estudió una cepa mutante de levadura carente de QCR6. Las imágenes de criomicroscopía mostraron que el supercomplejo se reorganiza en una forma más compacta y ligeramente distinta que restaura en parte una carga negativa continua en la superficie. No obstante, las simulaciones revelaron que sin la bisagra QCR6 la velocidad a la que el citocromo c transfiere electrones del Complejo III al Complejo IV disminuye. Un modelo cinético simple, que vincula el flujo de electrones con la producción de ATP, sugiere que bajo alta demanda energética esta pérdida de guía podría reducir la producción de ATP en aproximadamente un 30 por ciento. A demanda más baja, la diferencia es menor, porque una difusión más lenta y menos organizada todavía resulta suficiente.
Por qué esto importa para la salud y la evolución
En conjunto, el trabajo respalda una imagen nueva: en lugar de actuar como andamios estáticos, segmentos proteicos flexibles y lípidos cargados cooperan para confinar a los portadores de electrones en la superficie de la membrana y sesgar su movimiento a lo largo de rutas seguras y productivas. En levadura, una bisagra QCR6 inusualmente larga y una abundancia de cardiolipina generan esta “difusión guiada por reformación” que limita las fugas de electrones y aumenta la producción de energía. En otros organismos, bisagras más cortas, diseños distintos de supercomplejos o incluso anclajes covalentes parecen cumplir un objetivo similar: mantener a los portadores cerca de donde se necesitan. Comprender estos mecanismos sutiles de direccionamiento puede ayudar a explicar por qué los defectos en la cardiolipina o en la organización de los supercomplejos aparecen en el envejecimiento, la insuficiencia cardíaca y las enfermedades neurodegenerativas, y podría eventualmente orientar estrategias para ajustar el metabolismo energético celular.
Cita: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Palabras clave: supercomplejos mitocondriales, difusión de citocromo c, cardiolipina, cadena de transporte de electrones, bisagra QCR6