Clear Sky Science · fr
Une structure protéique transitoire guide les voies de diffusion en surface pour le transport d’électrons dans les supercomplexes membranaires
Comment les cellules protègent leurs lignes électriques
Chaque seconde, les cellules de votre corps déplacent des milliards d’électrons pour fabriquer la molécule énergétique ATP. Si même une petite fraction de ces électrons s’échappe, ils peuvent former des espèces réactives dangereuses qui endommagent l’ADN, les protéines et les lipides. Cette étude examine comment de minuscules protéines « lignes électriques » situées sur la membrane interne des mitochondries orientent ces électrons de manière sûre et efficace d’un point à un autre, révélant un rôle surprenant pour des segments protéiques flexibles apparemment désordonnés et pour des lipides membranaires particuliers.
Le réseau énergétique animé à l’intérieur des mitochondries
À l’intérieur des mitochondries, la production d’énergie s’effectue via une chaîne de grandes machines protéiques incrustées dans une membrane. Deux stations clés, appelées Complexe III et Complexe IV, se transmettent les électrons à l’aide d’une petite protéine porteuse nommée cytochrome c. Classiquement, les scientifiques imaginaient le cytochrome c dérivant en trois dimensions dans le milieu aqueux jusqu’à entrer en collision avec chaque complexe. Mais de nombreux organismes organisent aussi ces complexes en grappes appelées supercomplexes, ce qui pose la question de savoir si cette organisation améliore réellement l’efficacité du transport des électrons, ou si elle sert simplement à garder l’assemblage ordonné et à réduire les fuites accidentelles.
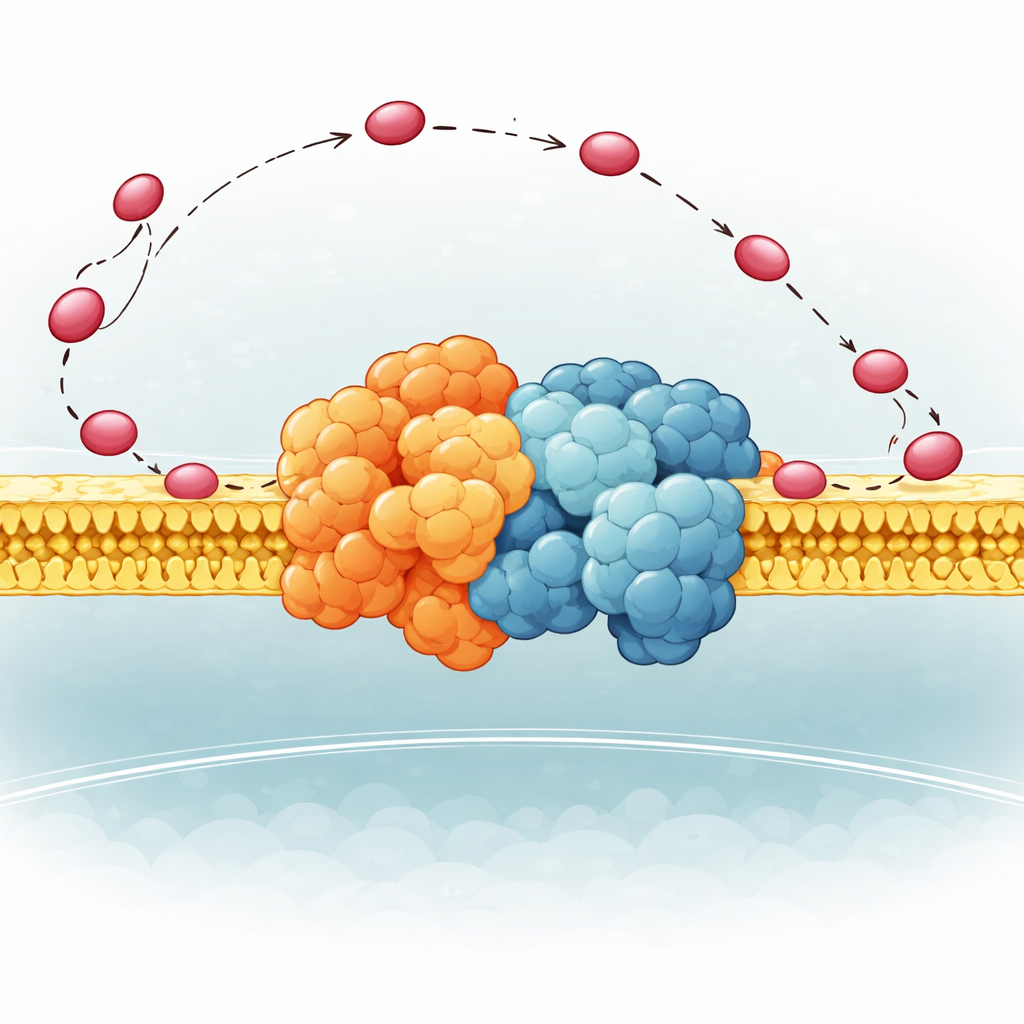
Une charnière flexible qui oriente le transporteur
Les auteurs se sont concentrés sur une petite partie du Complexe III de la levure appelée QCR6, qui possède un long segment « charnière » chargé négativement dont la structure était trop mobile pour avoir été capturée clairement auparavant. À l’aide d’une combinaison de méthodes informatiques avancées — algorithmes de repliement protéique, dynamique moléculaire et cryo‑microscopie électronique — ils ont généré un ensemble de conformations réalistes que cette charnière peut adopter lorsqu’elle est attachée à un supercomplexe Compex III–Complexe IV entier dans une membrane. Ils ont constaté que QCR6 n’est pas immobile : lorsqu’un cytochrome c s’approche, des parties de la charnière se replient en hélices temporaires et saisissent le transporteur ; au fur et à mesure que le cytochrome c se déplace du Complexe III vers le Complexe IV, la charnière peut s’étirer et se dérouler partiellement, le suivant et le guidant le long de la surface membranaire au lieu de le laisser errer dans le fluide environnant.
Les lipides membranaires comme guides invisibles
La membrane elle‑même joue aussi un rôle actif. L’équipe a remplacé les lipides génériques de leurs modèles par de la cardiolipine, un lipide chargé négativement connu pour son importance dans la santé mitochondriale et souvent altéré dans les maladies cardiaques et neurodégénératives. Les simulations ont montré que des zones chargées positivement sur QCR6 s’attachent aux têtes de cardiolipine, ancrant efficacement la charnière à la membrane pendant qu’elle escorte le cytochrome c. Cet accouplement rend énergétiquement moins coûteux le glissement du transporteur du Complexe III au Complexe IV le long de la surface, plutôt que de sauter aléatoirement en trois dimensions. Lorsque la cardiolipine était retirée, le coût énergétique de ce trajet augmentait fortement, davantage de cytochromes c dérivaient dans la solution en vrac et leur position était moins nettement orientée vers le site accepteur d’électrons.
Du vagabondage aléatoire au surf guidé
Par des simulations à grande échelle de dynamique brownienne, les chercheurs ont suivi les zones où le cytochrome c a tendance à stationner autour du supercomplexe. Avec une charnière QCR6 intacte et des lipides anioniques présents, la plupart des molécules de cytochrome c restent proches de la membrane et passent plus de temps près des sites de contact productifs sur le Complexe III et le Complexe IV. À mesure que la charnière s’étend, le nuage préféré de positions du cytochrome c se déplace du côté donneur vers le côté accepteur, « surfant » effectivement le long de la surface du complexe. Cette diffusion de surface guidée améliore la rapidité de la transmission d’électrons sans transformer le cytochrome c en une partie fixée en permanence de la machinerie ; les transporteurs peuvent toujours s’échanger librement avec le pool environnant.
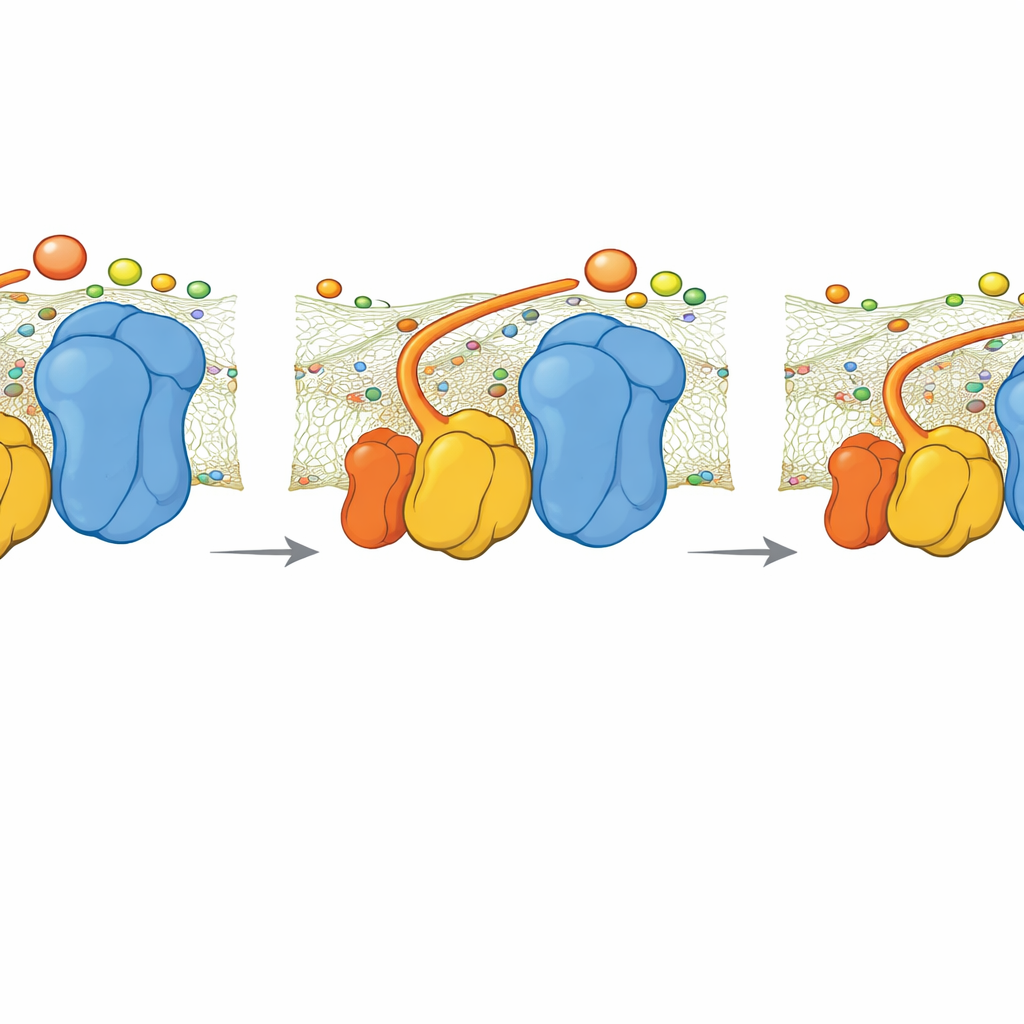
Que se passe‑t‑il quand la charnière manque
L’équipe a aussi étudié une souche mutante de levure dépourvue de QCR6. Les images cryo‑EM ont montré que le supercomplexe se réarrange en une forme plus compacte et légèrement différente qui restaure en partie une charge négative continue à la surface. Néanmoins, les simulations ont révélé qu’en l’absence de la charnière QCR6, la vitesse à laquelle le cytochrome c transfère des électrons du Complexe III au Complexe IV diminue. Un modèle cinétique simple, reliant le flux d’électrons à la production d’ATP, suggère que sous une forte demande énergétique cette perte de guidage pourrait réduire la production d’ATP d’environ 30 %. À plus faible demande, la différence est moindre, car une diffusion plus lente et moins organisée suffit encore.
Pourquoi cela compte pour la santé et l’évolution
Pris ensemble, les résultats soutiennent une nouvelle image : au lieu d’agir comme des échafaudages statiques, des segments protéiques flexibles et des lipides chargés coopèrent pour confiner les transporteurs d’électrons à la surface membranaire et orienter leur mouvement le long de voies sûres et productives. Chez la levure, une charnière QCR6 exceptionnellement longue et une abondance de cardiolipine génèrent cette « diffusion guidée par refolding » qui limite les fuites d’électrons et augmente le rendement énergétique. Chez d’autres organismes, des charnières plus courtes, des architectures de supercomplexe différentes ou même des attaches covalentes semblent poursuivre le même objectif — maintenir les transporteurs proches des lieux où ils sont nécessaires. Comprendre ces mécanismes subtils de guidage peut aider à expliquer pourquoi les défauts de la cardiolipine ou de l’organisation des supercomplexes se manifestent dans le vieillissement, l’insuffisance cardiaque et les maladies neurodégénératives, et pourrait finalement inspirer des stratégies pour ajuster le métabolisme énergétique cellulaire.
Citation: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Mots-clés: supercomplexes mitochondriaux, diffusion du cytochrome c, cardiolipine, chaîne de transport d’électrons, charnière QCR6