Clear Sky Science · he
מבנה חלבוני חולף מנווט מסלולי דיפוזיה על פני המשטח להעברת אלקטרונים בסופרקומפלקסים ממברנליים
איך התאים שומרים על קווי החשמל שלהם בטוחים
כל שנייה, התאים בגוף שלך מעבירים מיליארדי אלקטרונים כדי לייצר את מולקולת האנרגיה ATP. גם דליפה קטנה של חלק מהאלקטרונים עלולה להוליד חומרים תגובתיים מזיקים שפוצעים DNA, חלבונים ושומנים. המחקר הזה חוקר כיצד חלבונים זעירים — "קווי חשמל" — בממברנה הפנימית של המיטוכונדריה מכוונים את האלקטרונים בבטחה וביעילות מתחנה אחת לשנייה, וחושף תפקיד מפתיע לקטעים חלבוניים גמישים שנראים בלתי מסודרים ולשומנים מיוחדים בממברנה.
רשת הכוח העמוסה בתוך המיטוכונדריה
במיטוכונדריה, הפקת האנרגיה מתנהלת באמצעות שרשרת של מכונות חלבוניות גדולות שקועות בממברנה. שתי תחנות מרכזיות, קומפלקס III וקומפלקס IV, מעבירות אלקטרונים בעזרת נשא קטן בשם ציטוכרום c. באופן מסורתי, דמיינו את ציטוכרום c משתכשך בתלת־ממד בנוזל הפנימי עד שהוא פוגע בכל קומפלקס. אך באורגניזמים רבים הקומפלקסים מסודרים גם לצברים הנקראים סופרקומפלקסים, מה שמעלה את השאלה האם ארגון זה משפר באמת את היעילות בה מועברים האלקטרונים, או שפשוט מסדר את המכונה ומפחית דליפות אקראיות.
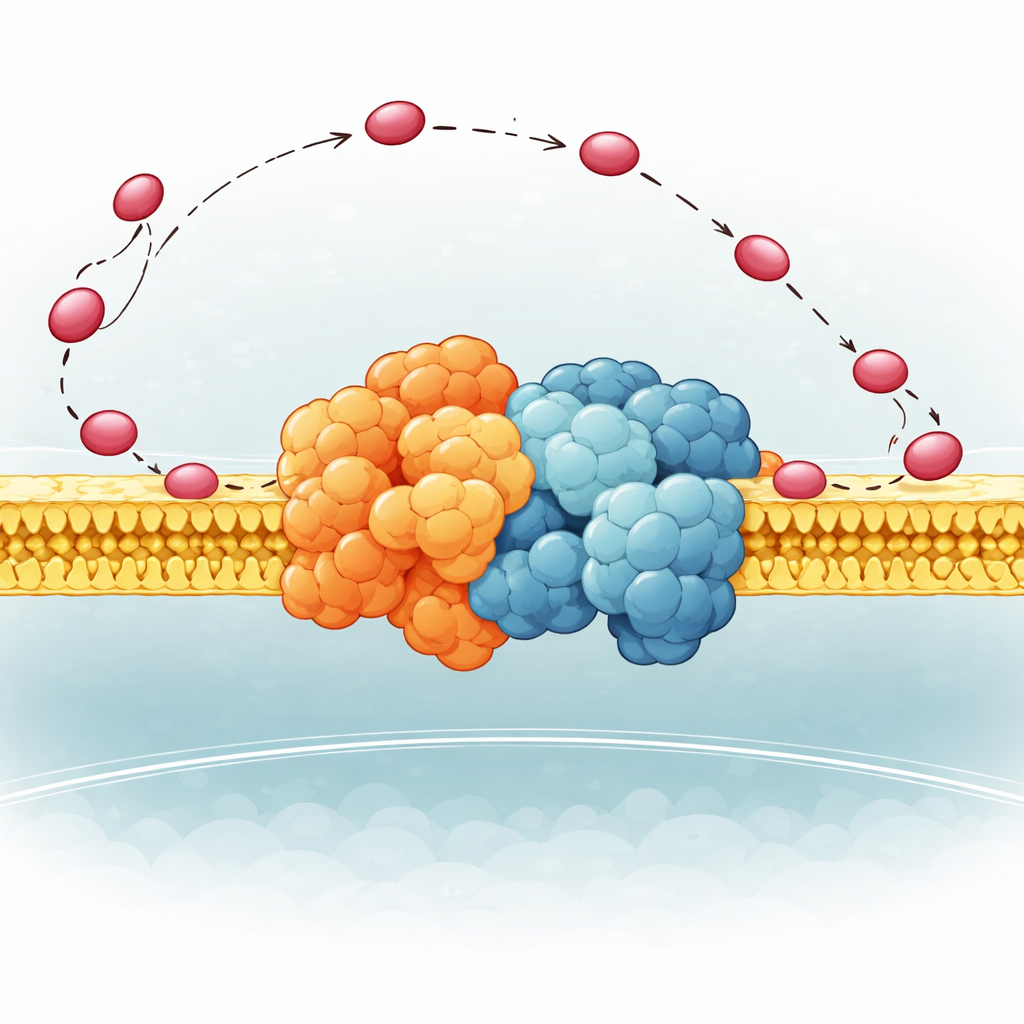
מפרק גמיש שמנווט את הנשא
המחברים התמקדו בחלק קטן של קומפלקס III בשמרים שנקרא QCR6, אשר כולל מקטע מפרקי ארוך בעל מטען שלילי שמבנהו היה גמיש מדי כדי ללכוד אותו בבירור קודם לכן. בשילוב של שיטות מתקדמות — אלגוריתמים לקיפול חלבונים, דינמיקת מולקולות ומיקרוסקופיה קריו־אלקטרונית — הם יצרו אנסמבל של צורות ריאליסטיות שהמפרק הזה יכול לאמץ כאשר הוא מחובר לסופרקומפלקס מלא של קומפלקס III–קומפלקס IV בממברנה. הם מצאו כי QCR6 אינו נייח: כאשר ציטוכרום c מתקרב, חלקי המפרק מקפלים זמנית להליקסים ותופסים את הנשא; כשהציטוכרום c נע מכיוון קומפלקס III לכיוון קומפלקס IV, המפרק יכול להימתח ולהתפרק חלקית, לעקוב ולהדריכו לאורך משטח הממברנה במקום לאפשר לו לשוטט לתוך הנוזל הסובב.
שומני הממברנה כמדריכים בלתי נראים
גם הממברנה עצמה ממלאת תפקיד פעיל. הצוות החליף בליפידים כלליים במודלים שלהם קרדיוליפין, שומן בעל מטען שלילי הידוע כחשוב לבריאות המיטוכונדריה ולעתים משתנה במחלת לב ובניוון עצבי. הסימולציות הראו כי אזורים טעונים בחיוב על QCR6 נצמדים לקבוצות־ראש של הקרדיוליפין, וכך מעגנים בפועל את המפרק לממברנה בזמן שהוא מלווה את ציטוכרום c. קשר זה מקל אנרגטית על הנשא להחליק מקומפלקס III לקומפלקס IV לאורך המשטח, במקום לקפוץ באופן אקראי בתלת־ממד. כאשר הסירו את הקרדיוליפין, עלה באופן חד העלות האנרגטית של המסע הזה, יותר ציטוכרום c נדדו לתוך התמיסה ועמדתם הפכה לפחות מוטה לכיוון אתרי הקבלה של האלקטרונים.
מנדנד אקראי להגלשה מונחתת
באמצעות הרצת סימולציות ברואניאניות בקנה מידה גדול, החוקרים עקבו היכן ציטוכרום c נוטה לשהות סביב הסופרקומפלקס. עם מפרק QCR6 שלם ונוכחות ליפידים אניוניים, רוב מולקולות הציטוכרום c נשארות קרובות לממברנה ומבלות יותר זמן קרוב לאתרי המגע הפרודוקטיביים על קומפלקס III וקומפלקס IV. כאשר המפרק מתארך, ענן המיקומים המועדף של ציטוכרום c זז מצד התורם אל צד המקבל, באופן אפקטיבי "גולש" לאורך משטח הקומפלקס. דיפוזיה מונחתת זו על פני המשטח משפרת את קצב העברת האלקטונים ללא הפיכת ציטוכרום c לחלק קבוע מהמכונה; הנשאים עדיין יכולים להחליף בחופשיות עם האוכלוסייה הסובבת.
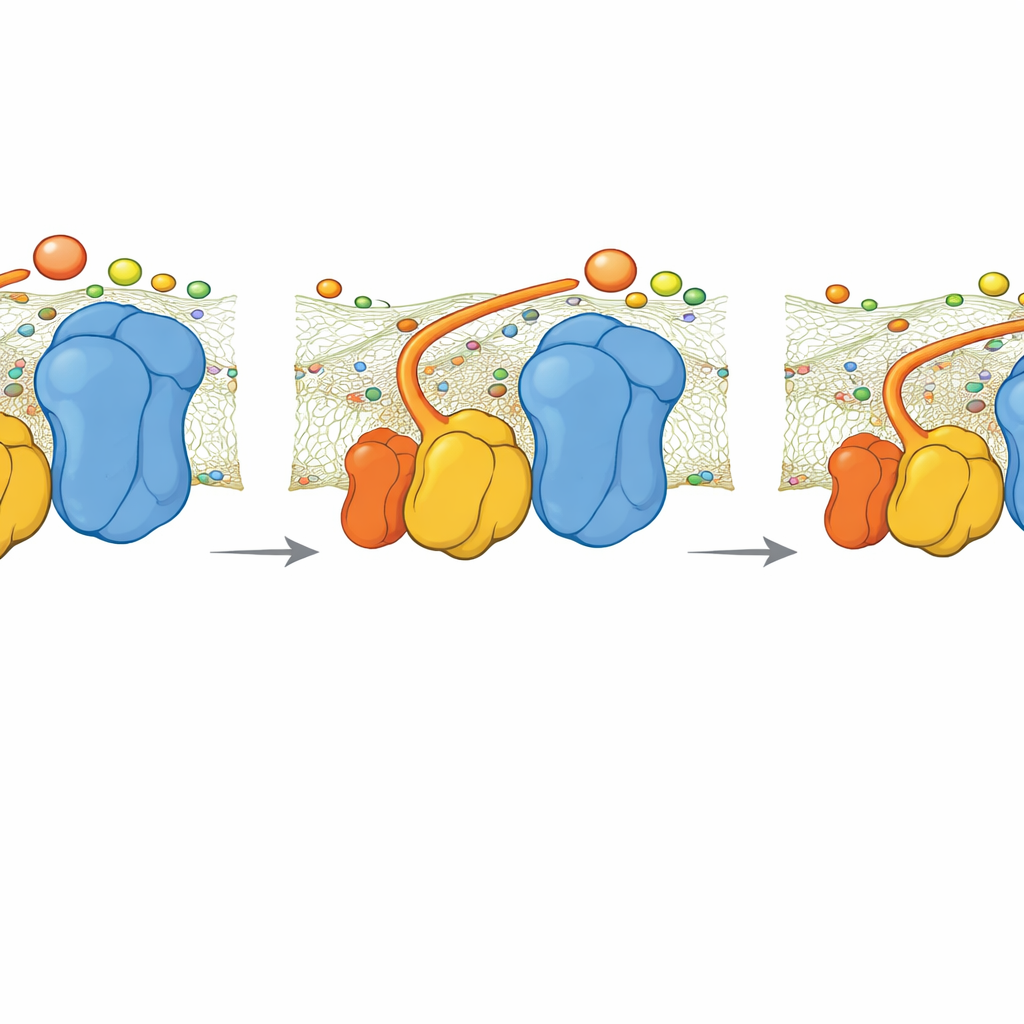
מה קורה כשחסר המפרק
הצוות גם חקר זן שמרי מוטנטי חסר QCR6. דימות קריו־EM הראה שהסופרקומפלקס מסתדר מחדש לצורה קומפקטית יותר ושונה במעט שמחזירה בחלקה מטען שלילי רציף על פני המשטח. למרות זאת, הסימולציות חשפו כי בלעדי מפרק QCR6 הקצב שבו ציטוכרום c מעביר אלקטרונים ממורכב III למורכב IV יורד. מודל קינטי פשוט שקושר את זרימת האלקטרונים לתפוקת ATP מציע כי בביקוש אנרגטי גבוה אובדן ההנחיה הזה יכול לחתוך את ייצור ה‑ATP בכ־30 אחוזים. בביקוש נמוך ההבדל קטן יותר, כי דיפוזיה איטית ופחות מסודרת עדיין מספיקה.
מדוע זה חשוב לבריאות ולאבולוציה
במבט הכללי, העבודה תומכת בתמונה חדשה: במקום לשמש כשלדי תמיכה סטטיים, מקטעים חלבוניים גמישים וליפידים טעונים משתפים פעולה כדי להגביל את נשאי האלקטרונים למשטח הממברנה ולהטות את תנועתם לאורך מסלולים בטוחים ופרודוקטיביים. בשמרים, מפרק QCR6 ארוך באופן יוצא דופן וקרדיוליפין בשפע יוצרים את "דיפוזיה מונחית על ידי קיפול חוזר" שמגבילה דליפת אלקטרונים ומגבירה את פלט האנרגיה. באורגניזמים אחרים, מפרקים קצרים יותר, עיצובים שונים של סופרקומפלקסים או אפילו קיבועים קוולנטיים נראים משרתים מטרה דומה — לשמור את הנשאים קרובים למקום שבו הם נדרשים. הבנת מנגנוני הניווט הדקים האלה עשויה לעזור להסביר מדוע פגמים בקרדיוליפין או בארגון הסופרקומפלקסים מופיעים בהזדקנות, אי־ספיקת לב ומחלות ניווניות עצביות, ועלולה בסופו של דבר להנחות אסטרטגיות לכוונון מטבוליזם האנרגיה התאי.
ציטוט: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
מילות מפתח: סופרקומפלקסים מיטוכונדריאליים, דיפוזיית ציטוכרום c, קרדיוליפין, שרשרת העברת האלקטרונים, מפרק QCR6