Clear Sky Science · zh
细菌蛋白-油酸复合物通过破坏细胞膜并抑制β-连环蛋白-GPX4轴在结直肠癌细胞中诱导类铁死亡
把细菌变成抗癌武器
结直肠癌是全球最常见的癌症之一,且常常学会逃避标准治疗。该研究探索了抗击这些肿瘤的一个意想不到的盟友:一种无害的细菌蛋白,当它与一种常见脂肪分子结合时,能够选择性地杀死结直肠癌细胞。通过弄清这种蛋白-脂复合物如何攻击肿瘤细胞同时在很大程度上保留健康细胞,研究人员希望为更有效且对患者更温和的治疗开辟新途径。
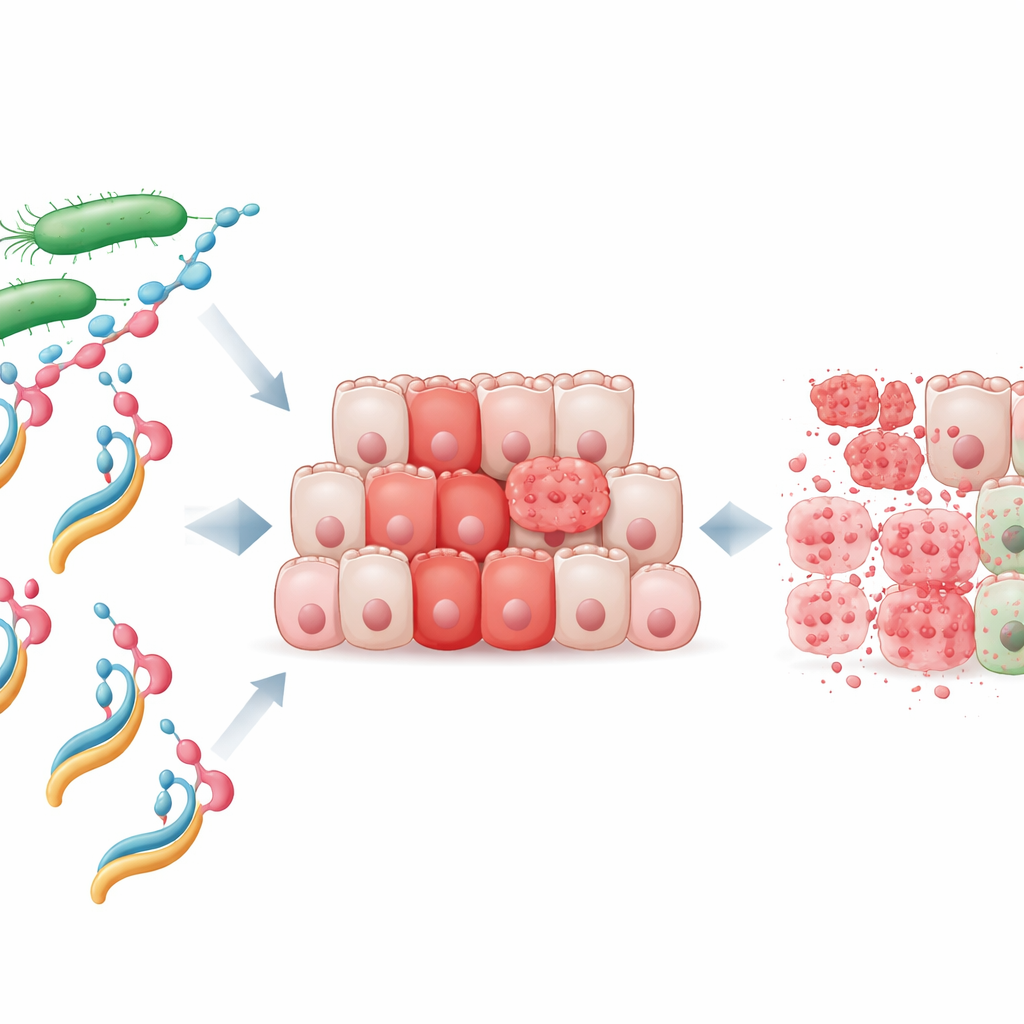
由蛋白与脂肪构建的新型武器
研究人员关注一种称为 NheA 的细菌蛋白,该蛋白单独存在时无害,甚至无法附着在人类细胞上。他们将纯化的 NheA 与油酸钠(一种来源于脂肪酸的分子)混合,得到他们所称的 NheA–O 复合物。类似的人源蛋白-脂复合物(如来源于乳汁的 HAMLET)已知能杀死癌细胞,但此前尚未有人证明细菌蛋白也可以转化为类似的肿瘤杀伤因子。体外试验显示,NheA–O 能快速降低结直肠癌细胞系的存活率,而单独成分——蛋白或脂肪——几乎没有影响。重要的是,正常结肠细胞对其敏感性远低,提示肿瘤细胞存在该复合物可以利用的特殊弱点。
直接攻击肿瘤细胞表面
利用先进成像技术,团队观察了 NheA–O 与癌细胞接触时的行为。标记的复合物在肿瘤细胞外表强烈发光,显示其与细胞膜紧密结合。细胞团(球状体)的三维成像证实 NheA–O 能渗透至类肿瘤结构的深处。为分离表面事件,研究者从癌细胞制备了巨型膜囊泡并暴露于 NheA–O。该复合物在这些囊泡上聚集、缩小其表面积,并使通常无法进入的染料分子渗入其中。用肿瘤细胞脂质制成的人工脂滴的额外测试显示,NheA–O 导致逐步泄漏,表明它物理上使癌细胞膜不稳定并穿孔。
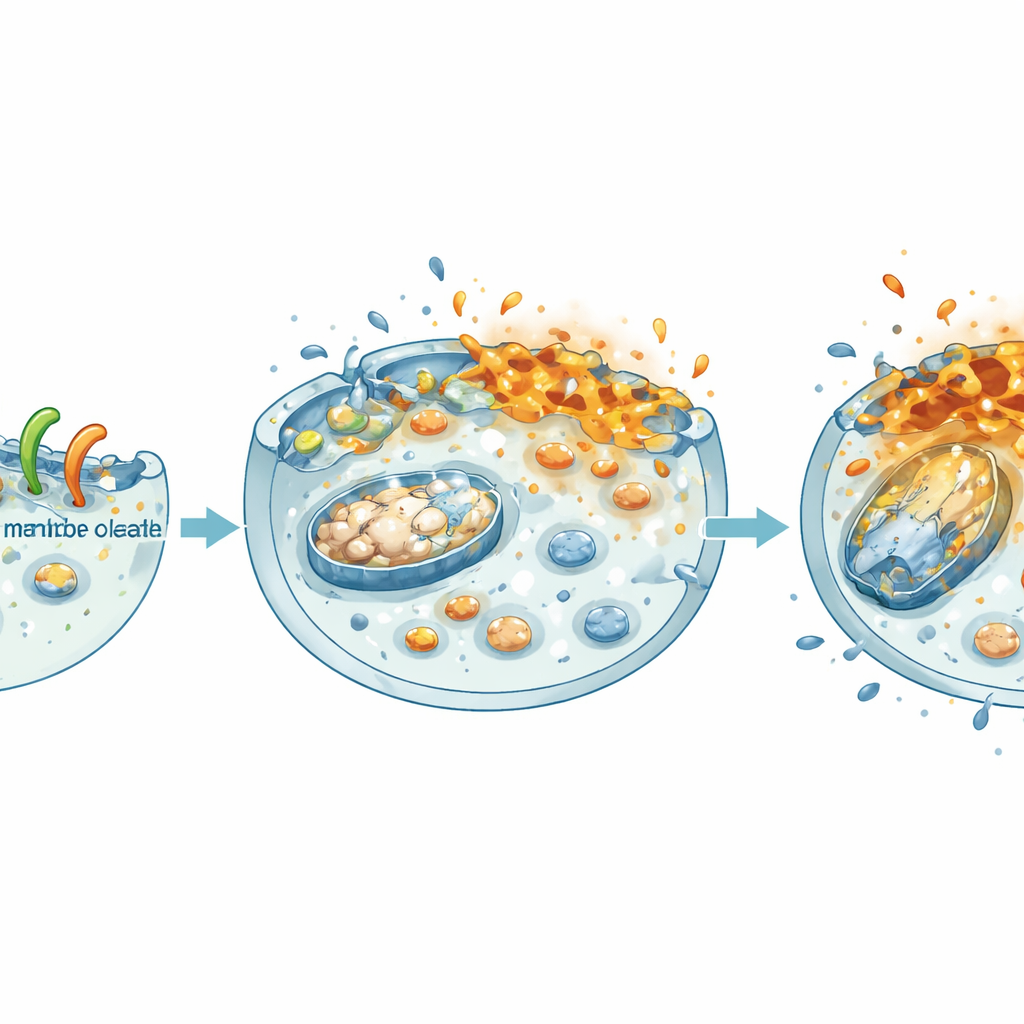
关闭细胞的能量与生长程序
一旦 NheA–O 扰动细胞膜,损伤便向内蔓延。团队发现,被处理的癌细胞丧失了线粒体跨膜电位——线粒体是细胞内的微小发电厂——其总体能量储备(ATP)在平面培养和三维球状体中都显著下降。与此同时,该复合物削弱了结直肠癌中的一个核心生长驱动通路:β‑连环蛋白通路。在患者数据中,β‑连环蛋白及其伴侣水平高与生存不良相关。在实验室中,NheA–O 降低了核内 β‑连环蛋白的含量、降低其活性并减少其促生长下游靶标的水平。因此,肿瘤细胞形成的克隆更少、迁移更慢并构建更小更脆弱的球状体——这些特征转化为肿瘤扩展和转移的减少。
在肿瘤膜中强迫发生类似“生锈”的死亡
该研究的一个关键发现是 NheA–O 诱导了一种特殊类型的细胞死亡,称为铁死亡,其类似于细胞脂质的“生锈”过程。该复合物提高了 ACSL4 的水平,这是一种使膜富含易受损脂肪构件的蛋白,同时降低了 GPX4 ——一种通常防止这些脂质氧化的关键“灭火员”酶。随着 GPX4 水平下降,膜中脂质损伤的化学标记急剧上升。促进铁死亡的药物使 NheA–O 更具致死性,而铁死亡抑制剂则在一定程度上挽救了细胞、减少膜损伤并部分恢复 β‑连环蛋白的活性。进一步的实验证明,NheA–O 促进对 GPX4 的标记,使其被细胞的蛋白降解机制拆解,并且已被耗竭 GPX4 的细胞尤其容易被杀死。
这对未来治疗可能意味着什么
综合来看,这些发现揭示了一种多方面的作用模式:NheA–O 附着于肿瘤细胞膜、破坏其完整性、耗尽其能量工厂,并通过瓦解保护性 GPX4 系统和沉默 β‑连环蛋白驱动的生长信号来强制引发类铁死亡。由于它同时打击多个脆弱点并在培养条件下在很大程度上保留正常结肠细胞,这种细菌蛋白‑脂复合物成为结直肠癌新疗法的有希望模板。尽管这些结果来自受控的细胞模型,接下来还需在动物乃至最终人类中验证,但它们拓展了这样一个概念:简单的蛋白-脂复合物——不论来自乳汁还是微生物——都可以被设计成精确而强效的抗癌剂。
引用: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
关键词: 结直肠癌, 铁死亡, 细菌蛋白, 细胞膜破坏, GPX4 与 β-连环蛋白