Clear Sky Science · he
קומפלקסים של חלבון חיידקי-אולאאט מעוררים מוות תאי דמוי פרופרטוזה בתאי סרטן המעי הגס על ידי פגיעה בממברנות התאים ועיכוב ציר β‑קטנין‑GPX4
הפיכת חיידקים ללוחמי סרטן
סרטן המעי הגס הוא אחד הסוגים הנפוצים ביותר של סרטן בעולם ולעתים קרובות לומד להתחמק מטיפולים סטנדרטיים. המחקר הזה חוקר בעל ברית לא צפוי במאבק בגידולים אלה: חלבון חיידקי חסר מזיק, שבעת שילובו עם מולקולת שומן נפוצה, יכול להשמיד באופן סלקטיבי תאי סרטן מעי גס. על־ידי הבנת האופן שבו קומפלקס חלבון‑שומן זה תוקף תאי גידול בעודו משאיר במידה רבה את התאים הבריאים ללא פגע, מקווים החוקרים לפתוח מסלול חדש לטיפולים שיעילים יותר ומעטים יותר בפגיעה בחולה.
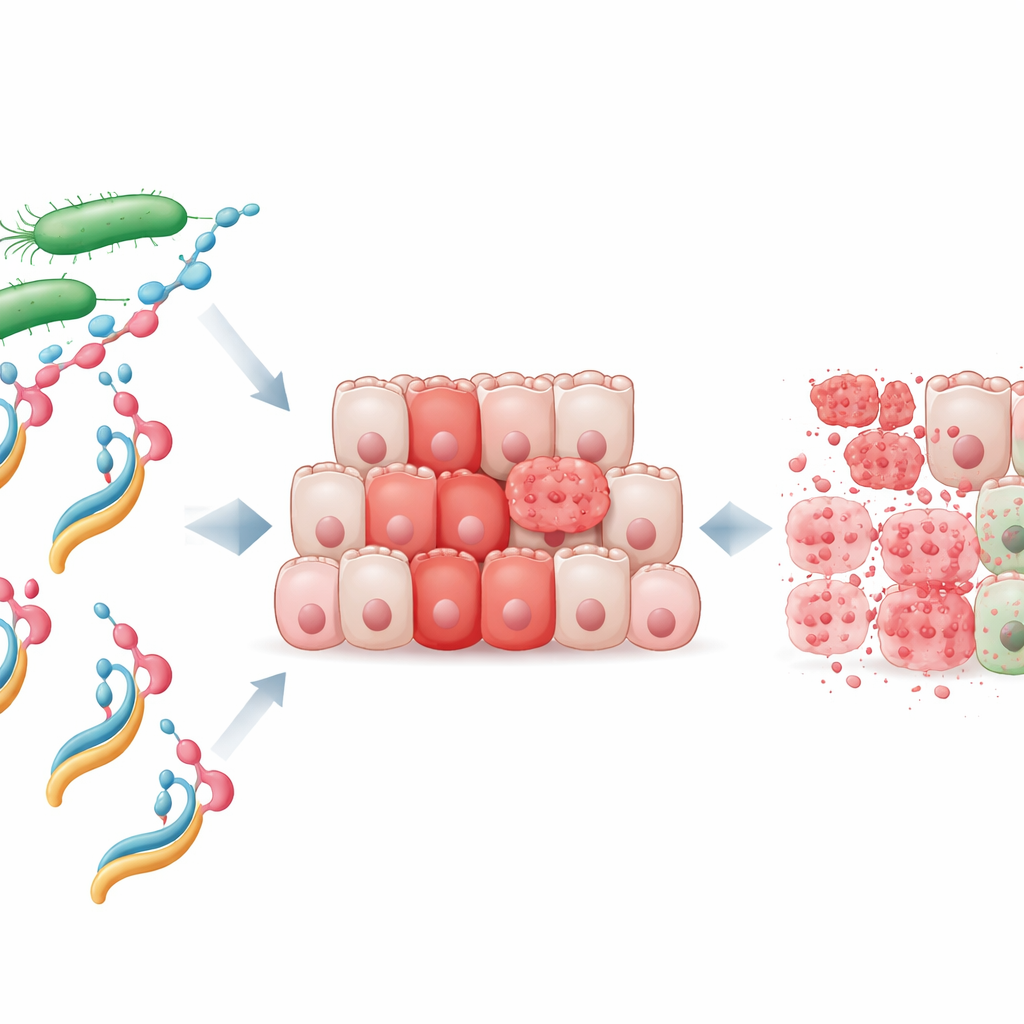
נשק חדש מבוסס על חלבון ושומן
החוקרים התרכזו בחלבון חיידקי בשם NheA, שביחידו חסר מזיק ואפילו אינו יכול להיצמד לתאים אנושיים. הם ערבבו NheA מזוקק עם אולאאט נתרן, מולקולה נגזרת של חומצת שומן, ליצירת קומפלקס שהם קוראים לו NheA–O. קומפלקסים דמויי‑חלבון‑שומן המתקיימים במערכת האנושית, כמו HAMLET המופק מחלב, ידועים ביכולתם להרוג תאי סרטן, אך עד כה לא הוסבר כי ניתן להפוך חלבון חיידקי לפועל טורף־גידולים דומה. ניסויים במעבדה הראו כי NheA–O הקטין במהירות את הישרדותם של שורות תאי סרטן מעי גס, בעוד שהמרכיבים הבודדים—החלבון או השומן לבדם—השפעה מועטה. באופן חשוב, תאי קולון נורמליים היו רגישים הרבה פחות, מה שמרמז כי לתאי הגידול יש חולשה מיוחדת שהקומפלקס יכול לנצל.
מתקפה ישירה על פני שטח התא הסרטני
באמצעות דימות מתקדם, הצוות עקב אחרי התנהגות NheA–O במפגשו עם תאי סרטן. גרסאות מתויגות של הקומפלקס זרחו בחוזקה סביב המעטפת החיצונית של תאי הגידול, והראו שהוא נקשר בחוזקה לממברנות שלהם. תמונות תלת‑ממד של צבירי תאים (ספירואידים) אישרו כי NheA–O יכול לחדור לעומק מבנים דמויי‑גידול. כדי לבודד את מה שקורה על פני השטח, יצרו החוקרים בועיות ממברנה ענקיות מתאי סרטן וחשפו אותן ל‑NheA–O. הקומפלקס הצטבר על הבועות הללו, הקטין את שטחן ואיפשר למולקולות צבע שבעבר לא יכלו לחדור—דלוף פנימה. בדיקות נוספות עם טיפות שומן מלאכותיות העשויות מליפידים של תאי הגידול הראו כי NheA–O גרם לדליפה מתמשכת, מה שמצביע על כך שהוא מייצב מבחינה פיזיקלית ומחורר את ממברנות תאי הסרטן.
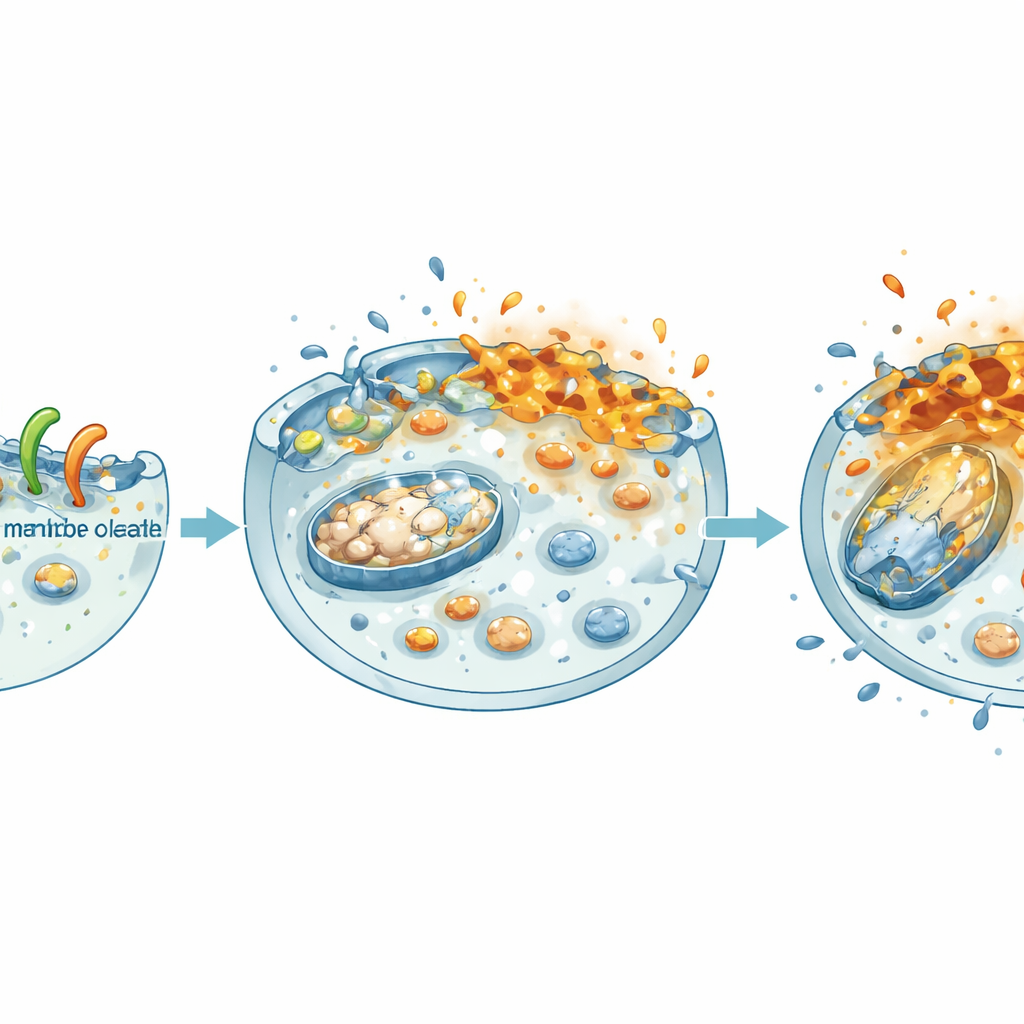
כיבוי תחנות הכוח ותכניות הגידול של התא
ברגע ש‑NheA–O מפריע לממברנה, הנזק מתפשט פנימה. הצוות מצא שהתאים המטופלים איבדו את המטען החשמלי על פני המיטוכונדריה—תחנות הכוח הקטנות בתוך התאים—ומאגרי האנרגיה שלהם (ATP) נפלו בצורה חדה, הן בתרביות שטח והן בספירואידים תלת‑ממדיים. במקביל, הקומפלקס החליש מנגנון צמיחה מרכזי בסרטן המעי הגס: מסלול ה‑β‑קטנין. בנתוני חולים, רמות גבוהות של β‑קטנין ושותפיו מקושרות להישרדות ירודה. במעבדה, NheA–O הפחית את כמות ה‑β‑קטנין בגרעין, הוריד את פעילותו והקטין את רמות היעדים המעודדים צמיחה. כתוצאה מכך, תאי הגידול יצרו פחות מושבות, נדדו לאט יותר ובנו ספירואידים קטנים וחלשים יותר—מאפיינים המתורגמים להפחתת התפשטות והתרבות הגידול.
הפעלת מוות דמוי‑חלודה בממברנות הגידול
ממצא מרכזי בעבודה זו הוא ש‑NheA–O מפעיל סוג מיוחד של מוות תאי הידוע כפרופרוטוזה (ferroptosis), הדומה לתהליך חימצון של שומני התא בדומה לחלודה. הקומפלקס העלה את רמות ACSL4, חלבון שמעשיר ממברנות בחומצות שומן רגישות, בעוד שהפחית את GPX4, אנזים קריטי שמונע בדרך כלל חמצון של שומנים אלה. ככל שרמות GPX4 ירדו, סימנים כימיים לנזק לליפידים בממברנות זינקו. תרופות המגבירות פרופרוטוזה הפכו את NheA–O לקטלני אף יותר, בעוד שחוסם פרופרוטוזה הציל חלקית את התאים, הקטין את נזקי הממברנה והשיב במידה מה פעילות β‑קטנין. ניסויים נוספים הראו כי NheA–O מקדם תג‑תווית של GPX4 לסילוק על‑ידי מערכת פירוק החלבונים של התא, וכי תאים שכבר סובלים מדלדול GPX4 היו קלים במיוחד להשמדה.
מה משמעות הדבר עבור טיפולים עתידיים
בצירוף כללי, הממצאים חושפים מנגנון פעולה מרובה־זרועות: NheA–O נצמד לממברנות תאי הגידול, מפר את שלמותן, מרוקן את תחנות האנרגיה שלהם ומאלץ מוות דמוי‑פרופרוטוזה על‑ידי פירוק מערכת ההגנה GPX4 ושתקת אותות הצמיחה המונעים על‑ידי β‑קטנין. מאחר שהוא פוגע בכמה חולשות בו־זמנית ומשאיר ברוב המקרים את תאי הקולון הנורמליים בתרביות במידה רבה של חסינות, קומפלקס חלבון‑שומן חיידקי זה מצטייר כתבנית מבטיחה לטיפולים חדשים בסרטן המעי הגס. למרות שהתוצאות הללו נובעות מדגמי תאים מבוקרים בקפידה וכעת יצטרכו להיבדק בחיות ובסופו של דבר בבני אדם, הן מרחיבות את הרעיון שלקומפלקסים פשוטים של חלבון‑ליפיד—מחלב או ממיקרובים—ניתן להנדס להיות סוכני אנטי‑סרטן מדויקים ועצמתיים.
ציטוט: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
מילות מפתח: סרטן המעי הגס, פרופרוטוזה (ferroptosis), חלבון חיידקי, פגיעה בממברנת התא, GPX4 ו‑β‑קטנין