Clear Sky Science · fr
Des complexes protéine-oléate bactériens induisent une mort cellulaire de type ferroptose dans des cellules de cancer colorectal en perturbant les membranes cellulaires et en inhibant l’axe β-caténine-GPX4
Transformer des bactéries en combattants du cancer
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde et parvient souvent à échapper aux traitements standards. Cette étude explore un allié inattendu dans la lutte contre ces tumeurs : une protéine bactérienne inoffensive qui, associée à une molécule lipidique courante, peut tuer sélectivement les cellules de cancer colorectal. En comprenant comment ce complexe protéine‑lipide attaque les cellules tumorales tout en épargnant en grande partie les cellules saines, les chercheurs espèrent ouvrir une nouvelle voie vers des thérapies à la fois plus efficaces et plus douces pour les patients.
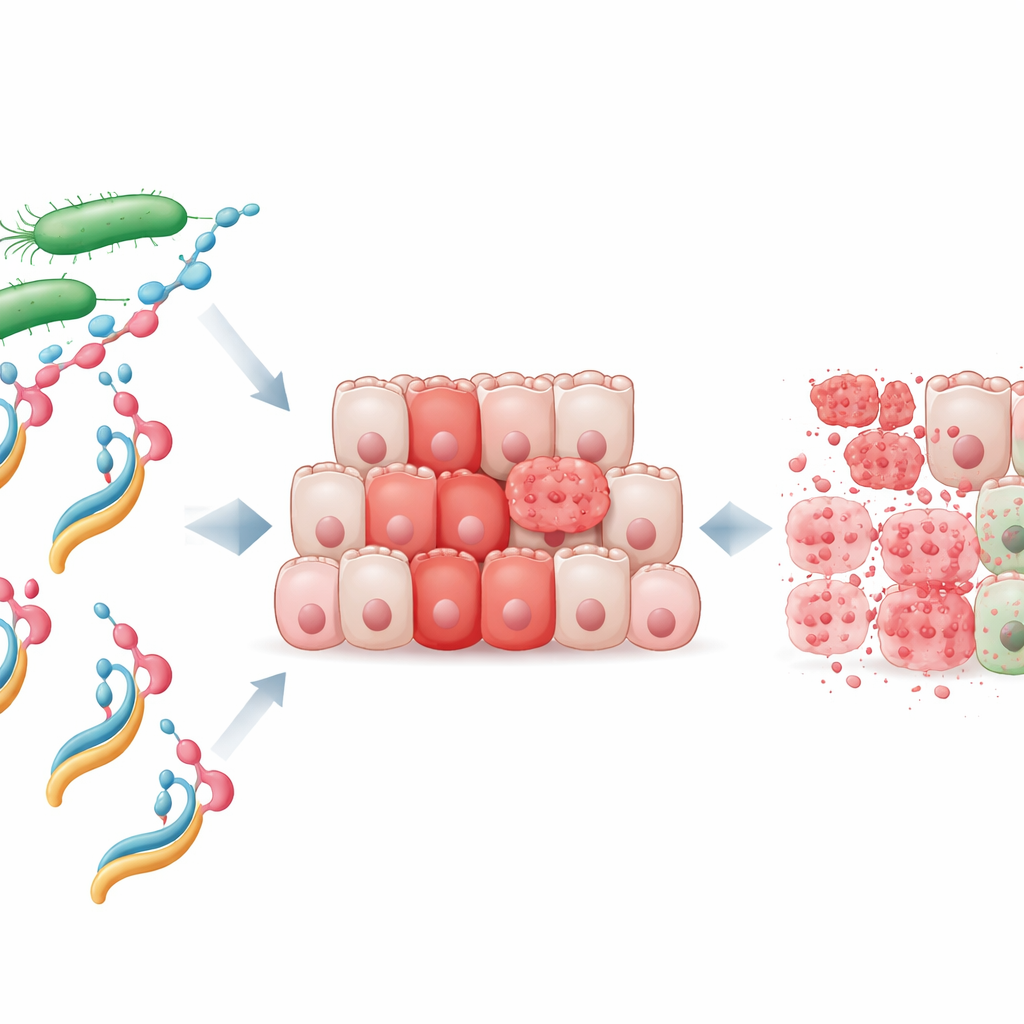
Une nouvelle arme constituée de protéine et de lipide
Les chercheurs se sont concentrés sur une protéine bactérienne appelée NheA, qui isolée est inoffensive et ne peut même pas s’attacher aux cellules humaines. Ils ont mélangé la NheA purifiée avec de l’oléate de sodium, une molécule dérivée d’un acide gras, pour créer ce qu’ils nomment le complexe NheA–O. Des complexes protéine‑lipide humains similaires, tels que le HAMLET dérivé du lait, sont connus pour tuer des cellules cancéreuses, mais jusqu’à présent personne n’avait montré qu’une protéine bactérienne pouvait être transformée en un agent antitumoral comparable. Les tests en laboratoire ont révélé que NheA–O réduisait rapidement la survie de lignées cellulaires de cancer colorectal, alors que les ingrédients individuels — protéine ou lipide seuls — avaient peu d’effet. Il est important de noter que les cellules normales du côlon étaient beaucoup moins sensibles, ce qui suggère que les cellules tumorales présentent une vulnérabilité particulière que ce complexe peut exploiter.
Attaque directe à la surface des cellules tumorales
À l’aide d’imagerie avancée, l’équipe a observé le comportement de NheA–O au contact des cellules cancéreuses. Des versions marquées du complexe brillaient intensément autour de la surface externe des cellules tumorales, montrant qu’il se lie fermement à leurs membranes. Des images tridimensionnelles d’amas cellulaires (sphéroïdes) ont confirmé que NheA–O peut pénétrer en profondeur dans des structures de type tumoral. Pour isoler ce qui se passe à la surface, les chercheurs ont créé de gigantesques bulles membranaires à partir de cellules cancéreuses et les ont exposées à NheA–O. Le complexe s’est agrégé sur ces bulles, a réduit leur surface et a permis à des molécules de colorant normalement exclues de s’infiltrer. Des tests supplémentaires avec des gouttelettes lipidiques artificielles fabriquées à partir des lipides des cellules tumorales ont montré que NheA–O provoquait des fuites progressives, indiquant qu’il déstabilise physiquement et perfore les membranes des cellules cancéreuses.
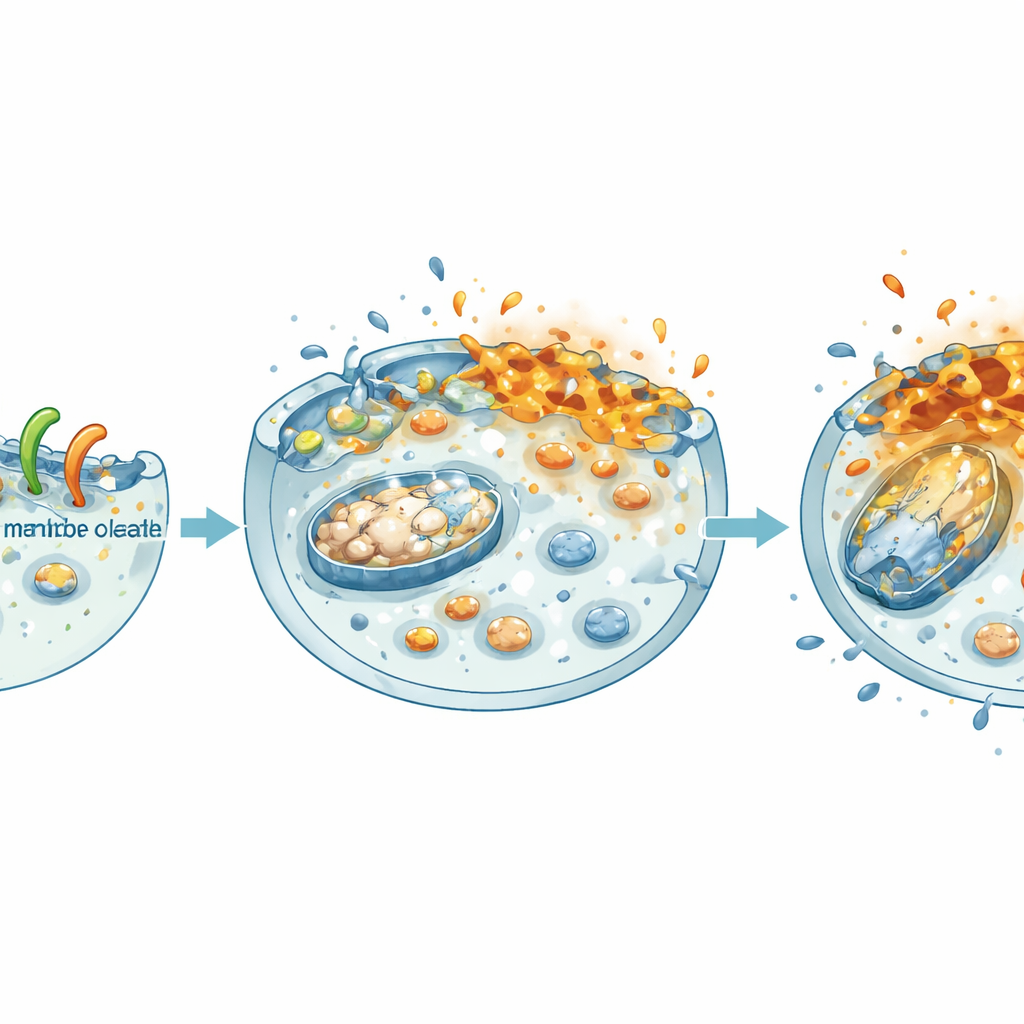
Mettre hors service l’énergie et les programmes de croissance cellulaires
Une fois que NheA–O perturbe la membrane, les dommages se propagent vers l’intérieur. L’équipe a constaté que les cellules tumorales traitées perdaient la charge électrique à travers leurs mitochondries — les petites centrales énergétiques intracellulaires — et que leurs réserves d’énergie globales (ATP) chutaient fortement, tant en culture à plat que dans des sphéroïdes 3D. Parallèlement, le complexe affaiblissait un moteur central de croissance dans le cancer colorectal : la voie β‑caténine. Dans les données de patients, des niveaux élevés de β‑caténine et de ses partenaires sont liés à une survie défavorable. En laboratoire, NheA–O réduisait la quantité de β‑caténine dans le noyau, diminuait son activité et abaissait les niveaux de ses cibles favorisant la croissance. En conséquence, les cellules tumorales formaient moins de colonies, migraient plus lentement et construisaient des sphéroïdes plus petits et plus fragiles — des caractéristiques qui se traduisent par une expansion et une dissémination tumorales réduites.
Forcer une mort des membranes tumorales de type « rouille »
Une découverte clé de ce travail est que NheA–O déclenche un type particulier de mort cellulaire connu sous le nom de ferroptose, qui ressemble à un processus d’oxydation des lipides des cellules. Le complexe augmentait les niveaux d’ACSL4, une protéine qui enrichit les membranes en composants lipidiques vulnérables, tout en réduisant GPX4, une enzyme cruciale « pompier » qui empêche normalement ces lipides de s’oxyder. À mesure que les niveaux de GPX4 diminuent, des marqueurs chimiques de dommages lipidiques dans les membranes augmentent fortement. Des médicaments qui renforcent la ferroptose rendaient NheA–O encore plus létal, tandis qu’un bloqueur de ferroptose sauvait partiellement les cellules, réduisait les lésions membranaires et restaurait une partie de l’activité de β‑caténine. Des expériences supplémentaires ont montré que NheA–O favorise le marquage de GPX4 en vue de sa destruction par la machinerie cellulairе d’élimination des protéines, et que les cellules déjà appauvries en GPX4 étaient particulièrement faciles à tuer.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, les résultats révèlent un mode d’action multi‑facettes : NheA–O s’accroche aux membranes des cellules tumorales, en perturbe l’intégrité, tarit leurs centrales énergétiques et provoque une mort de type ferroptose en démantelant le système protecteur GPX4 et en étouffant les signaux de croissance pilotés par β‑caténine. Parce qu’il cible plusieurs vulnérabilités à la fois et épargne en grande partie les cellules normales du côlon en culture, ce complexe protéine‑lipide bactérien apparaît comme un modèle prometteur pour de nouvelles thérapies contre le cancer colorectal. Bien que ces résultats proviennent de modèles cellulaires rigoureusement contrôlés et devront maintenant être testés chez l’animal puis, éventuellement, chez l’humain, ils élargissent le concept selon lequel de simples complexes protéine‑lipide — du lait ou de microbes — peuvent être conçus en agents anticancéreux précis et puissants.
Citation: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Mots-clés: cancer colorectal, ferroptose, protéine bactérienne, perturbation de la membrane cellulaire, GPX4 et β-caténine