Clear Sky Science · pl
Kompleksy białko‑oleinianowe bakterii wywołują śmierć komórek przypominającą ferroptozę w komórkach raka jelita grubego przez uszkadzanie błon komórkowych i hamowanie osi β‑katenina‑GPX4
Przekształcanie bakterii w sojuszników w walce z rakiem
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie i często potrafi uniknąć standardowych terapii. W badaniu tym analizowano niespodziewanego sprzymierzeńca w walce z tymi guzami: niegroźne białko bakteryjne, które w połączeniu z powszechną cząsteczką tłuszczową może selektywnie zabijać komórki raka jelita grubego. Zrozumienie, w jaki sposób kompleks białko–tłuszcz atakuje komórki nowotworowe, jednocześnie w dużej mierze oszczędzając komórki zdrowe, może otworzyć nową drogę do terapii skuteczniejszych i łagodniejszych dla pacjentów.
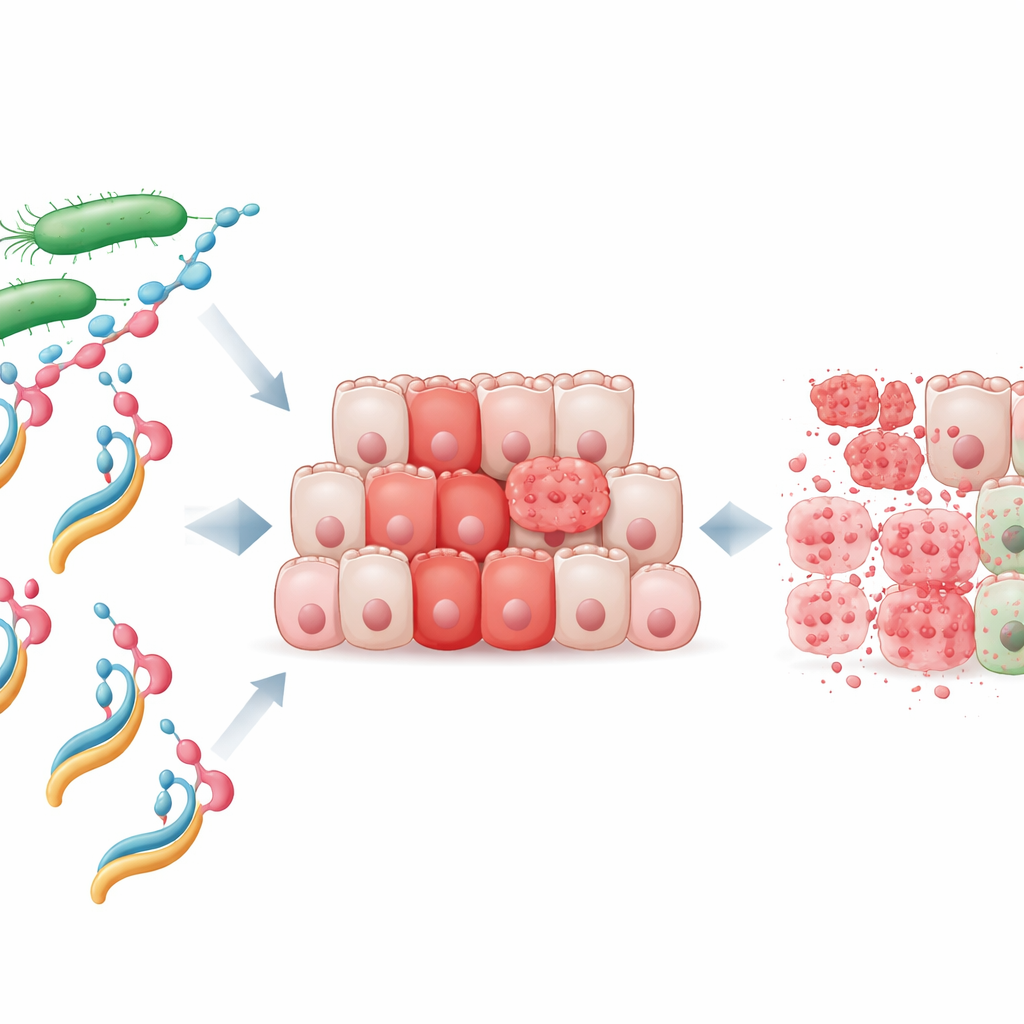
Nowa broń zbudowana z białka i tłuszczu
Naukowcy skupili się na białku bakteryjnym zwanym NheA, które samo w sobie jest niegroźne i nie potrafi nawet przyczepić się do komórek ludzkich. Oczyszczone NheA zmieszano z oleinianem sodu, cząsteczką pochodzącą od kwasu tłuszczowego, tworząc tzw. kompleks NheA–O. Podobne kompleksy białko‑tłuszcz pochodzenia ludzkiego, jak HAMLET z mleka, są znane z niszczenia komórek nowotworowych, ale dotąd nie wykazano, że białko bakteryjne można przekształcić w porównywalną broń przeciwnowotworową. Testy laboratoryjne pokazały, że NheA–O szybko zmniejsza przeżywalność linii komórek raka jelita grubego, podczas gdy poszczególne składniki — białko lub tłuszcz osobno — miały niewielki efekt. Co ważne, normalne komórki jelita były znacznie mniej wrażliwe, co sugeruje, że komórki nowotworowe mają specyficzną słabość, którą ten kompleks może wykorzystać.
Bezpośredni atak na powierzchnię komórek nowotworowych
Dzięki zaawansowanym metodom obrazowania zespół obserwował zachowanie NheA–O w kontakcie z komórkami nowotworowymi. Znakowane wersje kompleksu jasno świeciły w rejonie zewnętrznej powierzchni komórek nowotworowych, wykazując silne wiązanie z ich błonami. Trójwymiarowe obrazy skupisk komórkowych (sferoidów) potwierdziły, że NheA–O potrafi penetrować głęboko do struktur przypominających guzy. Aby wyizolować zdarzenia zachodzące na powierzchni, badacze stworzyli olbrzymie pęcherze błonowe z komórek nowotworowych i wystawili je na działanie NheA–O. Kompleks grupował się na tych pęcherzach, zmniejszał ich powierzchnię i umożliwiał przenikanie barwników, które normalnie są wykluczone. Dodatkowe testy z sztucznymi kroplami tłuszczu z lipidów komórek nowotworowych wykazały, że NheA–O powodował postępujące przecieki, co wskazuje, że fizycznie destabilizuje i perforuje błony komórek nowotworowych.
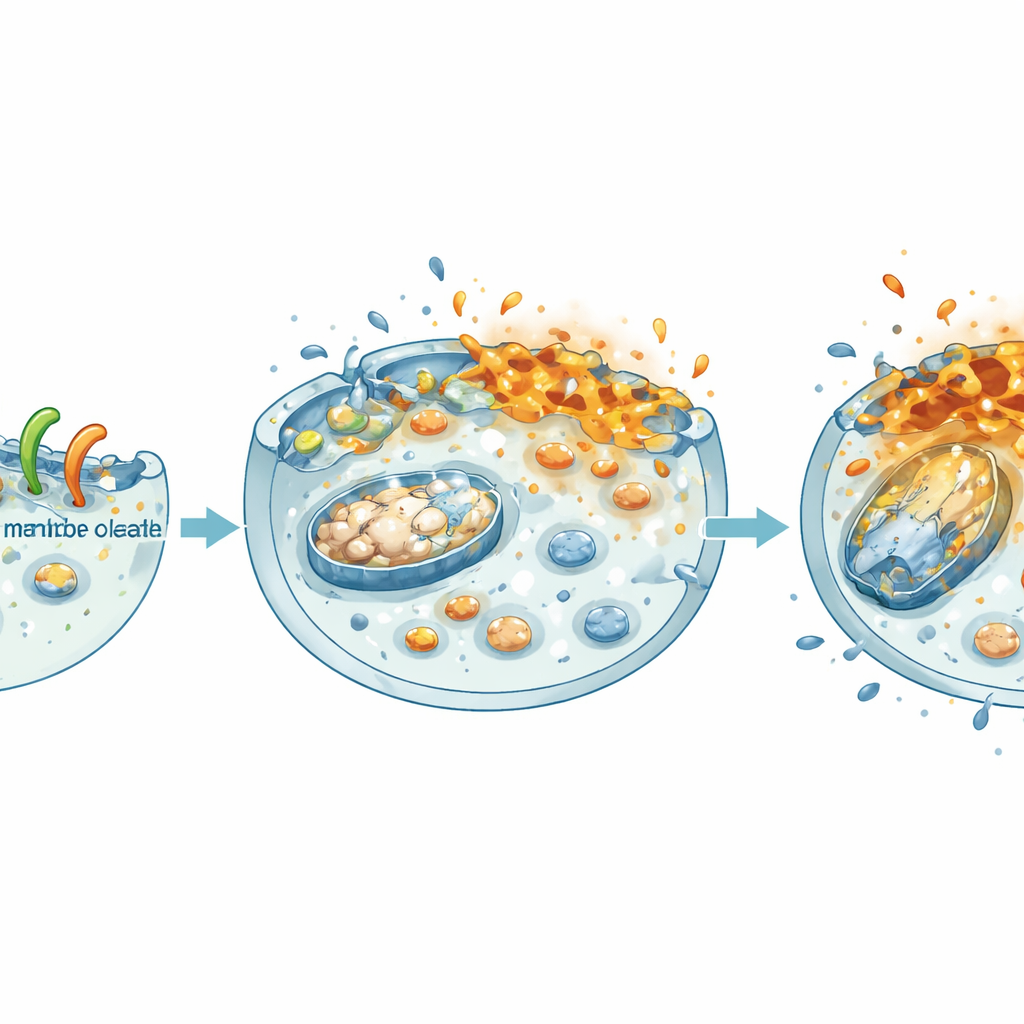
Wyłączanie „elektrowni” i programów wzrostu komórki
Gdy NheA–O narusza błonę, uszkodzenia rozprzestrzeniają się do wnętrza komórki. Zespół odkrył, że traktowane komórki nowotworowe utraciły potencjał elektryczny mitochondriów — maleńkich elektrowni komórkowych — a ich ogólne zasoby energetyczne (ATP) gwałtownie spadły, zarówno w hodowlach płaskich, jak i w sferoidach 3D. Jednocześnie kompleks osłabił centralny regulator wzrostu w raku jelita grubego: szlak β‑kateniny. W danych klinicznych wysokie poziomy β‑kateniny i jej partnerów korelują z gorszym przeżyciem. W warunkach laboratoryjnych NheA–O zmniejszał ilość β‑kateniny w jądrze, obniżał jej aktywność i redukował poziomy genów promujących wzrost zależnych od tego szlaku. W efekcie komórki nowotworowe tworzyły mniej kolonii, migrowały wolniej i budowały mniejsze, słabsze sferoidy — cechy przekładające się na ograniczone rozprzestrzenianie i wzrost guza.
Wymuszanie „zardzewienia” błon nowotworowych
Kluczowym odkryciem pracy jest to, że NheA–O wywołuje specyficzny rodzaj śmierci komórki znany jako ferroptoza, przypominający proces rdzewienia w tłuszczach komórkowych. Kompleks podnosił poziomy ACSL4, białka wzbogacającego błony w podatne na utlenianie kwasy tłuszczowe, jednocześnie obniżając GPX4 — kluczową „strażakową” enzymatyczną barierę, która normalnie zapobiega utlenianiu tych lipidów. W miarę spadku poziomów GPX4 nasilały się chemiczne markery uszkodzeń lipidów w błonach. Leki wzmacniające ferroptozę uczyniły NheA–O jeszcze bardziej śmiertelnym, podczas gdy inhibitor ferroptozy częściowo ratował komórki, zmniejszał uszkodzenia błon i przywracał część aktywności β‑kateniny. Dalsze eksperymenty wykazały, że NheA–O sprzyja znakowaniu GPX4 do degradacji przez komórkowe mechanizmy rozkładu białek, a komórki już pozbawione GPX4 były szczególnie podatne na zabijanie.
Co to może znaczyć dla przyszłych terapii
Podsumowując, wyniki ujawniają wieloaspektowy mechanizm działania: NheA–O przyczepia się do błon komórek nowotworowych, zaburza ich integralność, wyczerpuje ich „elektrownie” i wymusza śmierć przypominającą ferroptozę przez rozmontowanie ochronnego systemu GPX4 oraz wyciszenie sygnałów wzrostu zależnych od β‑kateniny. Ponieważ trafia jednocześnie w kilka słabości i w hodowlach komórkowych w dużej mierze oszczędza normalne komórki jelita, ten bakteryjno‑lipidowy kompleks jawi się jako obiecujący wzorzec do opracowania nowych terapii raka jelita grubego. Choć wyniki pochodzą z kontrolowanych modeli komórkowych i będą musiały zostać przetestowane na zwierzętach, a w końcu u ludzi, rozszerzają koncepcję, że proste kompleksy białko‑lipid — z mleka lub drobnoustrojów — można zaprojektować jako precyzyjne, silne środki przeciwnowotworowe.
Cytowanie: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Słowa kluczowe: rak jelita grubego, ferroptoza, białko bakteryjne, uszkodzenie błony komórkowej, GPX4 i β‑katenina