Clear Sky Science · ru
Комплексы бактериального белка с олеатом индуцируют гибель колоректальных раковых клеток, напоминающую ферроптоз, нарушая клеточные мембраны и ингибируя ось β-катенин–GPX4
Превращение бактерий в борцов с раком
Колоректальный рак — один из самых распространённых видов рака в мире, и он часто вырабатывает способы уклоняться от стандартных терапий. В этом исследовании рассматривается неожиданный союзник в борьбе с этими опухолями: безвредный бактериальный белок, который в сочетании с распространённой жирной молекулой способен селективно уничтожать клетки колоректального рака. Поняв, как этот белково-жировой комплекс атакует опухолевые клетки, при этом в значительной степени щадя здоровые, исследователи надеются открыть новый путь к терапиям, которые будут одновременно более эффективными и более мягкими для пациентов.
Новое оружие из белка и жира
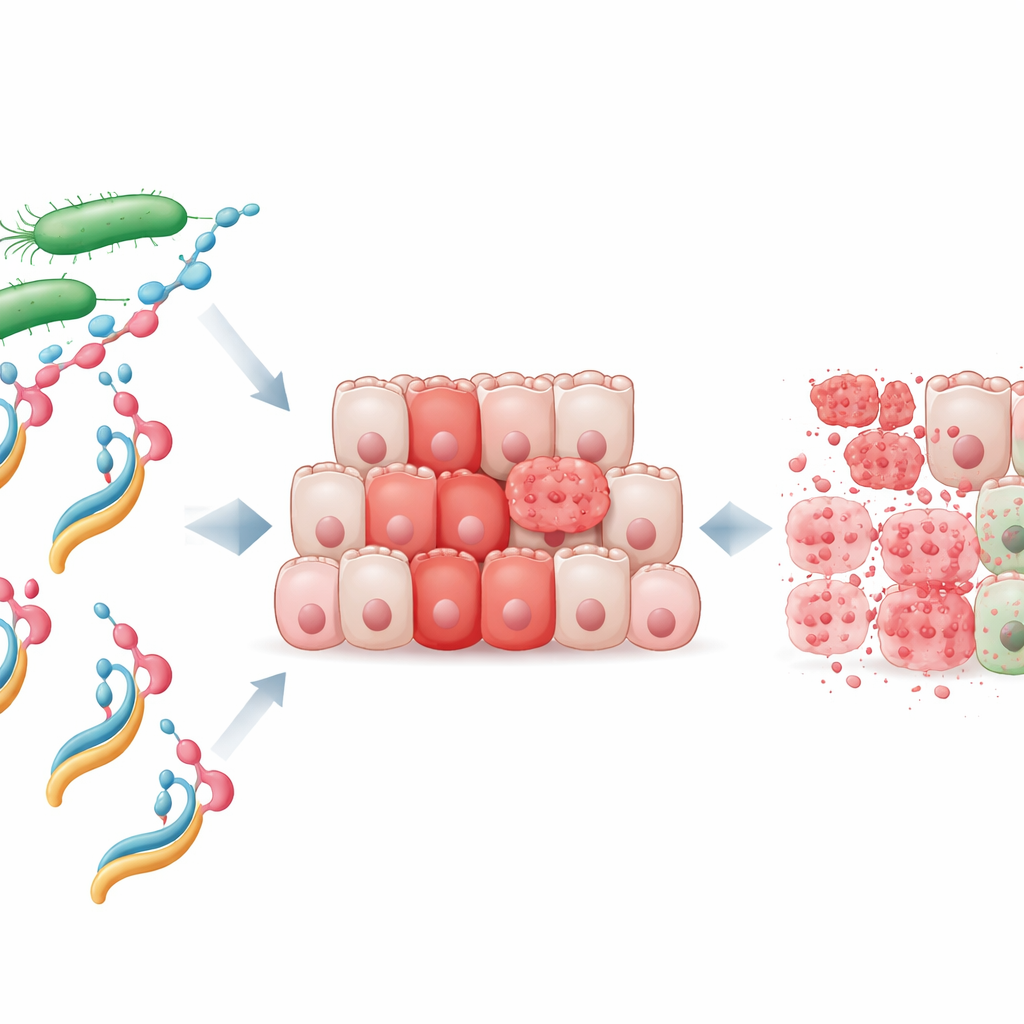
Исследователи сосредоточились на бактериальном белке под названием NheA, который сам по себе безвреден и даже не способен прочно прикрепляться к человеческим клеткам. Они смешали очищенный NheA с натриевой олеатом — молекулой, полученной из жирной кислоты — чтобы создать так называемый комплекс NheA–O. Сходные человеческие белково-жировые комплексы, например молочный HAMLET, известны своей способностью убивать раковые клетки, но до настоящего момента не было показано, что бактериальный белок может быть превращён в сопоставимый убийцу опухолей. Лабораторные тесты показали, что NheA–O быстро снижает выживаемость линий колоректальных раковых клеток, тогда как отдельные компоненты — только белок или только жир — оказывали незначительный эффект. Важно, что нормальные клетки толстой кишки были значительно менее чувствительны, что указывает на особую уязвимость опухолевых клеток, которую может использовать этот комплекс.
Прямой удар по поверхности опухолевой клетки
С помощью продвинутой визуализации команда наблюдала поведение NheA–O при контакте с раковыми клетками. Меченые версии комплекса ярко светились вокруг наружной поверхности опухолевых клеток, показывая, что он прочно связывается с их мембранами. Трёхмерные изображения клеточных кластеров (сфероидов) подтвердили, что NheA–O может проникать глубоко в структуры, подобные опухоли. Чтобы изолировать события на поверхности, исследователи создали гигантские мембранные пузыри из раковых клеток и подвергли их воздействию NheA–O. Комплекс собирался в кластеры на этих пузырях, уменьшал их площадь и позволял проникать внутрь красителям, которые обычно удерживаются снаружи. Дополнительные испытания с искусственными жировыми каплями, сделанными из липидов опухолевых клеток, показали, что NheA–O вызывает прогрессирующее просачивание, что свидетельствует о том, что он физически дестабилизирует и перфорирует мембраны раковых клеток.
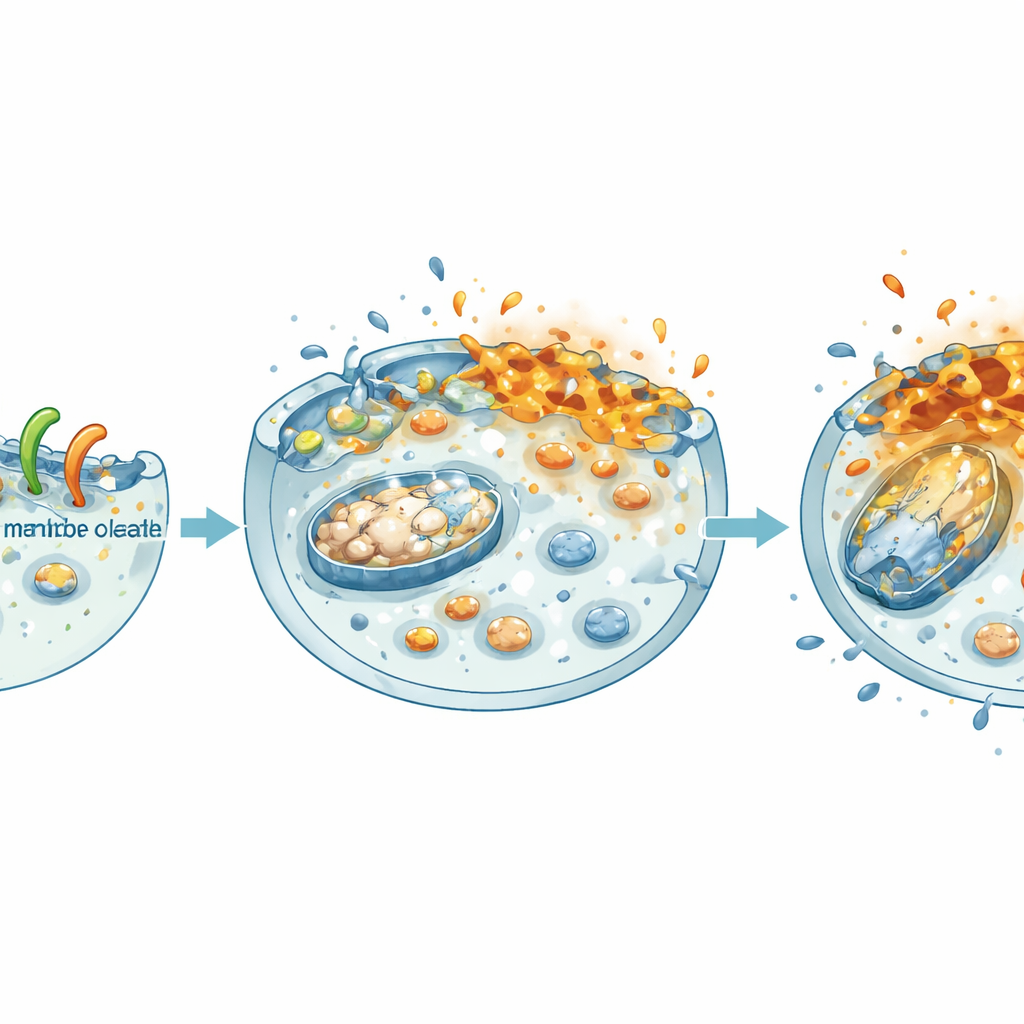
Отключение энергетических и ростовых программ клетки
Как только NheA–O нарушает мембрану, повреждение распространяется внутрь клетки. Команда обнаружила, что обрабатываемые клетки теряли электрический потенциал митохондрий — крошечных энергетических станций внутри клетки — и общий запас энергии (АТФ) резко падал, как в двумерных культурах, так и в 3D-сфероидах. Одновременно комплекс ослаблял центральный фактор роста при колоректальном раке: путь β‑катенин. В данных пациентов высокие уровни β‑катенина и его партнёров связаны с худшим выживанием. В лаборатории NheA–O снижал количество β‑катенина в ядре, уменьшал его активность и понижал уровни его стимулирующих рост мишеней. В результате опухолевые клетки образовывали меньше колоний, мигрировали медленнее и формировали меньшие, слабее структурированные сфероиды — характеристики, которые переводятся в замедленное расширение и распространение опухоли.
Вынуждение «ржавой» смерти в мембранах опухоли
Ключевое открытие этой работы состоит в том, что NheA–O вызывает особый тип гибели клеток, известный как ферроптоз, который напоминает процесс «ржавления» липидов клетки. Комплекс повышал уровни ACSL4 — белка, обогащающего мембраны уязвимыми жирными компонентами — одновременно снижая GPX4, ключевую «пожарную» ферментативную систему, которая обычно предотвращает окисление этих жиров. По мере снижения уровня GPX4 химические маркеры липидного повреждения в мембранах резко возрастали. Препараты, усиливающие ферроптоз, делали NheA–O ещё более летальным, тогда как блокатор ферроптоза частично спасал клетки, уменьшал повреждение мембраны и восстанавливал часть активности β‑катенина. Дальнейшие эксперименты показали, что NheA–O способствует мишенированию GPX4 для разрушения клеточной системой протеолиза, и что клетки с уже пониженным уровнем GPX4 особенно легко подвергались уничтожению.
Что это может значить для будущих методов лечения
В совокупности результаты раскрывают многосторонний механизм действия: NheA–O прикрепляется к мембранам опухолевых клеток, нарушает их целостность, истощает их энергетические станции и вызывает гибель, похожую на ферроптоз, разрушая защитную систему GPX4 и подавляя ростовые сигналы, управляемые β‑катенином. Поскольку комплекс затрагивает несколько уязвимостей одновременно и в культуре в значительной степени щадит нормальные клетки толстой кишки, этот бактериально-жировой белково-комплекс представляет собой перспективный шаблон для новых терапий колоректального рака. Хотя эти результаты получены в строго контролируемых клеточных моделях и теперь должны быть проверены на животных, а затем и на людях, они расширяют представление о том, что простые белково-липидные комплексы — из молока или микробов — можно сконструировать как точные и мощные противораковые агенты.
Цитирование: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Ключевые слова: колоректальный рак, ферроптоз, бактериальный белок, нарушение клеточной мембраны, GPX4 и β-катенин