Clear Sky Science · ja
細菌由来タンパク質―オレイン酸複合体は細胞膜を破壊しβ-カテニン–GPX4軸を阻害して大腸がん細胞でフェロトーシス様の細胞死を誘導する
細菌をがん治療の味方に変える
大腸がんは世界的に多いがんの一つであり、しばしば標準治療を回避する手段を獲得します。本研究は、この腫瘍と戦う思いがけない味方を探ります。それは無害な細菌由来のタンパク質で、一般的な脂肪性分子と組み合わせると選択的に大腸がん細胞を死に導くことができます。このタンパク質―脂質複合体がどのように腫瘍細胞を攻撃し、健康な細胞を大きく傷つけずに済むのかを解明することで、より効果的で患者に優しい治療法への新たな道を開くことが期待されます。
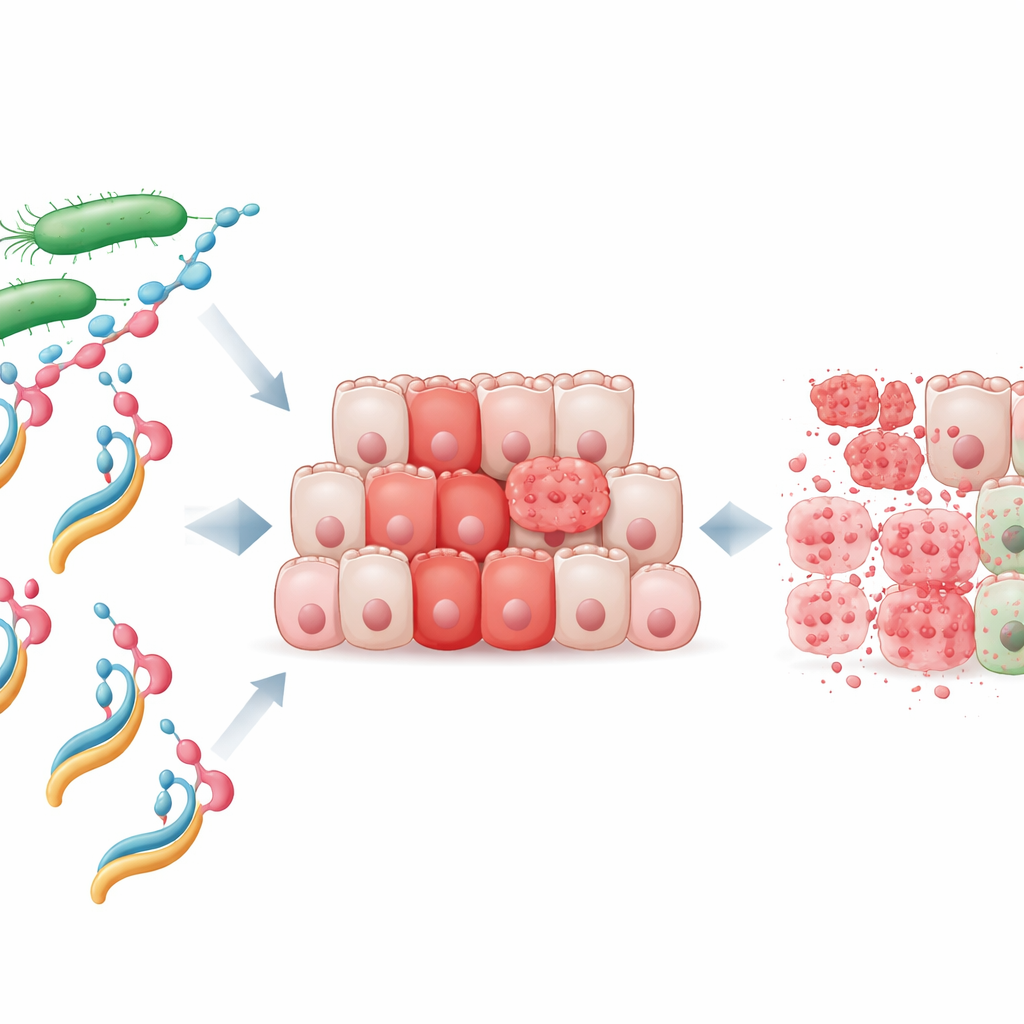
タンパク質と脂肪から作られた新たな武器
研究者らはNheAと呼ばれる細菌由来タンパク質に着目しました。単独では無害でヒト細胞に結合できないこのタンパク質を精製し、脂肪酸由来の分子であるオレイン酸ナトリウムと混ぜることで、NheA–Oと呼ぶ複合体を作製しました。牛乳由来のHAMLETのように、ヒト由来のタンパク質―脂質複合体ががん細胞を死滅させることは知られていましたが、細菌由来タンパク質が同等の腫瘍殺傷能を持ちうることが示されたのは今回が初めてです。培養実験ではNheA–Oが大腸がん細胞株の生存率を迅速に低下させた一方で、タンパク質単独や脂質単独ではほとんど効果がありませんでした。重要なのは、正常な結腸細胞ははるかに感受性が低く、腫瘍細胞に特有の脆弱性をこの複合体が突いていることを示唆しています。
腫瘍細胞表面への直接攻撃
高解像度イメージングを用いて、研究チームはNheA–Oががん細胞と出会ったときの振る舞いを観察しました。標識された複合体は腫瘍細胞の外側表面周辺に強く光り、膜にしっかり結合することを示しました。細胞塊(スフェロイド)の三次元画像は、NheA–Oが腫瘍様構造の奥深くまで浸透できることを確認しました。表面で何が起きるかを孤立させるために、研究者らはがん細胞由来の巨大膜胞(ジャイアントエレクトロポア膜)を作製し、NheA–Oに曝露しました。複合体はこれらの膜上に凝集し、膜面積を縮小させ、通常は侵入を許さない色素の流入を可能にしました。がん細胞由来の脂質から作った人工的な脂滴に対する追加試験でも、NheA–Oは進行性の漏出を引き起こし、がん細胞膜を物理的に不安定化し穿孔することを示しました。
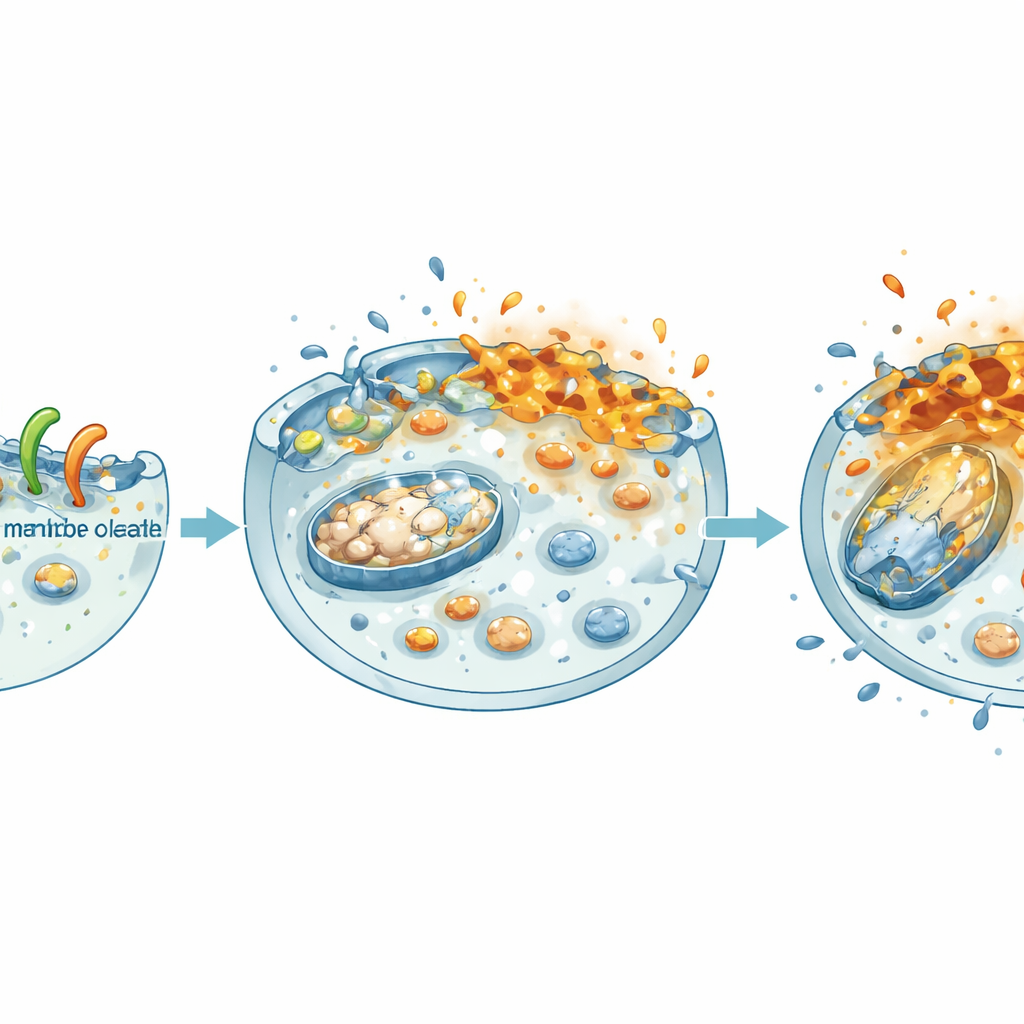
細胞のエネルギーと増殖プログラムを停止させる
NheA–Oが膜を攪乱すると、損傷は内側へ広がります。処理されたがん細胞ではミトコンドリア膜電位が失われ(細胞内の小さな発電所の電位低下)、ATPといった全体的なエネルギー貯蔵が平面培養と3Dスフェロイドの双方で急激に減少しました。同時に、この複合体は大腸がんで中心的な増殖ドライバーであるβ‑カテニン経路を弱めました。患者データでは、β‑カテニンとその共役因子の高発現が予後不良と関連しており、実験室ではNheA–Oは核内のβ‑カテニン量を低下させ、その活性を下げ、増殖を促す標的遺伝子の発現を減少させました。その結果、腫瘍細胞はコロニー形成能が低下し、移動速度が遅くなり、より小さく脆弱なスフェロイドを形成しました。これらは腫瘍の拡大と転移が抑えられることを意味します。
腫瘍膜にさび付くような死を強いる
本研究の重要な発見は、NheA–Oがフェロトーシスと呼ばれる脂質が酸化していく「さびつき」のような特殊な細胞死を誘導することです。複合体は膜を脆弱な脂質で豊富にするタンパク質ACSL4の量を増やし、一方でこれらの脂質の酸化を通常抑える重要な“消火役”酵素GPX4の量を低下させました。GPX4が減ると膜中の脂質損傷の化学的指標が急上昇しました。フェロトーシスを促進する薬剤はNheA–Oの致死性をさらに高めたのに対し、フェロトーシス阻害剤は細胞を部分的に救い、膜損傷を軽減し、いくつかのβ‑カテニン活性を回復させました。追加実験により、NheA–OがGPX4を細胞のタンパク質分解機構向けにタグ付けして破壊させることを促進し、GPX4が既に枯渇している細胞は特に殺されやすいことが示されました。
将来の治療にとっての意義
総じて、これらの所見は多面的な作用機序を明らかにします:NheA–Oは腫瘍細胞膜に結合してその一体性を破壊し、エネルギー生産を枯渇させ、保護的なGPX4システムを解体してβ‑カテニン主導の増殖シグナルを沈黙させることで、フェロトーシス様の死を強制します。複数の脆弱点を同時に突き、培養系では正常な結腸細胞を大部分で生き残らせることから、この細菌由来タンパク質―脂質複合体は新しい大腸がん治療の有望なテンプレートとして浮上します。これらの結果は厳密に制御された細胞モデルから得られたものであり、今後は動物実験や最終的にはヒトでの検証が必要ですが、牛乳由来でも微生物由来でも、単純なタンパク質―脂質複合体を精密で強力な抗がん剤へと設計できるという概念を拡げるものです。
引用: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
キーワード: 大腸がん, フェロトーシス, 細菌タンパク質, 細胞膜破壊, GPX4とβ-カテニン