Clear Sky Science · es
Complejos proteína-oleato bacterianos inducen una muerte celular parecida a la ferroptosis en células de cáncer colorrectal al alterar las membranas celulares e inhibir el eje β-catenina-GPX4
Convertir bacterias en combatientes contra el cáncer
El cáncer colorrectal es uno de los cánceres más comunes en todo el mundo y con frecuencia aprende a eludir los tratamientos estándar. Este estudio explora un aliado inesperado en la lucha contra estos tumores: una proteína bacteriana inocua que, al combinarse con una molécula grasa común, puede matar selectivamente células de cáncer colorrectal. Comprender cómo este complejo proteína–grasa ataca a las células tumorales mientras en gran medida preserva a las sanas podría abrir una nueva vía hacia terapias más efectivas y menos agresivas para los pacientes.
Un nuevo arma hecha de proteína y grasa
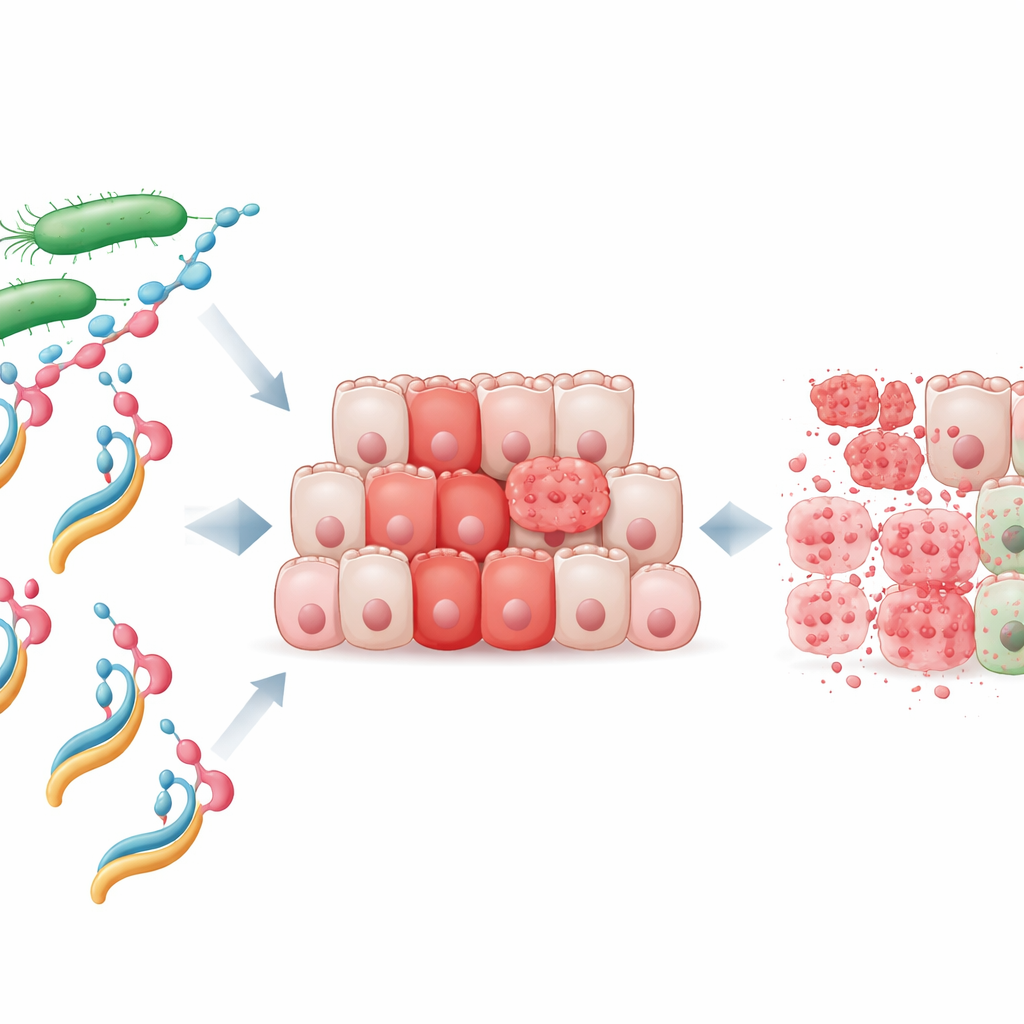
Los investigadores se centraron en una proteína bacteriana llamada NheA, que por sí sola es inocua e incluso no puede adherirse a las células humanas. Mezclaron NheA purificada con oleato de sodio, una molécula derivada de un ácido graso, para crear lo que denominan el complejo NheA–O. Complejos humanos similares proteína–grasa, como el HAMLET derivado de la leche, se sabe que matan células cancerosas, pero hasta ahora nadie había demostrado que una proteína bacteriana pudiera convertirse en un asesino tumoral comparable. Ensayos de laboratorio revelaron que NheA–O redujo rápidamente la supervivencia de líneas celulares de cáncer colorrectal, mientras que los ingredientes por separado—proteína o grasa sola—tuvieron poco efecto. De forma importante, las células normales del colon fueron mucho menos sensibles, lo que sugiere que las células tumorales presentan una vulnerabilidad especial que este complejo puede explotar.
Ataque directo a la superficie de la célula tumoral
Mediante imágenes avanzadas, el equipo observó cómo se comporta NheA–O cuando se encuentra con células cancerosas. Versiones marcadas del complejo brillaron intensamente alrededor de la superficie externa de las células tumorales, mostrando que se une con fuerza a sus membranas. Imágenes tridimensionales de agregados celulares (esferoides) confirmaron que NheA–O puede penetrar profundamente en estructuras similares a tumores. Para aislar lo que ocurre en la superficie, los investigadores crearon enormes burbujas de membrana a partir de células cancerosas y las expusieron a NheA–O. El complejo se agrupó en estas burbujas, redujo su área y permitió que moléculas de tinte normalmente excluidas se filtraran hacia el interior. Pruebas adicionales con gotas de grasa artificiales hechas de lípidos de células tumorales mostraron que NheA–O provocó una fuga progresiva, lo que indica que desestabiliza físicamente y perfora las membranas de las células cancerosas.
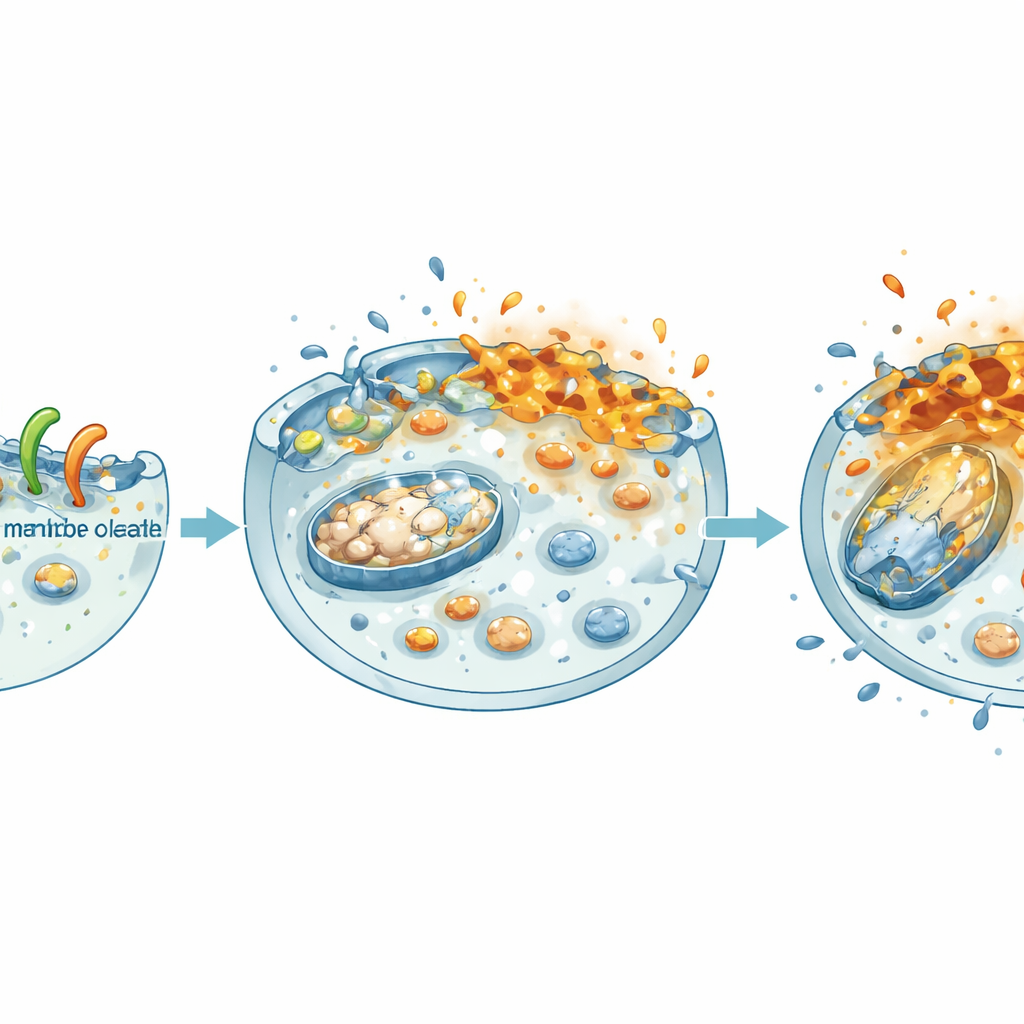
Apagar la energía y los programas de crecimiento de la célula
Una vez que NheA–O altera la membrana, el daño se extiende hacia el interior. El equipo encontró que las células cancerosas tratadas perdieron la diferencia de potencial a través de sus mitocondrias—las pequeñas centrales energéticas dentro de las células—y sus reservas energéticas generales (ATP) cayeron bruscamente, tanto en cultivos planos como en esferoides 3D. Al mismo tiempo, el complejo debilitó un impulsor central del crecimiento en el cáncer colorrectal: la vía de la β‑catenina. En datos de pacientes, niveles altos de β‑catenina y sus asociados se vinculan con una peor supervivencia. En el laboratorio, NheA–O redujo la cantidad de β‑catenina en el núcleo, disminuyó su actividad y redujo los niveles de sus dianas pro‑crecimiento. Como resultado, las células tumorales formaron menos colonias, migraron más despacio y construyeron esferoides más pequeños y débiles—características que se traducen en una menor expansión y diseminación tumoral.
Forzar una muerte tipo oxidación en las membranas tumorales
Un hallazgo clave de este trabajo es que NheA–O desencadena un tipo especial de muerte celular conocido como ferroptosis, que se asemeja a un proceso de oxidación (como el óxido) en las grasas de la célula. El complejo aumentó los niveles de ACSL4, una proteína que enriquece las membranas con bloques grasos vulnerables, mientras disminuía GPX4, una enzima crucial «bombero» que normalmente impide que estas grasas se oxiden. A medida que los niveles de GPX4 cayeron, los marcadores químicos de daño lipídico en las membranas se dispararon. Fármacos que potencian la ferroptosis hicieron que NheA–O fuera aún más letal, mientras que un bloqueador de la ferroptosis rescató parcialmente a las células, redujo el daño a la membrana y restauró algo de la actividad de β‑catenina. Experimentos adicionales mostraron que NheA–O promueve el marcado de GPX4 para su destrucción por la maquinaria celular de degradación de proteínas, y que las células ya privadas de GPX4 eran especialmente fáciles de eliminar.
Qué podría significar esto para tratamientos futuros
En conjunto, los hallazgos revelan un modo de acción multivectorial: NheA–O se adhiere a las membranas de las células tumorales, altera su integridad, agota sus centrales energéticas y provoca una muerte similar a la ferroptosis al desmantelar el sistema protector GPX4 y silenciar las señales de crecimiento impulsadas por β‑catenina. Dado que ataca varias vulnerabilidades a la vez y en cultivo respeta en gran medida a las células normales del colon, este complejo proteína–grasa bacteriano surge como un modelo prometedor para nuevas terapias contra el cáncer colorrectal. Aunque estos resultados proceden de modelos celulares cuidadosamente controlados y ahora deberán probarse en animales y, eventualmente, en humanos, amplían el concepto de que complejos simples proteína‑lípido—de la leche o de microbios—pueden ser diseñados como agentes anticancerígenos precisos y potentes.
Cita: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Palabras clave: cáncer colorrectal, ferroptosis, proteína bacteriana, alteración de la membrana celular, GPX4 y β-catenina