Clear Sky Science · ar
مركبات بروتين-الأوليات البكتيرية تحفّز موتًا خلوياً يشبه الفيروبتوزيس في خلايا سرطان القولون والمستقيم عن طريق تعطيل أغشية الخلايا وكبح محور β‑catenin‑GPX4
تحويل البكتيريا إلى مقاتلة للسرطان
يُعد سرطان القولون والمستقيم من أكثر أنواع السرطان شيوعًا في العالم وغالبًا ما يتعلّم كيف يتفادى العلاجات الاعتيادية. تستكشف هذه الدراسة حليفًا غير متوقع في مكافحة هذه الأورام: بروتين بكتيري غير ضار يمكن، عند اقترانه بجزيء دهن شائع، أن يقتل خلايا سرطان القولون والمستقيم بشكل انتقائي. من خلال فهم كيفية هجوم هذا المركب البروتيني‑الدهني على خلايا الورم مع الإبقاء إلى حد كبير على الخلايا السليمة، يأمل الباحثون في فتح طريق جديد لعلاجات أكثر فعالية وأقل ضررًا للمرضى.
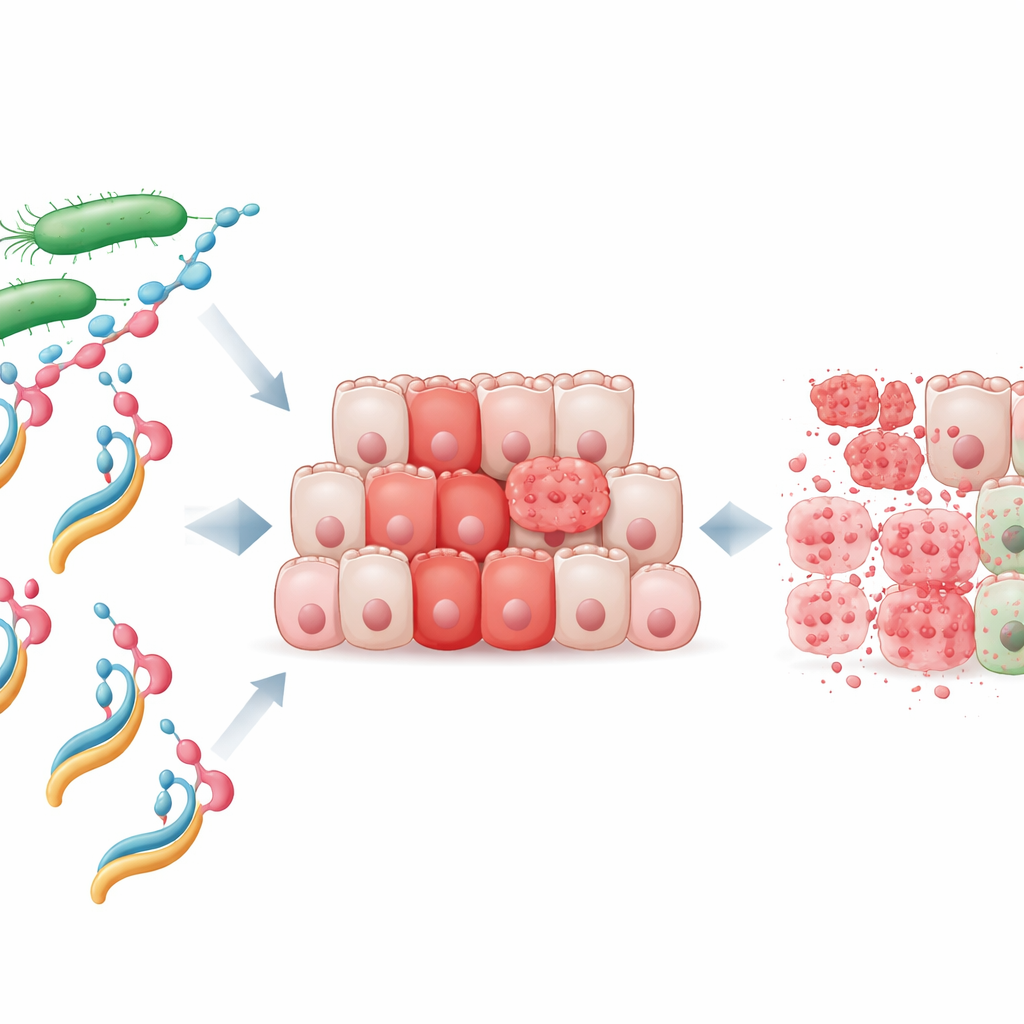
سلاح جديد مبني من بروتين ودهون
ركز الباحثون على بروتين بكتيري يُدعى NheA، والذي بمفرده غير ضار ولا يستطيع الالتصاق بالخلايا البشرية. مزجوا NheA النقي مع صوديوم الأوليات، وهو جزيء مشتق من حمض دهني، لابتكار ما أطلقوا عليه مركب NheA–O. تعرف مركبات بروتينية‑دهنية بشرية مماثلة، مثل HAMLET المستخرج من الحليب، بقدرتها على قتل الخلايا السرطانية، لكن حتى الآن لم يُظهر أحد أن بروتينًا بكتيريًا يمكن تحويله إلى قاتل للأورام مماثل. أظهرت الاختبارات المختبرية أن NheA–O خفض بسرعة قدرة خلايا خطوط سرطان القولون والمستقيم على البقاء، بينما كان للمكونات الفردية — البروتين أو الدهن وحدهما — تأثير ضئيل. والأهم أن خلايا القولون الطبيعية كانت أقل حساسية بكثير، ما يشير إلى أن خلايا الورم تمتلك نقطة ضعف خاصة يمكن أن يستغلها هذا المركب.
هجوم مباشر على سطح خلية الورم
باستخدام تقنيات تصوير متقدمة، راقب الفريق سلوك NheA–O عند مواجهته للخلايا السرطانية. أظهرت نسخ معنونة من المركب توهُّجًا قويًا حول السطح الخارجي لخلايا الورم، مما يدل على أنه يلتصق بغشائها بإحكام. وأكدت صور ثلاثية الأبعاد لمجموعات خلوية (كراتية) أن NheA–O قادر على اختراق هياكل شبيهة بالأورام بعمق. لعزل ما يحدث على السطح، أنشأ الباحثون فقاعات غشائية عملاقة من خلايا سرطانية وعرضوها لـ NheA–O. تجمّع المركب على هذه الفقاعات، قلّص مساحتها، وأتاح لجزيئات الصبغة التي تُستبعد عادة أن تتسرب إلى الداخل. اختبارات إضافية باستخدام قطرات دهنية اصطناعية مصنوعة من دهون خلايا الورم أظهرت أن NheA–O تسبب بتسرب تدريجي، مما يشير إلى أنه يزعزع ويثقب أغشية خلايا السرطان بشكل فيزيائي.
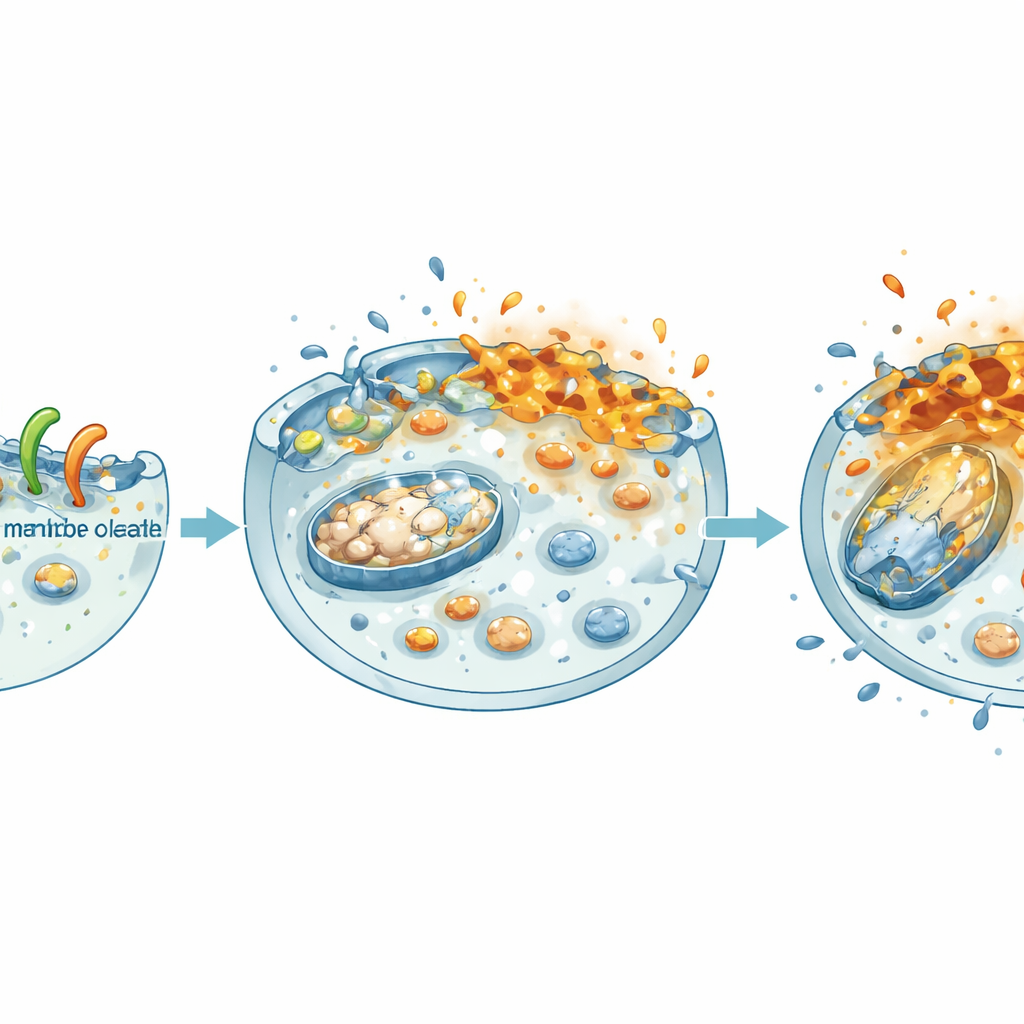
إغلاق محركات الطاقة وبرامج النمو في الخلية
بمجرد أن يخلّ NheA–O بتكامل الغشاء، يمتد الضرر إلى الداخل. وجد الفريق أن الخلايا السرطانية المعالجة فقدت الشحنة الكهربائية عبر الميتوكوندريا — محطات الطاقة الصغيرة داخل الخلايا — وانخفض مخزون الطاقة الكلي لديها (ATP) بشكل حاد، سواء في المزارع المسطحة أو في الكرات الثلاثية الأبعاد. وفي الوقت نفسه، أضعف المركب مسارًا محوريًا للنمو في سرطان القولون والمستقيم: مسار β‑catenin. في بيانات المرضى، ترتبط المستويات العالية من β‑catenin وشركائه ببقاء أسوأ. في المختبر، قلّل NheA–O كمية β‑catenin في النواة، وخفض نشاطه، وقلّل مستويات أهدافه المشجعة للنمو. ونتيجة لذلك، شكلت خلايا الورم مستعمرات أقل، وتراجعت سرعتها في الانتقال، وبنت كرات أصغر وأكثر ضعفًا — ميزات تترجم إلى تقلّص وانتشار أبطأ للورم.
فرض موت يشبه الصدأ في أغشية الورم
اكتشاف رئيسي في هذا العمل هو أن NheA–O يفعّل نوعًا خاصًا من موت الخلايا المعروف بالفيروبتوزيس، الذي يشبه عملية صدأ في دهون الخلية. زاد المركب مستويات ACSL4، وهو بروتين يزوّد الأغشية بمكونات دهنية عرضة للتأكسد، بينما خفّض GPX4، الإنزيم الحيوي «لرجل الإطفاء» الذي يمنع عادة أكسدة هذه الدهون. ومع انخفاض مستويات GPX4، ارتفعت مؤشرات التلف الدهني في الأغشية. جعلت أدوية تعزز الفيروبتوزيس من NheA–O أكثر فتكًا، في حين أن حاجزًا للفيروبتوزيس أنقذ الخلايا جزئيًا، وقلل تلف الغشاء، واستعاد بعض نشاط β‑catenin. أظهرت تجارب إضافية أن NheA–O يعزّز وسم GPX4 للتدمير عبر آلية تفكيك البروتين داخل الخلية، وأن الخلايا التي كانت ناقصة بالفعل في GPX4 كانت أسهل قتلًا بشكل خاص.
ماذا قد يعني هذا للعلاجات المستقبلية
تُظهر النتائج مجتمعة آلية عمل متعددة المسارات: يلتصق NheA–O بأغشية خلايا الورم، يخلّ بتكاملها، يفرغ مصانع الطاقة فيها، ويفرض موتًا شبيهًا بالفيروبتوزيس عن طريق تفكيك نظام الحماية GPX4 وإسكات إشارات النمو المدفوعة بβ‑catenin. وبما أنه يستهدف عدة نقاط ضعف مرة واحدة ويُبقي إلى حد كبير على خلايا القولون الطبيعية في الثقافة، يبرز هذا المركب البروتيني‑الدهني البكتيري كنموذج واعد لعلاجات جديدة لسرطان القولون والمستقيم. وبينما تأتي هذه النتائج من نماذج خلوية محكمة وستتطلب الآن اختبارات في حيوانات ومن ثم في البشر، فإنها توسّع فكرة أن مركبات بروتينية‑دهنية بسيطة — من الحليب أو الميكروبات — يمكن هندستها لتصبح عوامل مضادة للسرطان دقيقة وقوية.
الاستشهاد: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
الكلمات المفتاحية: سرطان القولون والمستقيم, الفيروبتوزيس, بروتين بكتيري, تدمير غشاء الخلية, GPX4 و β‑catenin