Clear Sky Science · nl
Bacterieel eiwit-oleaatcomplex veroorzaakt ferroptose-achtige celdood in dikkedarmkankercellen door celmembranen te verstoren en de β-catenine-GPX4-as te remmen
Bacteriën inzetten als kankerbestrijders
Dikkedarmkanker behoort wereldwijd tot de meest voorkomende vormen van kanker en weet vaak standaardbehandelingen te ontwijken. Deze studie onderzoekt een onverwachte bondgenoot in de strijd tegen deze tumoren: een onschadelijk bacterieel eiwit dat, wanneer het wordt gecombineerd met een veelvoorkomend vetmolecuul, selectief dikkedarmkankercellen kan doden. Door te begrijpen hoe dit eiwit–vetcomplex tumorcellen aanvalt terwijl het gezonde cellen grotendeels spaart, hopen onderzoekers een nieuwe weg naar therapieën te openen die zowel doeltreffender als vriendelijker voor patiënten zijn.
Een nieuw wapen opgebouwd uit eiwit en vet
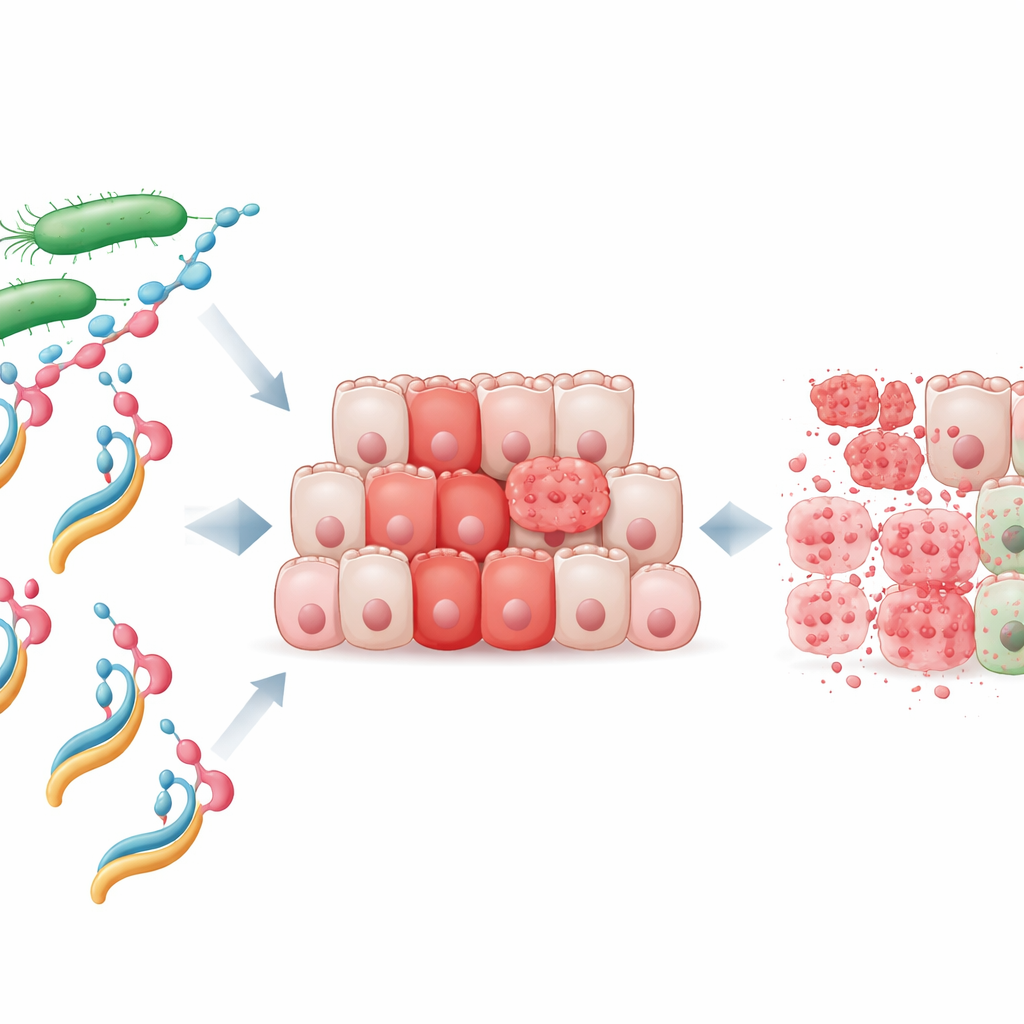
De onderzoekers richtten zich op een bacterieel eiwit genaamd NheA, dat op zichzelf onschadelijk is en zich niet eens aan menselijke cellen kan hechten. Ze mengden gezuiverd NheA met natriumoleaat, een vetzuurderivaat, om te creëren wat ze het NheA–O-complex noemen. Vergelijkbare menselijke eiwit–vetcomplexen, zoals het uit melk afkomstige HAMLET, staan bekend om hun vermogen kankercellen te doden, maar tot nu toe had nog niemand aangetoond dat een bacterieel eiwit in een vergelijkbare tumorkiller kan worden veranderd. Laboratoriumtests toonden aan dat NheA–O snel de overleving van dikkedarmkankercellijnen verminderde, terwijl de afzonderlijke bestanddelen — eiwit of vet alleen — weinig effect hadden. Belangrijk is dat normale darmcellen veel minder gevoelig waren, wat suggereert dat tumorcellen een speciale kwetsbaarheid hebben die dit complex kan benutten.
Directe aanval op het oppervlak van de tumorcel
Met geavanceerde beeldvorming observeerde het team hoe NheA–O zich gedraagt wanneer het in contact komt met kankercellen. Gelabelde versies van het complex gloeiden sterk rond het buitenoppervlak van tumorcellen, wat aantoont dat het zich stevig aan hun membranen hecht. Drie-dimensionale beelden van celclusters (spheroïden) bevestigden dat NheA–O diep in tumorachtigen structuren kan doordringen. Om te isoleren wat er aan het oppervlak gebeurt, maakten de onderzoekers reusachtige membraangebieden (giant membrane bubbles) van kankercellen en stelden die bloot aan NheA–O. Het complex klonterde op deze bellen, verkleinde hun oppervlak en liet normaal uitgesloten kleurstoffen naar binnen lekken. Aanvullende proeven met kunstmatige vetdruppels gemaakt van tumorcellipiden toonden aan dat NheA–O progressief lek veroorzaakte, wat aangeeft dat het fysiek de stabiliteit van en perforaties in kankercelmembraan veroorzaakt.
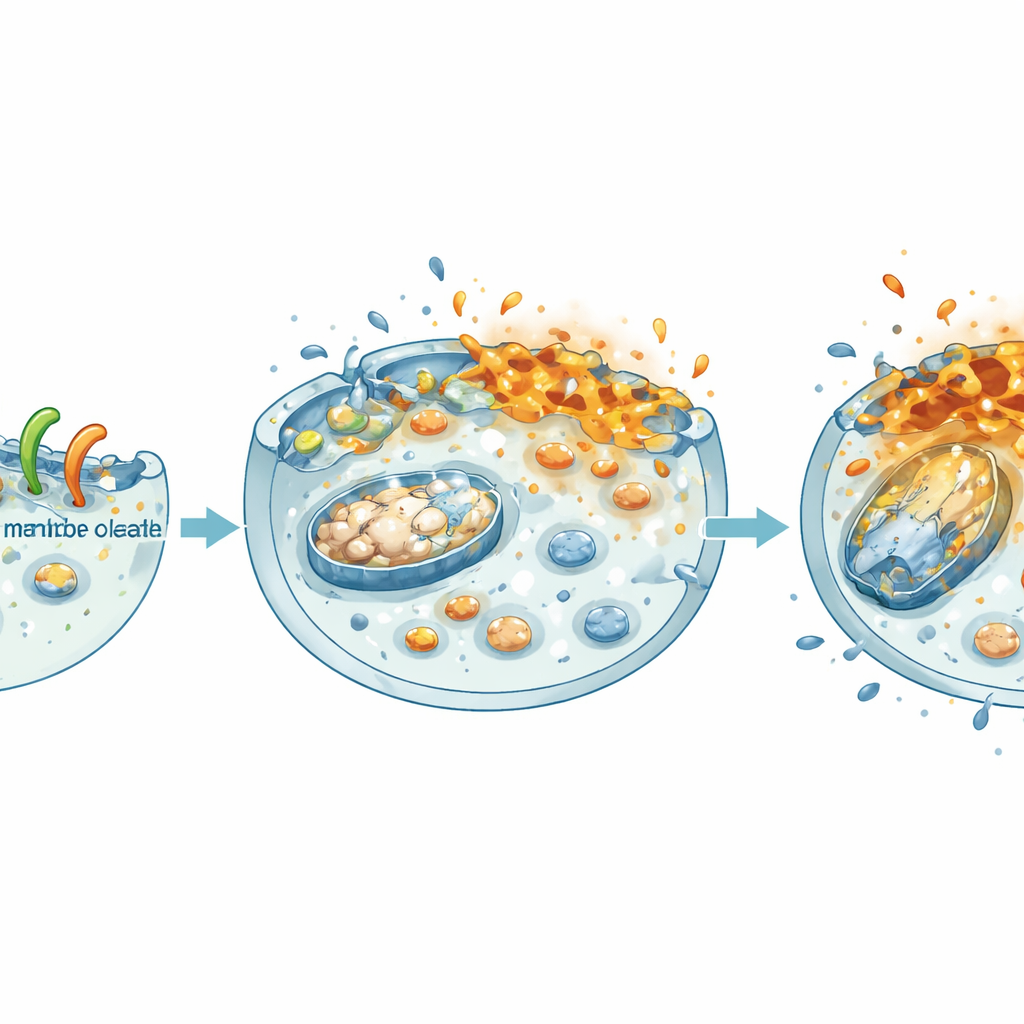
De energie- en groeiprogramma’s van de cel uitschakelen
Zodra NheA–O het membraan verstoort, verspreidt de schade zich naar binnen. Het team vond dat behandelde kankercellen het elektrische potentiaal over hun mitochondriën — de kleine energiecentrales in de cellen — verloren en dat hun totale energievoorraad (ATP) scherp daalde, zowel in platte kweek als in 3D-spheroïden. Tegelijk verzwakte het complex een centraal groeipad in dikkedarmkanker: de β‑catenine-route. In patiëntgegevens correleren hoge niveaus van β‑catenine en zijn partners met een slechte overleving. In het laboratorium verminderde NheA–O de hoeveelheid β‑catenine in de kern, verlaagde zijn activiteit en deed de niveaus van zijn groeibevorderende doelmoleculen dalen. Daardoor vormden tumorcellen minder kolonies, migreerden ze langzamer en bouwden ze kleinere, zwakkere spheroïden — kenmerken die zich vertalen in verminderde tumoruitbreiding en -verspreiding.
Een roestachtige dood in tumormembranen forceren
Een belangrijke ontdekking van dit werk is dat NheA–O een speciale vorm van celdood activeert die bekendstaat als ferroptose, die lijkt op een roestingsproces in de vetten van de cel. Het complex verhoogde de niveaus van ACSL4, een eiwit dat membranen verrijkt met kwetsbare vetcomponenten, terwijl het GPX4 verlaagde, een cruciaal “brandweermolecuul”-enzym dat normaal voorkomt dat deze vetten geoxideerd worden. Toen GPX4-niveaus daalden, schoten chemische markers van lipidedschade in membranen omhoog. Geneesmiddelen die ferroptose versterken maakten NheA–O nog dodelijker, terwijl een remmer van ferroptose de cellen gedeeltelijk redde, membranschade verminderde en enige β‑catenine-activiteit herstelde. Verdere experimenten toonden aan dat NheA–O bevordert dat GPX4 wordt gemerkt voor afbraak door het eiwitafbraakmechanisme van de cel, en dat cellen die al uitgeput zijn van GPX4 bijzonder gemakkelijk te doden waren.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat onthullen de bevindingen een meerledig werkingsmechanisme: NheA–O hecht zich aan tumorcelmembraan, verstoort hun integriteit, leegt hun energiecentrales en dwingt een ferroptose-achtige dood af door het beschermende GPX4-systeem te ontmantelen en β‑catenine-gestuurde groeisignalen te laten zwijgen. Omdat het meerdere kwetsbaarheden tegelijk raakt en normale darmcellen in kweek grotendeels spaart, komt dit bacteriële eiwit–vetcomplex naar voren als een veelbelovend sjabloon voor nieuwe therapieën tegen dikkedarmkanker. Hoewel deze resultaten afkomstig zijn van zorgvuldig gecontroleerde celmodellen en nu in dieren en uiteindelijk in mensen getest moeten worden, verbreden ze het concept dat eenvoudige eiwit–lipidecomplexen — uit melk of microben — ontworpen kunnen worden tot precieze, krachtige antikankermiddelen.
Bronvermelding: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Trefwoorden: dikkedarmkanker, ferroptose, bacterieel eiwit, verstoring van celmembraan, GPX4 en β-catenine