Clear Sky Science · sv
Bakterieprotein–oleatkomplex orsakar ferroptosliknande celldöd i kolorektala cancerceller genom att störa cellmembran och hämma β‑catenin–GPX4‑axeln
Att förvandla bakterier till cancerbekämpare
Kolorektal cancer är en av de vanligaste cancerformerna i världen och lär sig ofta att undvika standardbehandlingar. Denna studie undersöker en oväntad allierad i kampen mot dessa tumörer: ett ofarligt bakterieprotein som, när det förenas med en vanlig fettsyramolekyl, selektivt kan döda kolorektala cancerceller. Genom att förstå hur detta protein–fettsyrakomplex attackerar tumörceller samtidigt som det i stor utsträckning skonar friska celler hoppas forskarna kunna öppna en ny väg till behandlingar som både är effektivare och skonsammare för patienter.
Ett nytt vapen byggt av protein och fett
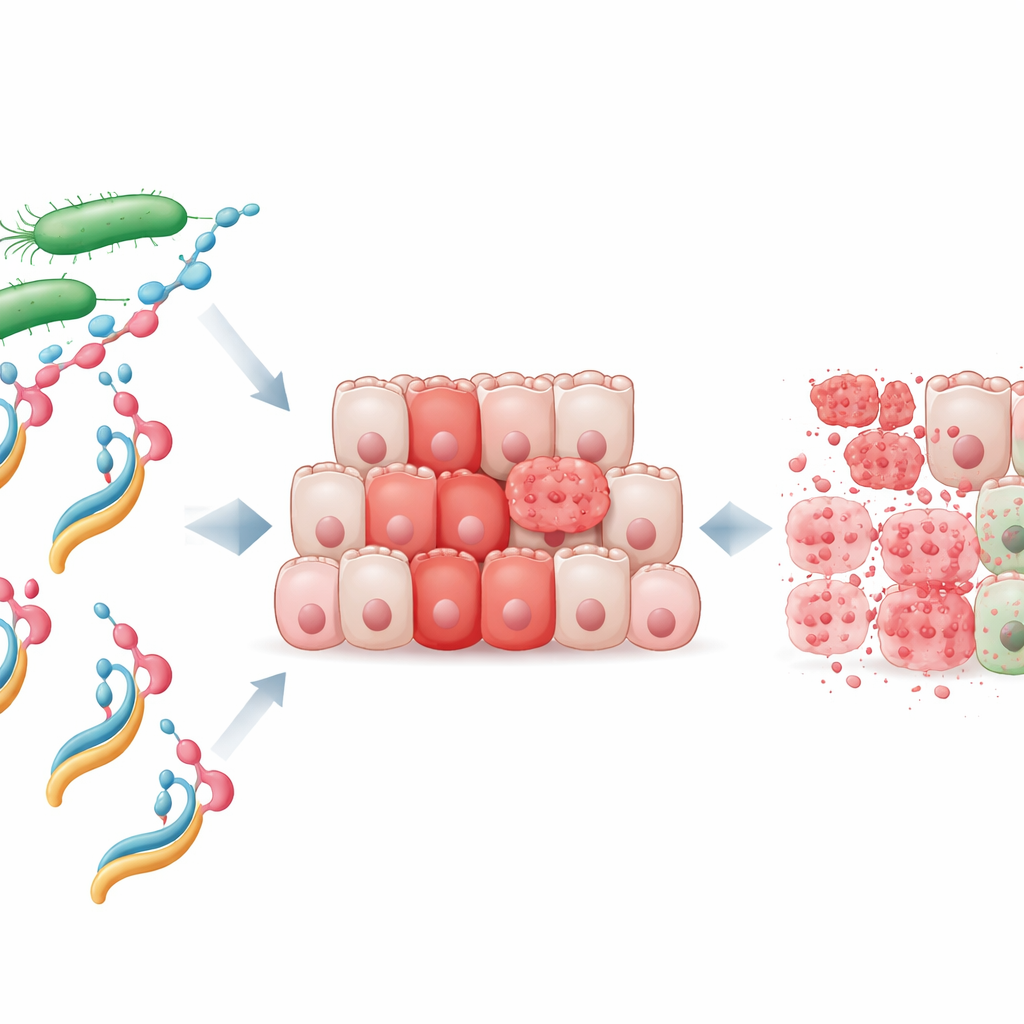
Forskarna fokuserade på ett bakterieprotein kallat NheA, som i sig är ofarligt och inte ens kan fästa vid humana celler. De blandade renat NheA med natriumoleat, en molekyl härledd från en fettsyra, för att skapa det de kallar NheA–O‑komplexet. Liknande mänskliga protein–fettkomplex, såsom det mjölk‑härledda HAMLET, är kända för att döda cancerceller, men hittills hade ingen visat att ett bakterieprotein kunde omvandlas till en jämförbar tumördödare. Laboratorietester visade att NheA–O snabbt minskade överlevnaden hos kolorektala cancercellinjer, medan de individuella ingredienserna – protein eller fett ensamma – hade liten effekt. Viktigt är att normala kolonceller var mycket mindre känsliga, vilket tyder på att tumörcellerna har en särskild svaghet som detta komplex kan utnyttja.
Direkt angrepp mot tumörcellens yta
Med avancerad avbildning följde teamet hur NheA–O beter sig när det möter cancerceller. Märkta versioner av komplexet lyste starkt runt tumörcellernas yttre yta, vilket visar att det binder tätt till deras membran. Tredimensionella bilder av cellklumpar (sfäroider) bekräftade att NheA–O kan tränga djupt in i tumörliknande strukturer. För att isolera vad som händer vid ytan skapade forskarna jätteblåsor av membran från cancerceller och exponerade dem för NheA–O. Komplexet klustrade på dessa blåsor, krympte deras area och tillät normalt utestängda färgämnen att läcka in. Ytterligare tester med artificiella fettkroppar gjorda av tumörcellers lipider visade att NheA–O orsakade progressiv läckage, vilket indikerar att det fysiskt destabiliserar och perforerar cancercellmembran.
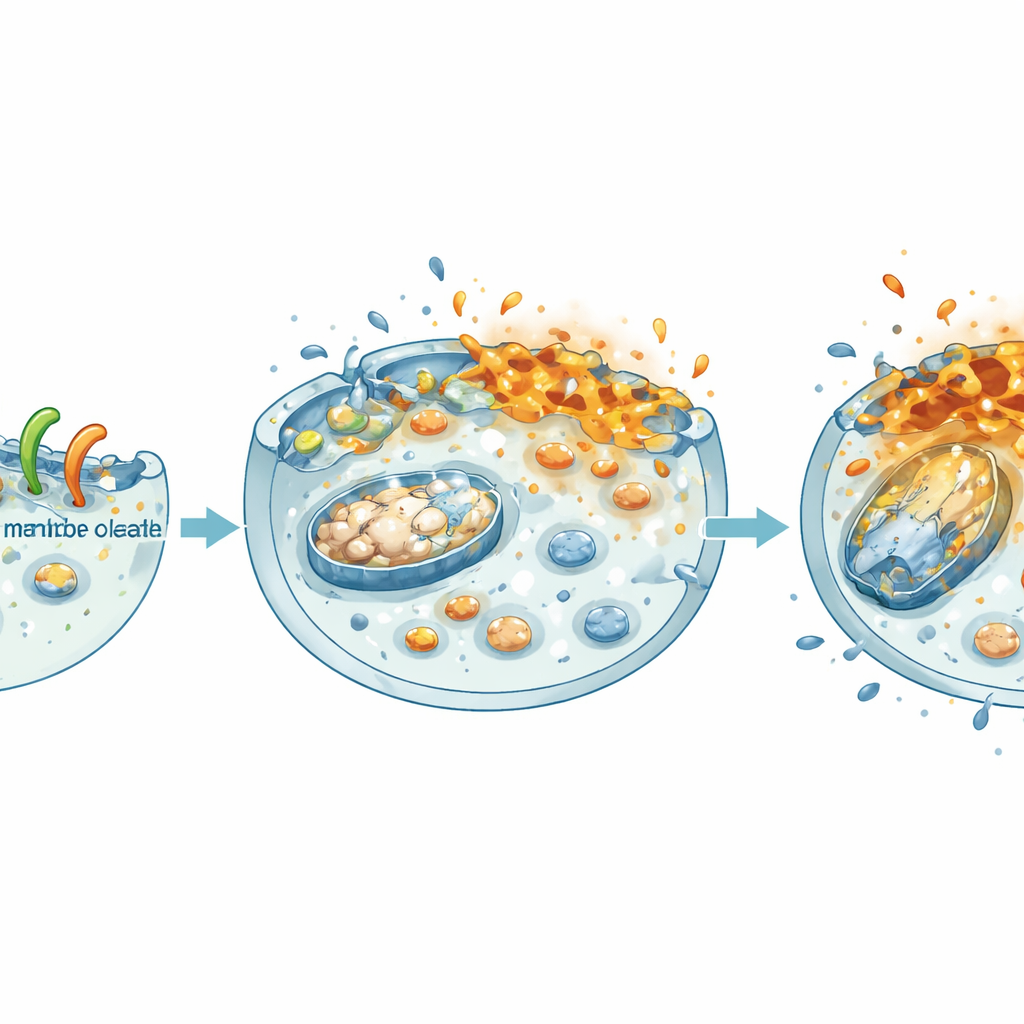
Stänger ner cellens kraft‑ och tillväxtprogram
När NheA–O väl stör membranet sprider sig skadan inåt. Teamet fann att behandlade cancerceller förlorade den elektriska spänningen över sina mitokondrier – cellernas små kraftverk – och deras totala energireserver (ATP) sjönk kraftigt, både i plana kulturer och i 3D‑sfäroider. Samtidigt försvagade komplexet en central tillväxtdrivare i kolorektal cancer: β‑catenin‑vägen. I patientdata är höga nivåer av β‑catenin och dess samarbetspartner kopplade till sämre överlevnad. I laboratoriet minskade NheA–O mängden β‑catenin i cellkärnan, sänkte dess aktivitet och minskade nivåerna av dess tillväxt‑främjande mål. Som ett resultat bildade tumörceller färre kolonier, migrerade långsammare och byggde mindre, svagare sfäroider – egenskaper som översätts till minskad tumörtillväxt och spridning.
Tvingar fram en rostliknande död i tumörmembran
En viktig upptäckt i detta arbete är att NheA–O utlöser en särskild typ av celldöd känd som ferroptos, som liknar en rostningsprocess i cellens fetter. Komplexet ökade nivåerna av ACSL4, ett protein som berikar membran med känsliga fettsyrebyggstenar, samtidigt som det sänkte GPX4, ett avgörande "brandbekämpande" enzym som normalt förhindrar dessa fetter från att oxidera. När GPX4‑nivåerna föll ökade kemiska markörer för lipid‑skada i membranen kraftigt. Läkemedel som förstärker ferroptos gjorde NheA–O ännu mer dödligt, medan en ferroptos‑hämmare delvis räddade cellerna, minskade membranskadorna och återställde viss β‑catenin‑aktivitet. Ytterligare experiment visade att NheA–O främjar märkning av GPX4 för nedbrytning av cellens protein‑rivaresystem, och att celler som redan var uttömda på GPX4 var särskilt lätta att döda.
Vad detta kan betyda för framtida behandlingar
Tillsammans visar fynden en mångsidig verkningsmekanism: NheA–O fäster vid tumörcellmembran, stör deras integritet, tömmer deras energifabriker och tvingar fram en ferroptosliknande död genom att demontera det skyddande GPX4‑systemet och tysta β‑catenin‑drivna tillväxtsignaler. Eftersom det slår mot flera sårbarheter samtidigt och i stor utsträckning skonar normala kolonceller i kultur framstår detta bakterieprotein–fettkomplex som en lovande mall för nya terapier mot kolorektal cancer. Även om dessa resultat kommer från noggrant kontrollerade cellmodeller och nu behöver testas i djur och så småningom människor, breddar de konceptet att enkla protein–lipid‑komplex – från mjölk eller mikrober – kan konstrueras till precisa, potenta anticancer‑medel.
Citering: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Nyckelord: kolorektal cancer, ferroptos, bakterieprotein, störning av cellmembran, GPX4 och β‑catenin