Clear Sky Science · pt
Complexos proteína-oleato bacterianos induzem morte celular semelhante à ferroptose em células de câncer colorretal ao desorganizar membranas celulares e inibir o eixo β-catenina-GPX4
Transformando bactérias em combatentes do câncer
O câncer colorretal é um dos tipos de câncer mais comuns no mundo e frequentemente aprende a escapar dos tratamentos padrão. Este estudo explora um aliado inesperado na luta contra esses tumores: uma proteína bacteriana inofensiva que, quando combinada com uma molécula gordurosa comum, pode matar seletivamente células de câncer colorretal. Ao entender como esse complexo proteína–gordura ataca células tumorais enquanto poupa em grande parte as saudáveis, os pesquisadores esperam abrir uma nova via para terapias mais eficazes e menos agressivas aos pacientes.
Uma nova arma feita de proteína e gordura
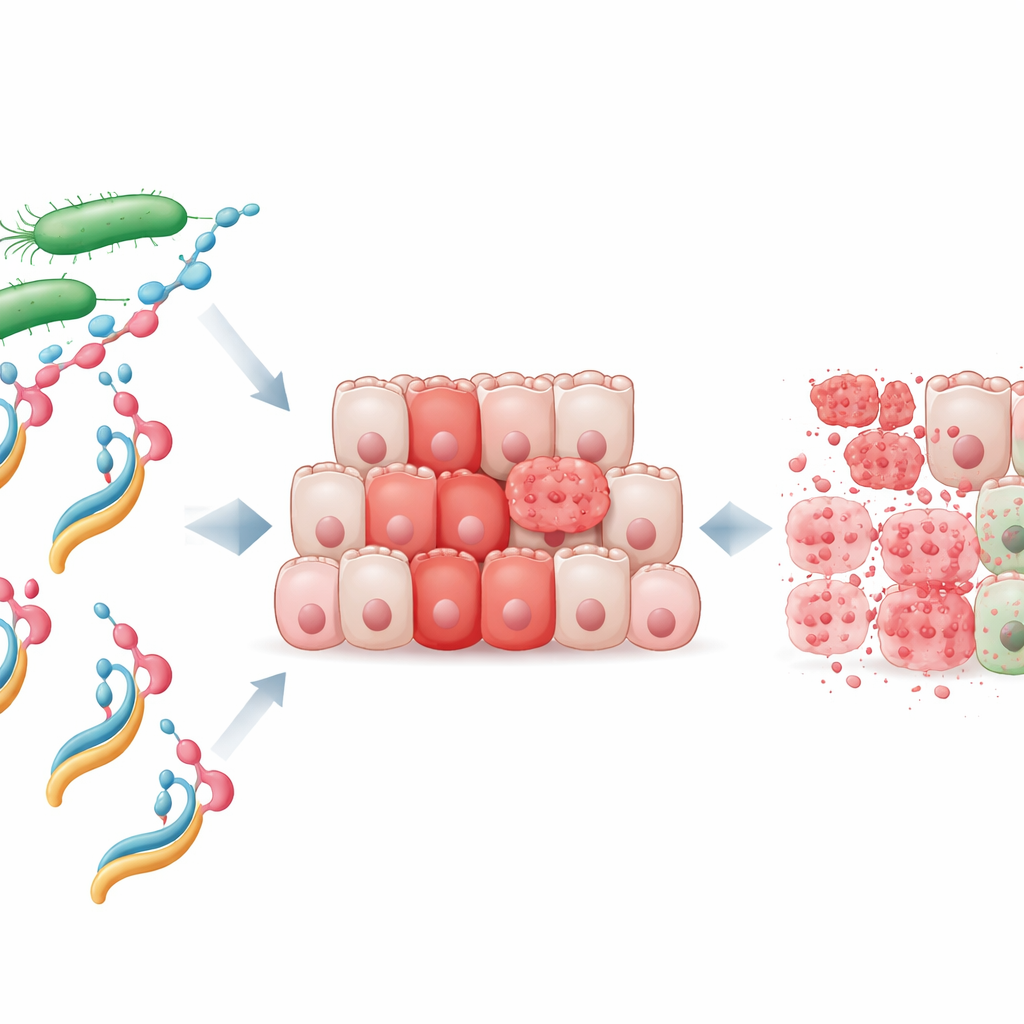
Os pesquisadores concentraram-se em uma proteína bacteriana chamada NheA, que por si só é inofensiva e nem consegue se ligar a células humanas. Eles misturaram NheA purificada com oleato de sódio, uma molécula derivada de ácido graxo, para criar o que chamaram de complexo NheA–O. Complexos proteína–gordura humanos semelhantes, como o HAMLET derivado do leite, são conhecidos por matar células cancerosas, mas até agora ninguém havia demonstrado que uma proteína bacteriana poderia ser transformada em um agente antitumoral comparável. Testes em laboratório revelaram que NheA–O reduziu rapidamente a sobrevivência de linhas celulares de câncer colorretal, enquanto os ingredientes isolados — proteína ou gordura sozinhos — tiveram pouco efeito. Importante, células normais do cólon foram muito menos sensíveis, sugerindo que as células tumorais possuem uma vulnerabilidade específica que este complexo pode explorar.
Ataque direto na superfície da célula tumoral
Usando imagens avançadas, a equipe observou como NheA–O se comporta ao encontrar células cancerosas. Versões marcadas do complexo brilharam intensamente ao redor da superfície externa das células tumorais, mostrando que ele se liga firmemente às suas membranas. Imagens tridimensionais de aglomerados celulares (esferoides) confirmaram que NheA–O pode penetrar profundamente em estruturas semelhantes a tumores. Para isolar o que acontece na superfície, os pesquisadores criaram grandes bolsas de membrana a partir de células cancerosas e as expuseram a NheA–O. O complexo se agrupou nessas bolsas, reduziu sua área e permitiu que moléculas de corante normalmente excluídas vazassem para dentro. Testes adicionais com gotas artificiais de gordura feitas a partir de lipídios de células tumorais mostraram que NheA–O causou vazamento progressivo, indicando que ele desestabiliza fisicamente e perfura as membranas das células cancerosas.
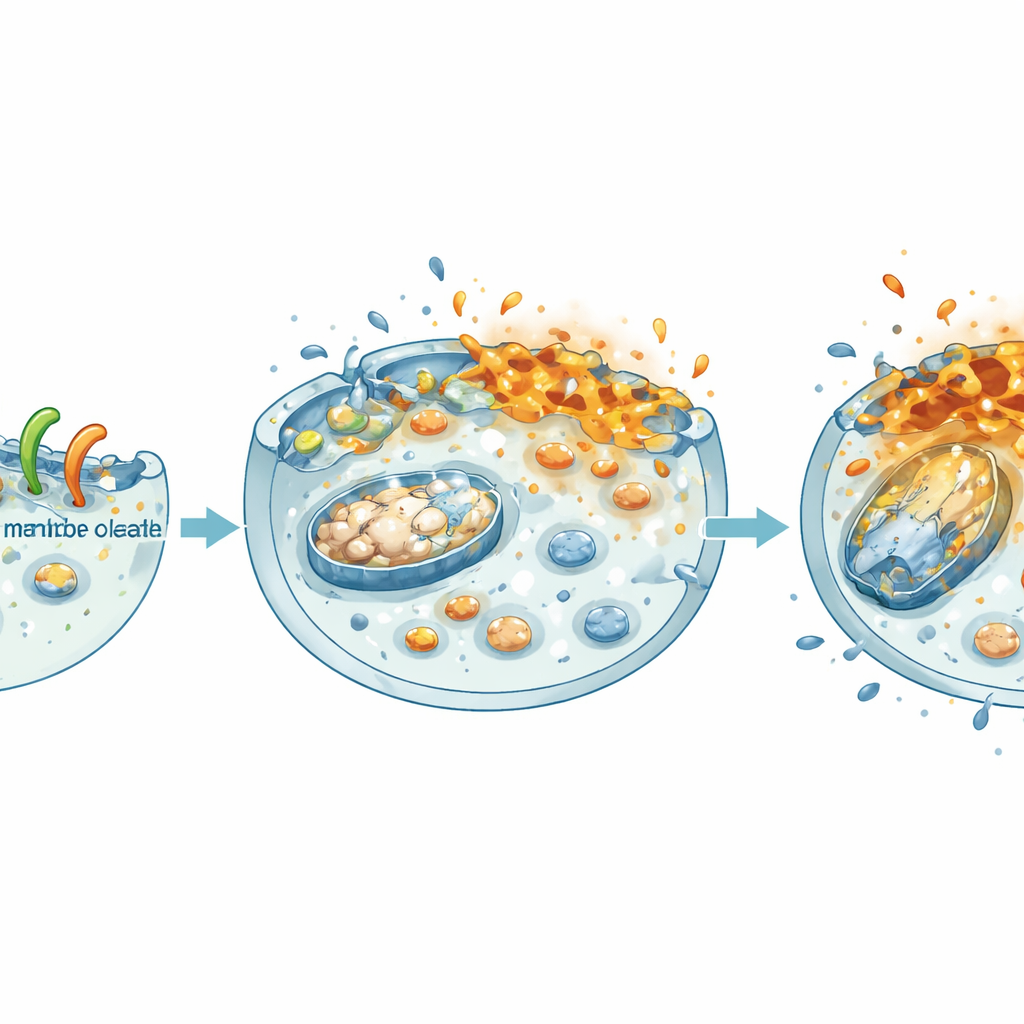
Desligando as usinas e os programas de crescimento da célula
Uma vez que NheA–O perturba a membrana, o dano se espalha para o interior. A equipe constatou que células cancerosas tratadas perderam a diferença de potencial nas suas mitocôndrias — as pequenas usinas de energia dentro das células — e seus estoques gerais de energia (ATP) caíram acentuadamente, tanto em culturas planas quanto em esferoides 3D. Ao mesmo tempo, o complexo enfraqueceu um motor central de crescimento no câncer colorretal: a via da β‑catenina. Em dados de pacientes, níveis elevados de β‑catenina e seus parceiros estão ligados a pior sobrevida. Em laboratório, NheA–O reduziu a quantidade de β‑catenina no núcleo, diminuiu sua atividade e baixou os níveis de seus alvos promotores de crescimento. Como resultado, as células tumorais formaram menos colônias, migraram mais devagar e construíram esferoides menores e mais fracos — características que se traduzem em menor expansão e disseminação tumoral.
Forçando uma morte semelhante a ferrugem nas membranas tumorais
Uma descoberta-chave deste trabalho é que NheA–O desencadeia um tipo especial de morte celular conhecido como ferroptose, que se assemelha a um processo de oxidação (como ferrugem) nas gorduras da célula. O complexo aumentou os níveis de ACSL4, uma proteína que enriquece as membranas com blocos gordurosos vulneráveis, enquanto reduzia o GPX4, uma enzima “bombeira” crucial que normalmente impede que essas gorduras se oxidem. À medida que os níveis de GPX4 caíram, marcadores químicos de dano lipídico nas membranas dispararam. Fármacos que intensificam a ferroptose tornaram NheA–O ainda mais letal, enquanto um bloqueador de ferroptose resgatou parcialmente as células, reduziu o dano nas membranas e restaurou parte da atividade da β‑catenina. Experimentos adicionais mostraram que NheA–O promove a marcação do GPX4 para destruição pela maquinaria de degradação protéica da célula, e que células já com níveis reduzidos de GPX4 eram especialmente fáceis de matar.
O que isso pode significar para tratamentos futuros
Em conjunto, os achados revelam um modo de ação multifacetado: NheA–O se fixa às membranas das células tumorais, desorganiza sua integridade, esgota suas usinas de energia e força uma morte semelhante à ferroptose ao desmontar o sistema protetor GPX4 e silenciar sinais de crescimento dirigidos pela β‑catenina. Por atingir várias vulnerabilidades de uma só vez e poupar em grande parte as células normais do cólon em cultura, esse complexo proteína–gordura bacteriano surge como um template promissor para novas terapias contra o câncer colorretal. Embora esses resultados provenham de modelos celulares cuidadosamente controlados e agora precisem ser testados em animais e, eventualmente, em humanos, eles ampliam o conceito de que complexos simples de proteína–lipídio — do leite ou de micróbios — podem ser projetados em agentes antitumorais precisos e potentes.
Citação: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Palavras-chave: câncer colorretal, ferroptose, proteína bacteriana, ruptura da membrana celular, GPX4 e β-catenina