Clear Sky Science · it
Complessi proteina-oleato batterici inducono una morte cellulare simile alla ferroptosi nelle cellule del cancro colorettale interrompendo le membrane cellulari e inibendo l’asse β-catenina-GPX4
Trasformare i batteri in alleati contro il cancro
Il cancro colorettale è uno dei tumori più diffusi al mondo e spesso impara a sfuggire ai trattamenti standard. Questo studio esplora un alleato inaspettato nella lotta contro questi tumori: una proteina batterica innocua che, quando associata a una comune molecola grassa, può uccidere selettivamente le cellule del cancro colorettale. Comprendendo come questo complesso proteina-grasso attacca le cellule tumorali risparmiando in gran parte quelle sane, i ricercatori sperano di aprire una nuova strada verso terapie più efficaci e meno dannose per i pazienti.
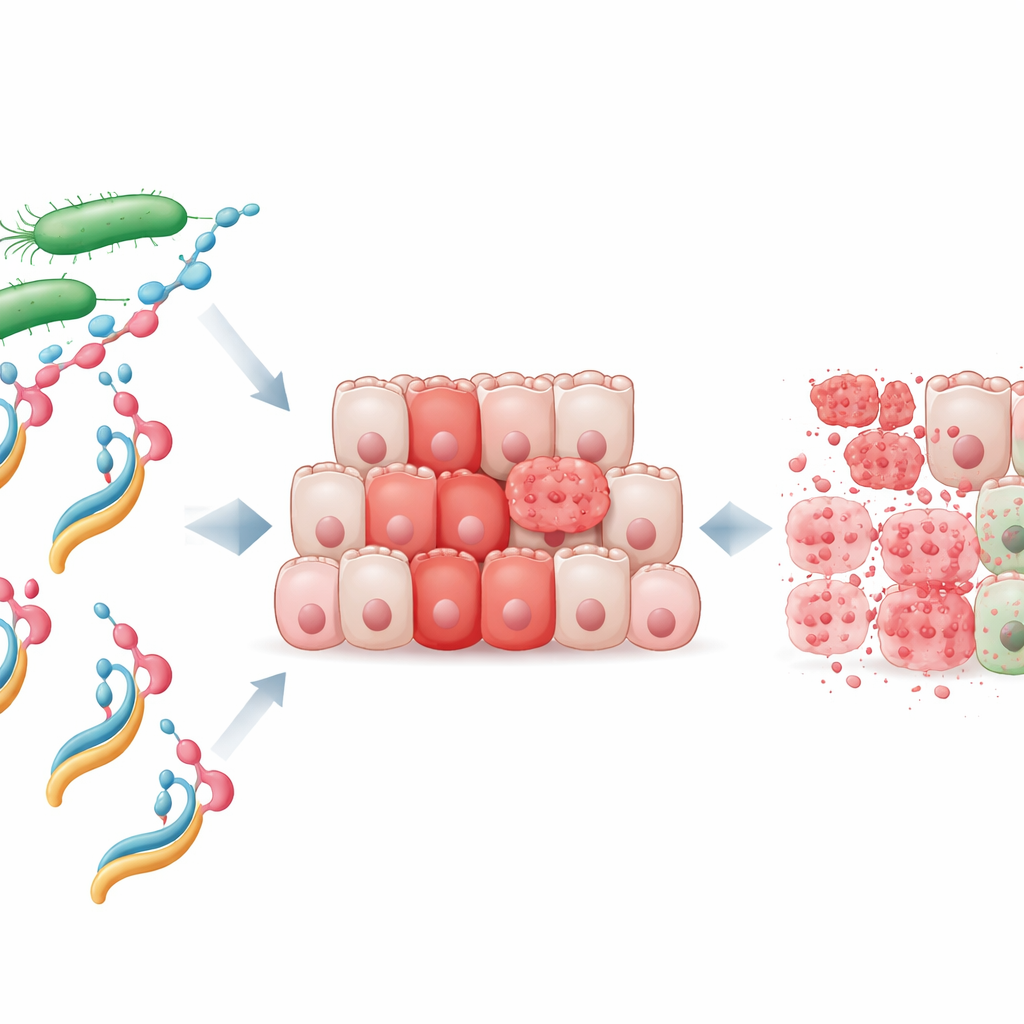
Una nuova arma costruita da proteina e grasso
I ricercatori si sono concentrati su una proteina batterica chiamata NheA, che da sola è innocua e non riesce nemmeno ad agganciarsi alle cellule umane. Hanno miscelato NheA purificata con oleato di sodio, una molecola derivata da un acido grasso, per creare quello che chiamano complesso NheA–O. Complessi proteina-lipide umani simili, come l’HAMLET derivato dal latte, sono noti per uccidere le cellule tumorali, ma fino ad ora non era stato dimostrato che una proteina batterica potesse essere trasformata in un analogo agente anticancro. I test di laboratorio hanno mostrato che NheA–O riduce rapidamente la sopravvivenza delle linee cellulari del cancro colorettale, mentre i singoli ingredienti — proteina o grasso da soli — avevano scarso effetto. Importante, le cellule del colon normali risultavano molto meno sensibili, suggerendo che le cellule tumorali possiedono una vulnerabilità particolare che questo complesso può sfruttare.
Attacco diretto sulla superficie delle cellule tumorali
Utilizzando immagini avanzate, il gruppo ha osservato come si comporta NheA–O quando incontra le cellule tumorali. Versioni marcate del complesso hanno emesso forte segnale attorno alla superficie esterna delle cellule tumorali, mostrando che si lega saldamente alle loro membrane. Immagini tridimensionali di aggregati cellulari (sferoidi) hanno confermato che NheA–O può penetrare in profondità in strutture simili al tumore. Per isolare ciò che accade alla superficie, i ricercatori hanno creato bolle di membrana giganti a partire da cellule tumorali ed esposte a NheA–O. Il complesso si è raggruppato su queste bolle, ne ha ridotto l’area e ha permesso a molecole di colorante normalmente escluse di penetrare all’interno. Test aggiuntivi con gocce grasse artificiali composte dai lipidi delle cellule tumorali hanno mostrato che NheA–O provoca perdite progressive, indicando che destabilizza fisicamente e perfora le membrane delle cellule tumorali.
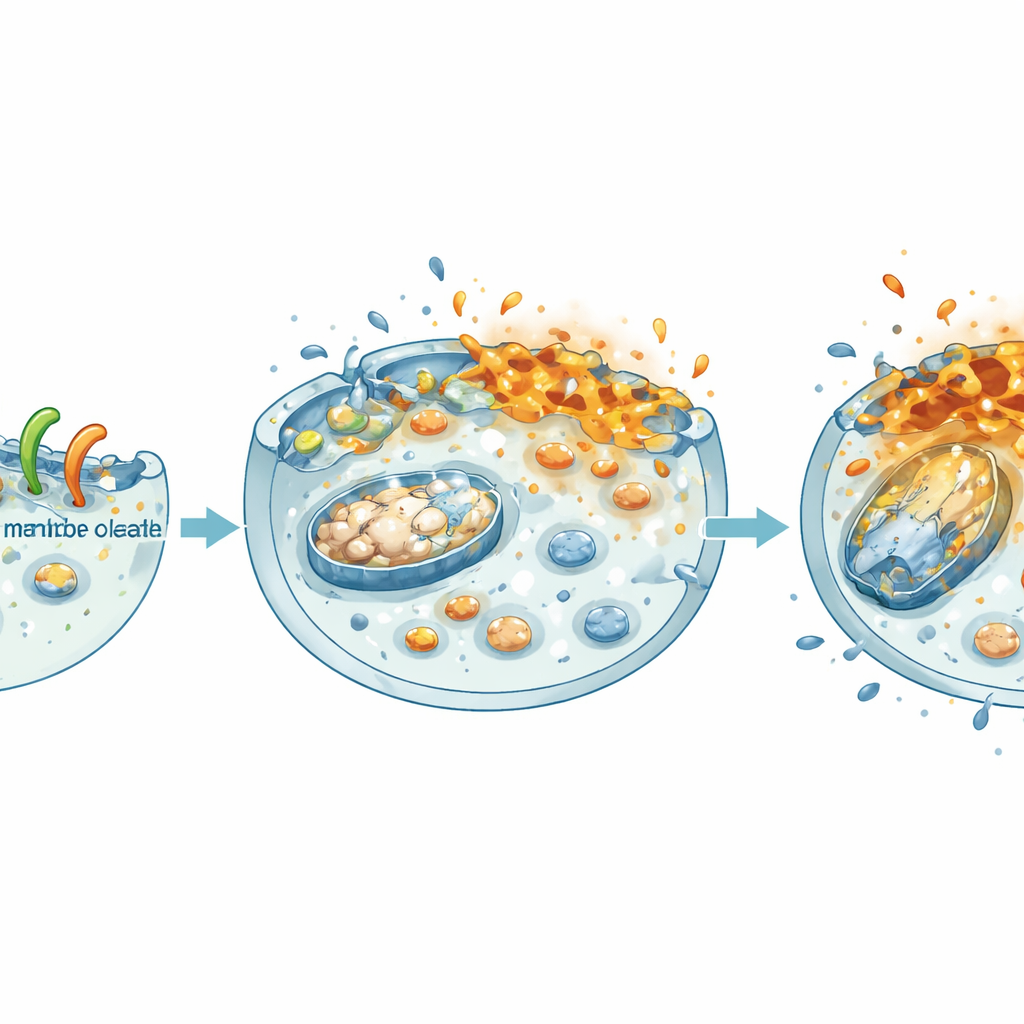
Spegnere i programmi di energia e crescita cellulare
Una volta che NheA–O compromette la membrana, il danno si propaga verso l’interno. Il gruppo ha riscontrato che le cellule tumorali trattate perdevano il potenziale elettrico attraverso i mitocondri — le piccole centrali energetiche della cellula — e le loro riserve complessive di energia (ATP) diminuivano bruscamente, sia nelle colture monostrato sia negli sferoidi 3D. Allo stesso tempo, il complesso indeboliva un motore centrale della crescita nel cancro colorettale: la via della β‑catenina. Nei dati dei pazienti, alti livelli di β‑catenina e dei suoi partner sono associati a scarsa sopravvivenza. In laboratorio, NheA–O ha ridotto la quantità di β‑catenina nel nucleo, ne ha abbassato l’attività e ha diminuito i livelli dei suoi target che promuovono la crescita. Di conseguenza, le cellule tumorali formavano meno colonie, migravano più lentamente e costruivano sferoidi più piccoli e fragili — caratteristiche che si traducono in una ridotta espansione e diffusione tumorale.
Indurre una morte simile alla ruggine nelle membrane tumorali
Una scoperta chiave di questo lavoro è che NheA–O innesca una forma speciale di morte cellulare nota come ferroptosi, che ricorda un processo di ossidazione (simile alla ruggine) nei grassi della cellula. Il complesso ha aumentato i livelli di ACSL4, una proteina che arricchisce le membrane con acidi grassi particolarmente vulnerabili, mentre ha ridotto GPX4, un enzima cruciale che normalmente impedisce a questi lipidi di ossidarsi. Con la diminuzione di GPX4, i marker chimici del danno lipidico nelle membrane sono aumentati notevolmente. Farmaci che potenziano la ferroptosi hanno reso NheA–O ancora più letale, mentre un inibitore della ferroptosi ha parzialmente salvato le cellule, riducendo il danno alle membrane e ripristinando in parte l’attività della β‑catenina. Ulteriori esperimenti hanno mostrato che NheA–O promuove il marchiamento di GPX4 per la distruzione da parte del sistema di degradazione proteica della cellula, e che le cellule già deplete di GPX4 erano particolarmente facili da uccidere.
Cosa potrebbe significare per i trattamenti futuri
Nel loro complesso, i risultati rivelano un meccanismo d’azione multiplo: NheA–O si aggancia alle membrane delle cellule tumorali, ne compromette l’integrità, svuota le loro centrali energetiche e induce una morte simile alla ferroptosi smantellando il sistema protettivo GPX4 e silenziando i segnali di crescita guidati da β‑catenina. Poiché colpisce più vulnerabilità contemporaneamente e risparmia in larga misura le cellule del colon normale in coltura, questo complesso proteina-grasso batterico emerge come un promettente modello per nuove terapie contro il cancro colorettale. Sebbene questi risultati provengano da modelli cellulari strettamente controllati e debbano ora essere testati in animali e, in ultima analisi, nell’uomo, essi ampliano il concetto secondo cui semplici complessi proteina-lipide — derivati dal latte o dai microrganismi — possono essere ingegnerizzati per diventare agenti anticancro precisi e potenti.
Citazione: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Parole chiave: cancro colorettale, ferroptosi, proteina batterica, disgregazione della membrana cellulare, GPX4 e β-catenina