Clear Sky Science · de
Bakterielle Protein‑Oleat‑Komplexe induzieren ferroptoseähnlichen Zelltod in kolorektalen Krebszellen durch Störung der Zellmembranen und Hemmung der β‑Catenin‑GPX4‑Achse
Bakterien zu Krebsbekämpfern machen
Das kolorektale Karzinom gehört zu den weltweit häufigsten Krebsarten und entwickelt oft Wege, Standardtherapien zu entgehen. Diese Studie untersucht einen unerwarteten Verbündeten im Kampf gegen diese Tumore: ein harmloses bakterielles Protein, das in Kombination mit einem verbreiteten Fettmolekül selektiv kolorektale Krebszellen töten kann. Indem Forscher verstehen, wie dieser Protein‑Fett‑Komplex Tumorzellen angreift, während er gesunde Zellen weitgehend verschont, erhofft man sich einen neuen Weg zu Therapien, die sowohl wirksamer als auch schonender für die Patienten sind.
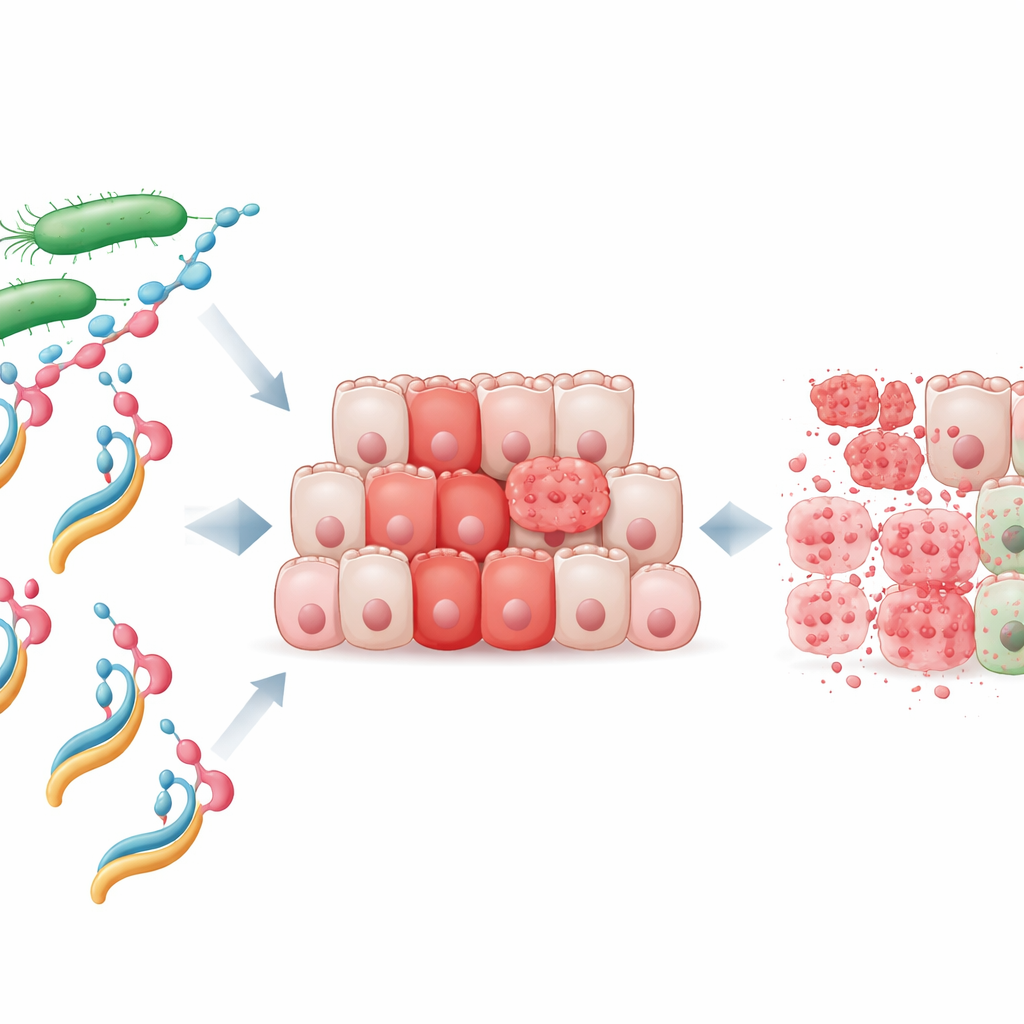
Eine neue Waffe aus Protein und Fett
Die Forschenden konzentrierten sich auf ein bakterielles Protein namens NheA, das für sich genommen harmlos ist und sich nicht einmal an menschliche Zellen anheften kann. Sie kombinierten gereinigtes NheA mit Natriumoleat, einem aus Fettsäuren abgeleiteten Molekül, und erzeugten so den sogenannten NheA–O‑Komplex. Ähnliche menschliche Protein‑Fett‑Komplexe, etwa das milchabgeleitete HAMLET, sind dafür bekannt, Krebszellen zu töten, doch bislang hatte niemand gezeigt, dass ein bakterielles Protein in einen vergleichbaren Tumorkiller verwandelt werden kann. Laboruntersuchungen ergaben, dass NheA–O die Überlebensrate von kolorektalen Krebszelllinien rasch verringerte, während die einzelnen Bestandteile — Protein oder Fett allein — nur geringe Effekte zeigten. Wichtig ist, dass normale Darmzellen deutlich weniger empfindlich waren, was darauf hindeutet, dass Tumorzellen eine spezielle Verwundbarkeit besitzen, die dieser Komplex ausnutzen kann.
Direkter Angriff auf die Tumorzelloberfläche
Mithilfe fortschrittlicher Bildgebung beobachtete das Team, wie sich NheA–O verhält, wenn es auf Krebszellen trifft. Markierte Versionen des Komplexes leuchteten stark an der Außenseite der Tumorzellen und zeigten so, dass er fest an deren Membranen bindet. Drei‑dimensionale Aufnahmen von Zellverbänden (Spheroiden) bestätigten, dass NheA–O tief in tumorähnliche Strukturen eindringen kann. Um zu isolieren, was an der Oberfläche geschieht, erzeugten die Forschenden große Membranblasen aus Krebszellen und setzten diese NheA–O aus. Der Komplex verklumpte auf diesen Blasen, verkleinerte deren Fläche und ließ normalerweise ausgeschlossene Farbstoffmoleküle eindringen. Zusätzliche Tests mit künstlichen Fetttröpfchen aus Tumorzelllipiden zeigten, dass NheA–O fortschreitendes Austreten verursachte, was darauf hindeutet, dass es die Membranen von Krebszellen physikalisch destabilisiert und perforiert.
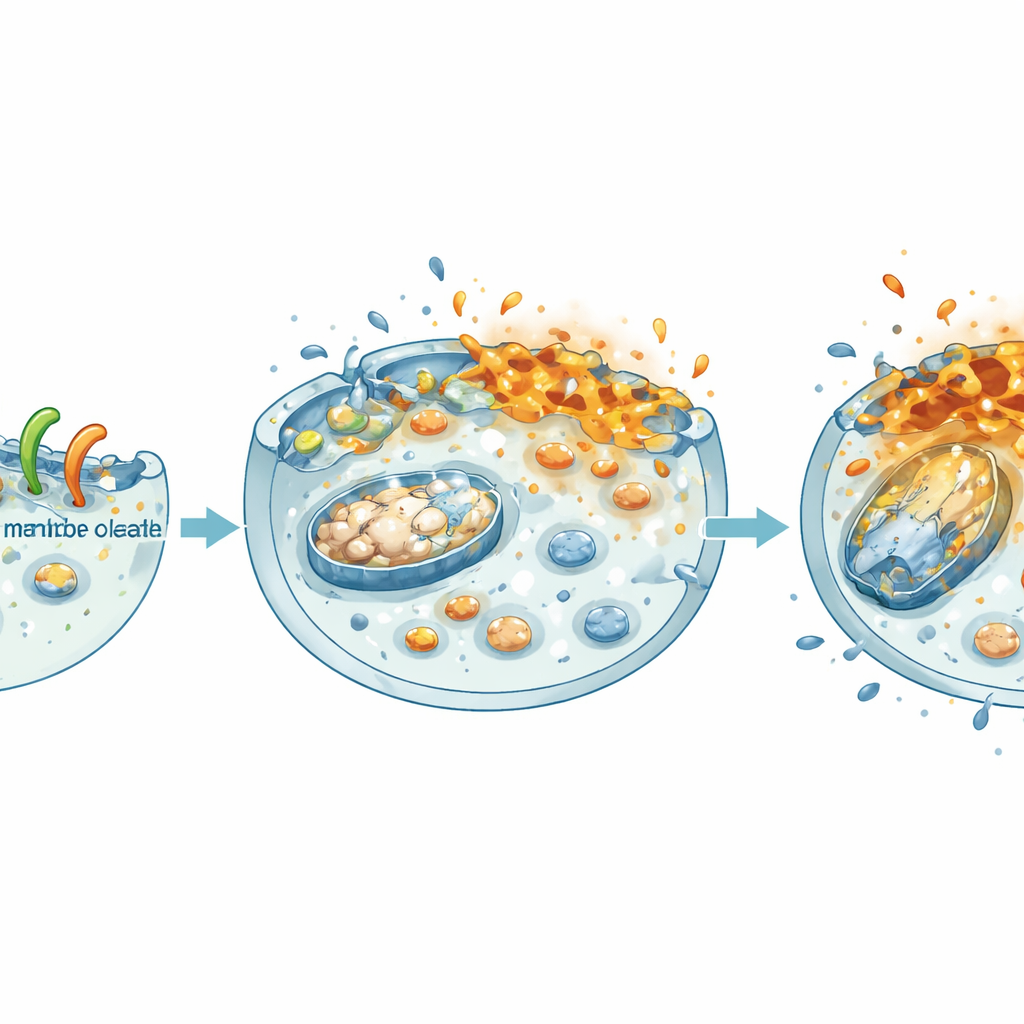
Abschalten der Energie‑ und Wachstumsprogramme der Zelle
Nachdem NheA–O die Membran gestört hatte, breitete sich der Schaden nach innen aus. Das Team fand heraus, dass behandelte Krebszellen die elektrische Spannung ihrer Mitochondrien — den kleinen Kraftwerken der Zelle — verloren und ihre gesamten Energiespeicher (ATP) stark sanken, sowohl in zweidimensionalen Kulturen als auch in 3D‑Spheroiden. Gleichzeitig schwächte der Komplex einen zentralen Wachstumsförderer im kolorektalen Krebs: den β‑Catenin‑Signalweg. In Patientendaten sind hohe Werte von β‑Catenin und seinen Partnern mit schlechter Überlebensprognose verbunden. Im Labor verringerte NheA–O die Menge an β‑Catenin im Zellkern, reduzierte dessen Aktivität und senkte die Levels seiner wachstumsfördernden Zielgene. Infolgedessen bildeten Tumorzellen weniger Kolonien, migrierten langsamer und bildeten kleinere, schwächere Spheroide — Eigenschaften, die sich in reduziertem Tumorwachstum und geringerer Ausbreitung niederschlagen.
Erzwungener rostähnlicher Tod in Tumormembranen
Eine zentrale Entdeckung dieser Arbeit ist, dass NheA–O eine spezielle Form des Zelltods auslöst, bekannt als Ferroptose, die einem Rostprozess in den Fetten der Zelle ähnelt. Der Komplex erhöhte die Spiegel von ACSL4, einem Protein, das Membranen mit anfälligen Fettsubstraten anreichert, während er GPX4 verringerte, ein zentrales „Feuerwehr“‑Enzym, das normalerweise verhindert, dass diese Fette oxidieren. Mit abnehmendem GPX4 stiegen chemische Marker für Lipid‑Schäden in den Membranen stark an. Medikamente, die Ferroptose verstärken, machten NheA–O noch lethaler, während ein Ferroptose‑Blocker die Zellen teilweise rettete, Membranschäden verringerte und etwas β‑Catenin‑Aktivität wiederherstellte. Weitere Experimente zeigten, dass NheA–O die Markierung von GPX4 für den Abbau durch die zelluläre Proteinhaschere fördert und dass Zellen, denen GPX4 bereits fehlte, besonders leicht zu töten waren.
Was das für zukünftige Behandlungen bedeuten könnte
Zusammengefasst offenbaren die Ergebnisse einen mehrgleisigen Wirkmechanismus: NheA–O heftet sich an Tumorzellmembranen, stört deren Integrität, erschöpft ihre Energiemechanismen und erzwingt einen ferroptoseähnlichen Tod, indem es das schützende GPX4‑System demontiert und β‑Catenin‑getriebene Wachstums‑Signale zum Schweigen bringt. Da es mehrere Verwundbarkeiten gleichzeitig trifft und in Zellkultur normale Darmzellen weitgehend verschont, bietet sich dieser bakterielle Protein‑Fett‑Komplex als vielversprechende Vorlage für neue Therapien gegen kolorektalen Krebs an. Auch wenn diese Befunde aus kontrollierten Zellmodellen stammen und nun in Tiermodellen und schließlich am Menschen geprüft werden müssen, erweitern sie das Konzept, dass einfache Protein‑Lipid‑Komplexe — aus Milch oder Mikroben — zu präzisen, potenten Antikrebswirkstoffen entwickelt werden können.
Zitation: Ullah, N., Yabrag, A., Ali, A. et al. Bacterial protein-oleate complexes induce ferroptosis-like cell death in colorectal cancer cells by disrupting cell membranes and inhibiting the β-catenin-GPX4 axis. Cell Death Discov. 12, 182 (2026). https://doi.org/10.1038/s41420-026-03097-9
Schlüsselwörter: kolorektales Karzinom, Ferroptose, bakterielles Protein, Störung der Zellmembran, GPX4 und β‑Catenin