Clear Sky Science · zh
NRIP1 共同激活转位入核的 FOXO3 以上调 TFAM 表达并促进非小细胞肺癌的放射抗性
为何让肺癌治疗更有效很重要
放疗是治疗非小细胞肺癌(最常见的肺癌类型)的主要手段。然而,许多肿瘤会逐步学会抵御放射,从而导致疾病复发或转移。本研究提出了一个简单但至关重要的问题:癌细胞内部发生了什么,使其中一些细胞能够摆脱辐射的致死作用?能否利用这些内部机制对抗肿瘤,提高治疗效果?
癌细胞如何躲避辐射造成的损伤
辐射主要通过产生大量有害分子(即活性氧种)和破坏 DNA 来杀死癌细胞。这些攻击与细胞的能量工厂——线粒体密切相关。研究者注意到,放射抗性的肺癌细胞不仅在放疗后存活率更高,而且具有更多的线粒体 DNA 以及更高水平的关键线粒体蛋白 TFAM,该蛋白有助于复制并保护线粒体 DNA。与原始、未获得抗性的细胞相比,这些耐受细胞显示出更少的氧化损伤、更低的程序性细胞死亡以及明显更高的 TFAM 水平,指向 TFAM 作为帮助癌细胞经受治疗的核心保护因子。
细胞核内的开关如何强化这道保护屏障
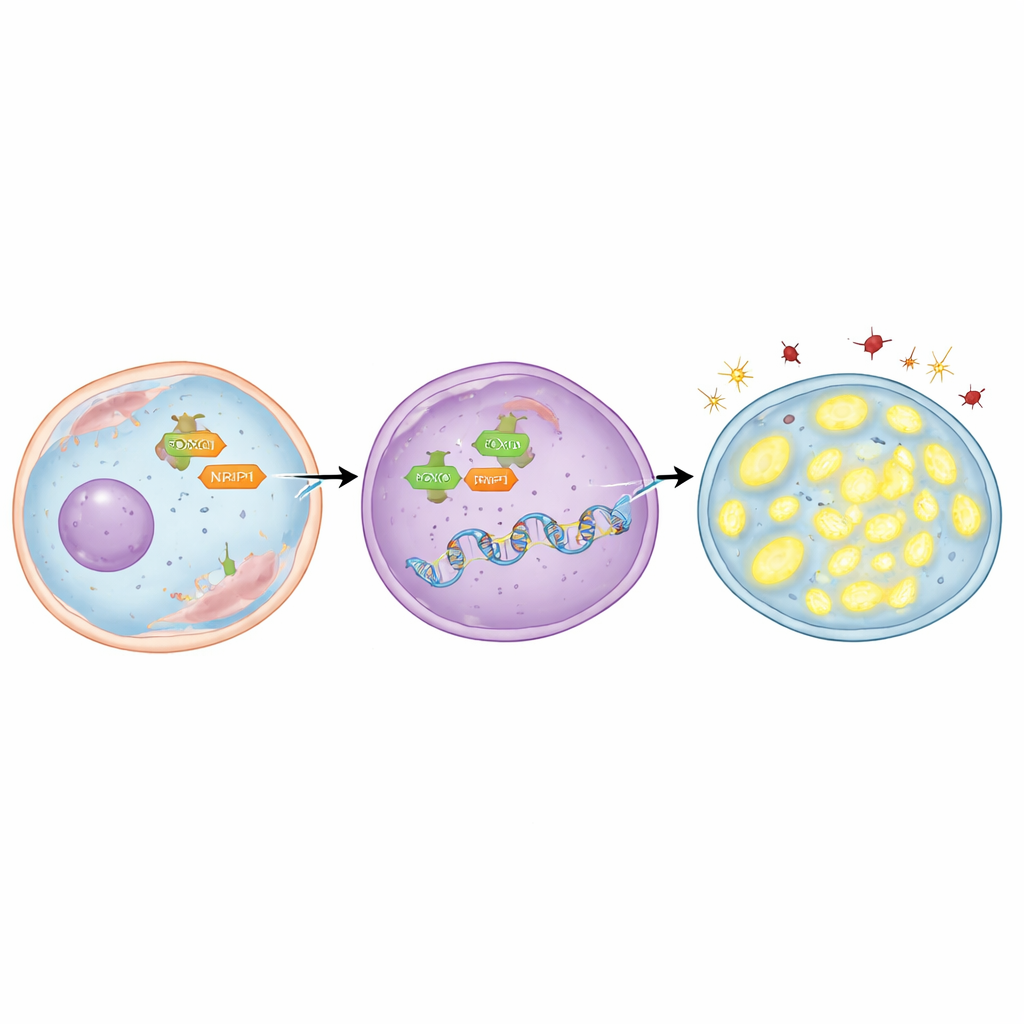
为找出谁将 TFAM “开启”,团队聚焦于一种名为 FOXO3 的调控蛋白,它可以从细胞质转移到细胞核——基因调控发生的场所。他们发现 TFAM 基因含有多个短的 DNA 序列是 FOXO3 可结合的位点。通过计算建模和实验上绘制蛋白–DNA 接触的技术,他们证明了 FOXO3 直接结合这些区域。在放射抗性肺癌细胞中,FOXO3 的表达更高且集中存在于细胞核。当实验性降低 FOXO3 时,TFAM 水平下降,有害分子堆积,线粒体丢失 DNA,且放疗后死亡的癌细胞增多。相反,使用一种促使 FOXO3 进入细胞核的化合物可提升 TFAM、保护线粒体、降低损伤并使细胞更难被杀死——除非同时阻断 TFAM 本身。
增强保护反应的辅助蛋白
故事并未止步于 FOXO3。研究者还考察了 NRIP1,这是一种在癌症中与多种基因调控因子配对的辅助蛋白。他们发现 NRIP1 与 FOXO3 存在物理相互作用,而且在放射抗性细胞中这种伙伴关系更强。在一条天然缺乏功能性 NRIP1 的肺癌细胞系中,TFAM 水平相对较低;恢复正常 NRIP1 可在不改变 FOXO3 总量的情况下提高 TFAM。在表达 NRIP1 的放射抗性细胞中,下调 NRIP1 会降低 TFAM、增加氧化应激、减少线粒体 DNA,并在放疗后促使更多细胞走向死亡。重要的是,NRIP1 并不改变进入细胞核的 FOXO3 数量;相反,它作为一种共激活因子,使已经到位的 FOXO3 更高效地激活 TFAM。
来自活体肿瘤的证据
为检验这些分子事件在整体生物体内是否重要,研究团队将放射抗性肺癌细胞植入小鼠体内形成肿瘤。当在植入前稳定降低这些细胞中的 FOXO3 时,形成的肿瘤生长更慢。在 FOXO3 下调的基础上施加放疗则使肿瘤进一步缩小,同时不损害动物的总体健康。FOXO3 缺失的这些肿瘤表现出更多的氧化应激、较少的线粒体 DNA、更强的细胞死亡信号以及显著更低的 TFAM 水平。综合来看,这些发现支持这样一个观点:FOXO3 驱动的 TFAM 表达在 NRIP1 的增强下,帮助肿瘤在活体中维持强健的线粒体并抵御放射。
这对未来肺癌治疗意味着什么
对非专业读者来说,结论是:一些肺癌通过强化其细胞能量工厂变得更能耐受放射。三者协同——FOXO3 转入细胞核、NRIP1 提供辅助以及 TFAM 加强线粒体——构成了一条保护回路,使肿瘤细胞能修复损伤并持续存活。通过阻断 FOXO3 活性、干扰其与 NRIP1 的合作或直接降低 TFAM,未来的治疗策略或可剥夺肿瘤这层隐蔽的盔甲。这类策略可能使标准放疗更为有效,或在降低剂量的同时实现更好的肿瘤控制并减少治疗失败。
引用: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
关键词: 非小细胞肺癌, 放射抗性, 线粒体, FOXO3, TFAM