Clear Sky Science · it
NRIP1 co-attiva FOXO3 traslocato nel nucleo per aumentare l'espressione di TFAM e promuovere la radioresistenza nel carcinoma polmonare non a piccole cellule
Perché è importante rendere più efficaci le terapie per il cancro polmonare
La radioterapia è una pietra miliare nel trattamento del carcinoma polmonare non a piccole cellule, il tipo più comune di cancro al polmone. Tuttavia molti tumori imparano gradualmente a sopravvivere alla radiazione, permettendo alla malattia di ripresentarsi o di diffondersi. Questo studio pone una domanda semplice ma cruciale: cosa accade all’interno delle cellule tumorali che permette ad alcune di resistere alle radiazioni, e si possono sfruttare quei meccanismi interni contro il tumore per rendere il trattamento più efficace?
Come le cellule tumorali eludono i danni da radiazione
La radiazione uccide le cellule tumorali principalmente generando ondate di molecole dannose chiamate specie reattive dell'ossigeno e provocando rotture nel DNA. Questi attacchi sono strettamente legati alle centrali energetiche della cellula, i mitocondri. I ricercatori hanno osservato che le cellule di cancro polmonare radioresistenti non solo sopravvivono meglio dopo la radiazione, ma possiedono anche più DNA mitocondriale e livelli più elevati di una proteina mitocondriale chiave chiamata TFAM, che aiuta a copiare e proteggere il DNA mitocondriale. Confrontando queste cellule resistenti con le loro controparti non resistenti, si è riscontrato meno danno ossidativo, meno morte cellulare programmata e chiaramente livelli più alti di TFAM, indicando TFAM come uno scudo centrale che aiuta le cellule tumorali a sopportare il trattamento.
Interruttori nel nucleo cellulare che rafforzano questo scudo
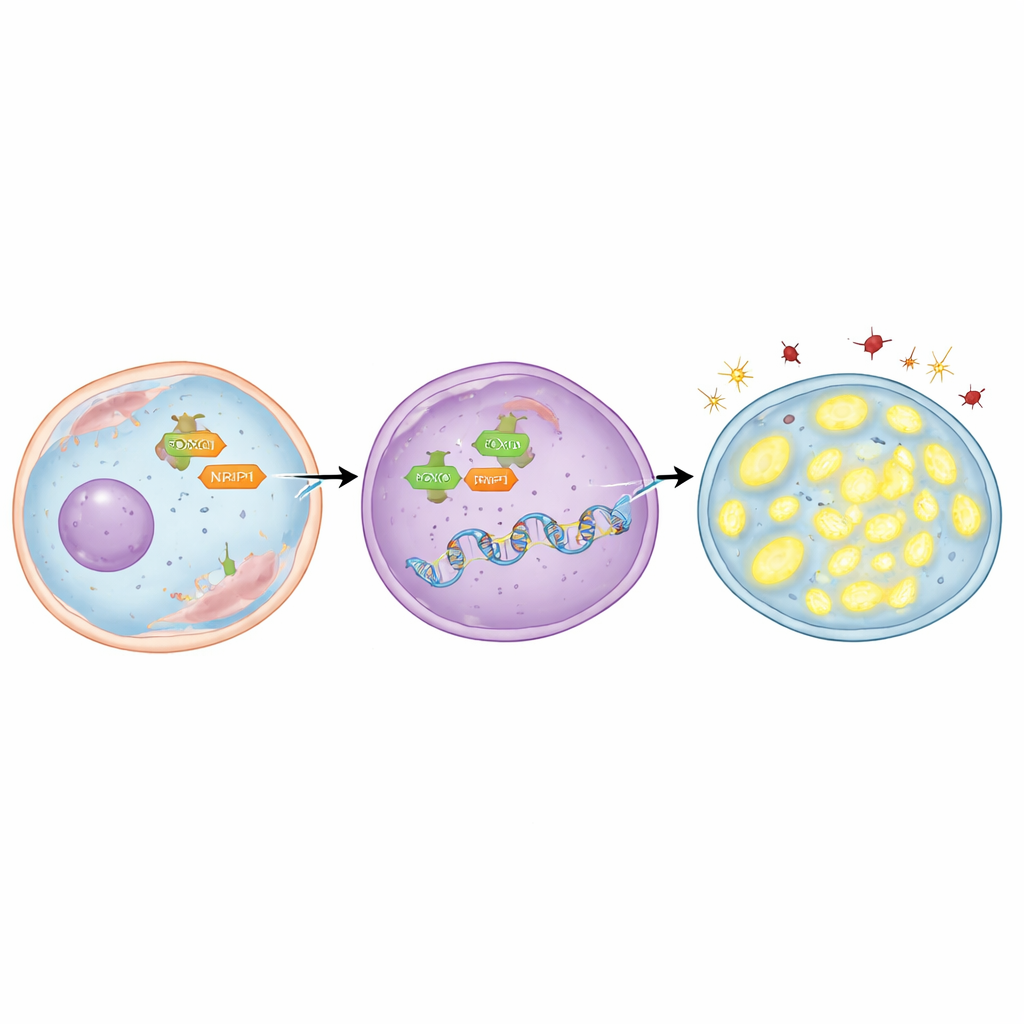
Per capire chi attiva TFAM, il gruppo si è concentrato su una proteina regolatrice chiamata FOXO3, che può spostarsi dall'interno liquido della cellula al nucleo, dove si prendono le decisioni genetiche. Hanno scoperto che il gene TFAM contiene diverse brevi sequenze di DNA a cui FOXO3 può legarsi. Utilizzando sia modellizzazione al computer sia tecniche di laboratorio che mappano i contatti proteina–DNA, hanno dimostrato che FOXO3 si lega direttamente a queste regioni. Nelle cellule di cancro polmonare radioresistenti, FOXO3 era presente in quantità maggiori e concentrato nel nucleo. Quando FOXO3 è stato ridotto sperimentalmente, i livelli di TFAM sono diminuiti, le molecole danneggiate si sono accumulate, i mitocondri hanno perso DNA e un maggior numero di cellule tumorali è morto dopo la radiazione. Al contrario, l'uso di un composto che favorisce la traslocazione di FOXO3 nel nucleo ha aumentato TFAM, preservato i mitocondri, ridotto il danno e reso le cellule più difficili da eliminare—salvo quando TFAM stessa era bloccata contemporaneamente.
Una proteina partner che potenzia la risposta protettiva
La storia non si ferma a FOXO3. I ricercatori hanno anche esaminato NRIP1, una proteina costituente che collabora con molti regolatori genici nel cancro. Hanno scoperto che NRIP1 interagisce fisicamente con FOXO3 e che questa partnership è più forte nelle cellule radioresistenti. In una linea cellulare di cancro polmonare che mancava naturalmente di NRIP1 funzionale, i livelli di TFAM erano relativamente bassi; il ripristino di NRIP1 normale ha aumentato TFAM senza cambiare la quantità totale di FOXO3. Nelle cellule radioresistenti che esprimevano NRIP1, il suo abbattimento ha ridotto TFAM, aumentato lo stress ossidativo, abbassato il DNA mitocondriale e spinto più cellule verso la morte dopo la radiazione. È importante sottolineare che NRIP1 non modificava la quantità di FOXO3 che raggiungeva il nucleo; agiva piuttosto come co-attivatore, rendendo FOXO3 più efficiente nell’attivare TFAM una volta che era già al suo posto.
Prove tratte da tumori in organismi viventi
Per verificare se questi eventi molecolari hanno rilevanza in un organismo completo, il gruppo ha impiantato cellule di cancro polmonare radioresistenti nei topi per formare tumori. Quando FOXO3 è stato stabilmente ridotto in queste cellule prima dell'impianto, i tumori risultanti crescevano più lentamente. L'aggiunta della radioterapia in combinazione con la riduzione di FOXO3 ha ridotto ulteriormente i tumori, senza danneggiare la salute complessiva degli animali. Questi tumori carenti di FOXO3 mostravano maggiore stress ossidativo, meno DNA mitocondriale, segni più marcati di morte cellulare e livelli di TFAM sostanzialmente più bassi. Nel complesso, questi risultati supportano l'idea che l'espressione di TFAM guidata da FOXO3, potenziata da NRIP1, aiuti i tumori a mantenere mitocondri robusti e a resistere alla radiazione in un sistema vivente.
Cosa significa per il futuro del trattamento del cancro polmonare
Per i non specialisti, la conclusione è che alcuni tumori polmonari diventano più resistenti alla radiazione rafforzando le loro centrali cellulari. Un trio di attori—FOXO3 che si sposta nel nucleo, NRIP1 che ne facilita l’azione e TFAM che rinforza i mitocondri—forma un circuito protettivo che permette alle cellule tumorali di riparare i danni e continuare a sopravvivere. Bloccando l’attività di FOXO3, interrompendo la sua collaborazione con NRIP1 o riducendo direttamente TFAM, future terapie potrebbero spogliare i tumori di questa armatura nascosta. Tali strategie potrebbero rendere la radioterapia standard più efficace, permettendo potenzialmente dosi più basse o un controllo migliore del tumore con meno fallimenti del trattamento.
Citazione: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Parole chiave: carcinoma polmonare non a piccole cellule, radioresistenza, mitocondri, FOXO3, TFAM