Clear Sky Science · de
NRIP1 ko‑aktiviert nukleär transloziertes FOXO3 zur Hochregulation von TFAM und fördert Radioresistenz bei nicht‑kleinzelligem Lungenkrebs
Warum es wichtig ist, Lungentherapien wirksamer zu machen
Die Strahlentherapie ist ein Grundpfeiler der Behandlung von nicht‑kleinzelligem Lungenkrebs, der häufigsten Form von Lungenkrebs. Dennoch lernen viele Tumoren im Verlauf, Bestrahlung zu überstehen, sodass die Erkrankung zurückkehren oder sich ausbreiten kann. Diese Studie stellt eine einfache, aber entscheidende Frage: Was läuft innerhalb der Krebszellen ab, das einigen von ihnen erlaubt, Strahlung zu widerstehen, und lassen sich diese inneren Mechanismen gegen den Tumor wenden, um die Therapie wirksamer zu machen?
Wie Krebszellen dem Strahlenschaden ausweichen
Strahlung tötet Krebszellen vor allem, indem sie Schübe schädlicher Moleküle, sogenannter reaktiver Sauerstoffspezies, erzeugt und DNA bricht. Diese Angriffe stehen in engem Zusammenhang mit den Kraftwerken der Zelle, den Mitochondrien. Die Forschenden stellten fest, dass radioresistente Lungenkrebszellen nicht nur nach Bestrahlung besser überleben, sondern auch mehr mitochondriale DNA und höhere Mengen eines zentralen mitochondrialen Proteins namens TFAM besitzen, das bei der Vervielfältigung und dem Schutz der mitochondrialen DNA hilft. Im Vergleich zu ihren ursprünglichen, nicht resistenten Gegenstücken zeigten diese resistenten Zellen weniger oxidative Schäden, weniger programmierter Zelltod und deutlich höhere TFAM‑Spiegel, was TFAM als wichtigen Schild identifiziert, der Krebszellen das Aushalten der Behandlung erleichtert.
Schalter im Zellkern, die diesen Schutz verstärken
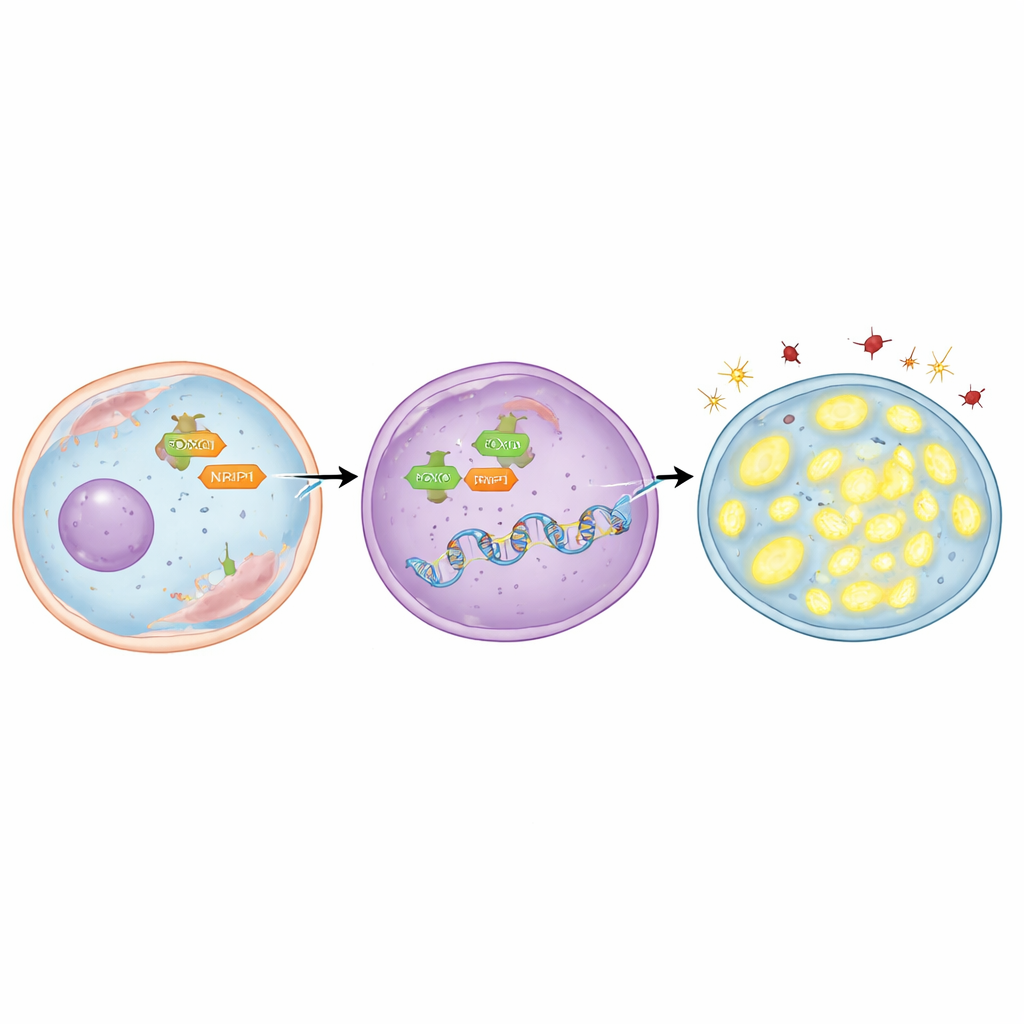
Um herauszufinden, wer TFAM „anschaltet“, konzentrierte sich das Team auf ein Regulationsprotein namens FOXO3, das aus dem zytoplasmatischen Bereich in den Zellkern wandern kann, wo genetische Entscheidungen getroffen werden. Sie entdeckten, dass das TFAM‑Gen mehrere kurze DNA‑Sequenzen enthält, an die FOXO3 andocken kann. Mithilfe von Computermodellen und Laborverfahren, die Protein‑DNA‑Interaktionen nachweisen, zeigten sie, dass FOXO3 direkt an diese Regionen bindet. In radioresistenten Lungenkrebszellen wurde FOXO3 in höheren Mengen und konzentriert im Zellkern gefunden. Wenn FOXO3 experimentell reduziert wurde, sanken die TFAM‑Spiegel, schädliche Moleküle häuften sich, Mitochondrien verloren DNA und nach Bestrahlung starben mehr Krebszellen. Umgekehrt erhöhte ein Wirkstoff, der FOXO3 in den Zellkern treibt, TFAM, schützte Mitochondrien, verringerte Schäden und machte die Zellen schwerer tödlich — es sei denn, TFAM wurde gleichzeitig blockiert.
Ein Helferprotein, das die Schutzreaktion verstärkt
Die Geschichte endet nicht bei FOXO3. Die Forschenden untersuchten zudem NRIP1, ein Helferprotein, das mit vielen Genregulatoren in Krebs zusammenarbeitet. Sie fanden heraus, dass NRIP1 physisch mit FOXO3 interagiert und dass diese Partnerschaft in radioresistenten Zellen stärker ausgeprägt ist. In einer Lungenkrebszelllinie, die naturgemäß keine funktionelle NRIP1 besaß, waren die TFAM‑Werte relativ niedrig; die Wiederherstellung von NRIP1 hob TFAM an, ohne die Gesamtmenge an FOXO3 zu verändern. In radioresistenten Zellen, die NRIP1 exprimierten, führte das Herunterregulieren von NRIP1 zu vermindertem TFAM, erhöhtem oxidativem Stress, verringerter mitochondrialer DNA und zu mehr Zelltod nach Bestrahlung. Wichtig ist: NRIP1 veränderte nicht die Menge an FOXO3, die den Zellkern erreichte; vielmehr fungierte es als Koaktivator und machte FOXO3 effektiver darin, TFAM einzuschalten, sobald FOXO3 bereits am Ort war.
Belege aus Tumoren in lebenden Tieren
Um zu prüfen, ob diese molekularen Vorgänge in einem ganzen Organismus relevant sind, setzten die Forschenden radioresistente Lungenkrebszellen in Mäuse ein, sodass Tumoren wuchsen. Wenn FOXO3 in diesen Zellen vor der Implantation dauerhaft reduziert wurde, wuchsen die resultierenden Tumoren langsamer. In Kombination mit Strahlentherapie schrumpften die Tumoren noch stärker, ohne die allgemeine Gesundheit der Tiere zu beeinträchtigen. Diese FOXO3‑reduzierten Tumoren zeigten mehr oxidativen Stress, weniger mitochondriale DNA, stärkere Anzeichen von Zelltod und deutlich geringere TFAM‑Spiegel. Zusammen stützen diese Befunde die Idee, dass FOXO3‑getriebene TFAM‑Expression, verstärkt durch NRIP1, Tumoren hilft, robuste Mitochondrien aufrechtzuerhalten und in einem lebenden System Strahlung zu widerstehen.
Was das für die zukünftige Lungenkrebsbehandlung bedeutet
Für Nicht‑Fachleute lautet die Botschaft: Manche Lungenkrebserkrankungen werden strahlenhart, indem sie ihre zellulären Kraftwerke stärken. Ein Trio aus FOXO3‑Translokation in den Zellkern, NRIP1‑Unterstützung und TFAM‑Stärkung der Mitochondrien bildet einen Schutzkreis, der Tumorzellen erlaubt, Schäden zu reparieren und weiter zu überleben. Durch das Blockieren der FOXO3‑Aktivität, das Stören seiner Partnerschaft mit NRIP1 oder das direkte Senken von TFAM könnten künftige Therapien Tumoren diese verborgene Rüstung nehmen. Solche Strategien könnten die Standard‑Strahlentherapie wirkungsvoller machen und möglicherweise niedrigere Dosen oder eine bessere Tumorkontrolle mit weniger Therapieversagen ermöglichen.
Zitation: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Schlüsselwörter: nicht‑kleinzelliger Lungenkrebs, Radioresistenz, Mitochondrien, FOXO3, TFAM