Clear Sky Science · fr
NRIP1 co-activate la translocation nucléaire de FOXO3 pour augmenter l'expression de TFAM et favoriser la radio-résistance dans le cancer du poumon non à petites cellules
Pourquoi améliorer l'efficacité des traitements du cancer du poumon est important
La radiothérapie est une pierre angulaire du traitement du cancer du poumon non à petites cellules, la forme la plus fréquente de cancer du poumon. Pourtant, de nombreuses tumeurs apprennent progressivement à survivre aux radiations, permettant à la maladie de réapparaître ou de se disséminer. Cette étude pose une question simple mais cruciale : que se passe-t-il à l'intérieur des cellules cancéreuses qui permet à certaines d'entre elles de résister aux radiations, et peut-on exploiter ces mécanismes internes contre la tumeur pour rendre le traitement plus efficace ?
Comment les cellules cancéreuses esquivent les dommages causés par les radiations
La radiation tue les cellules cancéreuses en grande partie en générant des rafales de molécules nocives appelées espèces réactives de l'oxygène et en endommageant l'ADN. Ces attaques sont étroitement liées aux centrales énergétiques de la cellule, les mitochondries. Les chercheurs ont observé que les cellules de cancer du poumon radio-résistantes non seulement survivent mieux après irradiation, mais présentent aussi davantage d'ADN mitochondrial et des niveaux accrus d'une protéine mitochondriale clé, TFAM, qui aide à copier et protéger l'ADN mitochondrial. Comparées à leurs homologues non résistantes, ces cellules résistantes présentaient moins de dommages oxydatifs, moins d'apoptose et des niveaux clairement plus élevés de TFAM, désignant TFAM comme un bouclier central aidant les cellules cancéreuses à endurer le traitement.
Interrupteurs dans le noyau cellulaire qui renforcent ce bouclier
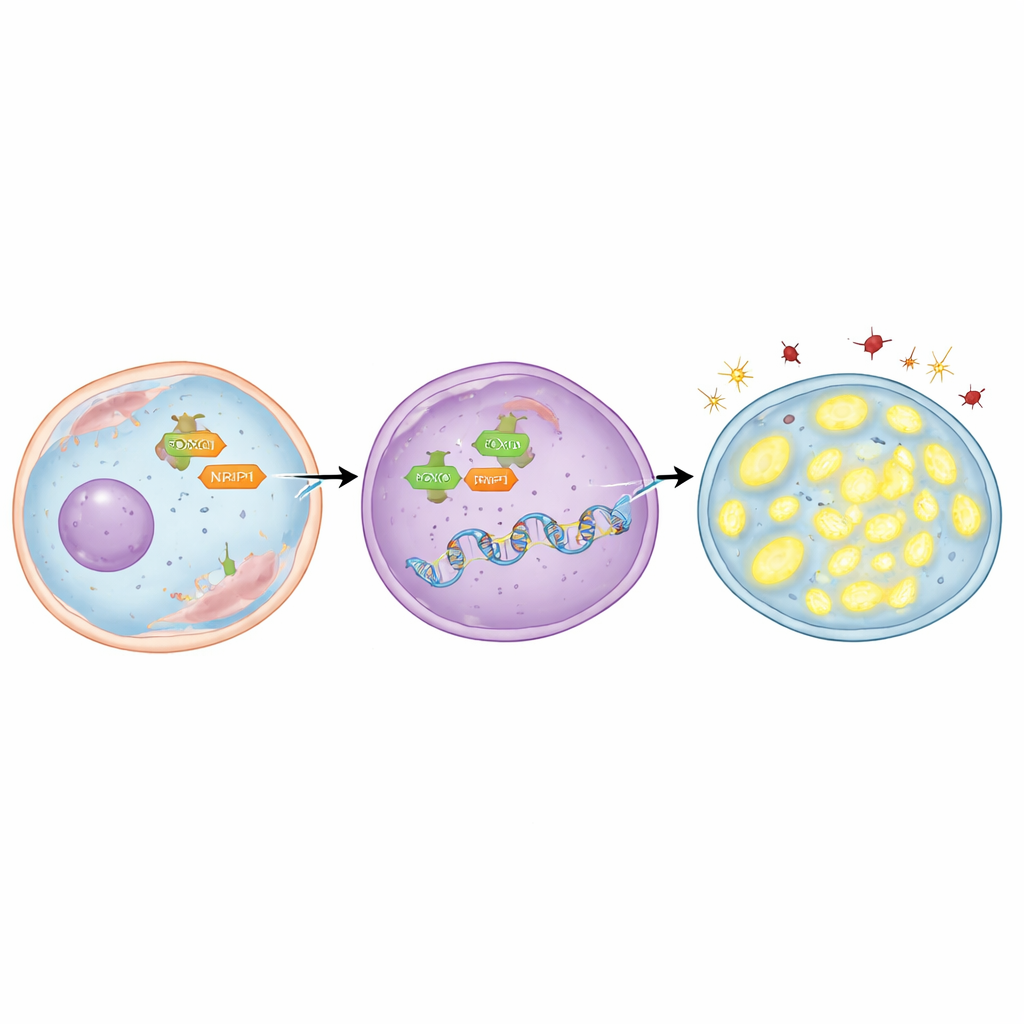
Pour savoir qui active TFAM, l'équipe s'est concentrée sur une protéine régulatrice appelée FOXO3, qui peut migrer du cytosol vers le noyau, là où se prennent les décisions génétiques. Ils ont découvert que le gène TFAM contient plusieurs courtes séquences d'ADN que FOXO3 peut reconnaître. À l'aide de modélisation informatique et de techniques de laboratoire cartographiant les contacts protéine–ADN, ils ont montré que FOXO3 se lie directement à ces régions. Dans les cellules radio-résistantes, FOXO3 était présent en quantités plus élevées et concentré dans le noyau. Quand FOXO3 était réduit expérimentalement, les niveaux de TFAM diminuaient, les molécules endommagées s'accumulaient, les mitochondries perdaient de l'ADN et davantage de cellules mouraient après irradiation. À l'inverse, l'utilisation d'un composé favorisant la translocation nucléaire de FOXO3 augmentait TFAM, préservait les mitochondries, réduisait les dommages et rendait les cellules plus difficiles à éliminer — sauf si TFAM était bloqué en même temps.
Une protéine auxiliaire qui amplifie la réponse protectrice
L'histoire ne s'arrête pas à FOXO3. Les chercheurs ont également étudié NRIP1, une protéine auxiliaire qui accompagne de nombreux régulateurs génétiques dans le cancer. Ils ont trouvé que NRIP1 interagit physiquement avec FOXO3 et que ce partenariat est renforcé dans les cellules radio-résistantes. Dans une lignée cellulaire de cancer du poumon qui manquait naturellement de NRIP1 fonctionnel, les niveaux de TFAM étaient relativement bas ; restaurer NRIP1 normal augmentait TFAM sans changer la quantité totale de FOXO3. Dans les cellules radio-résistantes exprimant NRIP1, réduire NRIP1 diminuait TFAM, augmentait le stress oxydatif, abaissait l'ADN mitochondrial et entraînait davantage de mort cellulaire après irradiation. De manière importante, NRIP1 n'altérait pas la quantité de FOXO3 atteignant le noyau ; elle agissait plutôt comme co-activateur, améliorant la capacité de FOXO3 à activer TFAM une fois installé sur l'ADN.
Preuves issues de tumeurs chez des animaux vivants
Pour tester si ces événements moléculaires ont une importance au niveau de l'organisme, l'équipe a implanté des cellules de cancer du poumon radio-résistantes chez des souris afin de former des tumeurs. Quand FOXO3 avait été durablement réduit dans ces cellules avant l'implantation, les tumeurs ainsi formées croissaient plus lentement. Ajouter la radiothérapie à la réduction de FOXO3 a encore diminué la taille des tumeurs, sans nuire à l'état de santé général des animaux. Ces tumeurs déficientes en FOXO3 montraient plus de stress oxydatif, moins d'ADN mitochondrial, des signes renforcés d'apoptose et des niveaux de TFAM sensiblement plus faibles. Ensemble, ces résultats soutiennent l'idée que l'expression de TFAM pilotée par FOXO3, amplifiée par NRIP1, aide les tumeurs à maintenir des mitochondries robustes et à résister aux radiations dans un système vivant.
Ce que cela signifie pour le traitement futur du cancer du poumon
Pour les non-spécialistes, la conclusion est que certains cancers du poumon deviennent résistants aux radiations en renforçant leurs centrales énergétiques cellulaires. Un trio d'acteurs — FOXO3 se déplaçant dans le noyau, NRIP1 l'aidant à fonctionner, et TFAM renforçant les mitochondries — forme un circuit protecteur qui permet aux cellules tumorales de réparer les dommages et de survivre. En bloquant l'activité de FOXO3, en perturbant son partenariat avec NRIP1, ou en réduisant directement TFAM, des thérapies futures pourraient dépouiller les tumeurs de cette armure cachée. De telles stratégies pourraient rendre la radiothérapie standard plus efficace, permettant potentiellement d'abaisser les doses ou d'améliorer le contrôle tumoral avec moins d'échecs thérapeutiques.
Citation: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Mots-clés: cancer du poumon non à petites cellules, radio-résistance, mitochondries, FOXO3, TFAM