Clear Sky Science · ru
NRIP1 коактивирует ядерно транслоцированный FOXO3 для повышения экспрессии TFAM и развития радиорезистентности при немелкоклеточном раке легкого
Почему важно повышать эффективность лечения рака легкого
Лучевая терапия — один из основных методов лечения немелкоклеточного рака легкого, наиболее распространенного типа рака легкого. Однако многие опухоли со временем учатся выживать после облучения, что позволяет болезни возвращаться или распространяться. В этом исследовании поставлен простой, но ключевой вопрос: что происходит внутри раковых клеток, что позволяет некоторым из них игнорировать радиацию, и можно ли эти внутренние механизмы обратить против опухоли, чтобы сделать лечение более эффективным?
Как раковые клетки уклоняются от повреждений, вызванных радиацией
Радиация убивает раковые клетки главным образом за счет генерации всплесков вредных молекул, называемых реактивными формами кислорода, и за счет разрывов ДНК. Эти атаки тесно связаны с энергостанциями клетки — митохондриями. Исследователи заметили, что радиорезистентные клетки рака легкого не только лучше выживают после облучения, но и содержат больше митохондриальной ДНК и более высокий уровень ключевого митохондриального белка TFAM, который помогает копировать и защищать митохондриальную ДНК. По сравнению с исходными, неустойчивыми к облучению клетками, эти резистентные клетки демонстрировали меньше окислительного повреждения, меньше апоптоза и заметно более высокие уровни TFAM, что указывает на TFAM как на центральный щит, помогающий клеткам выживать при лечении.
Переключатели в ядре, укрепляющие этот щит
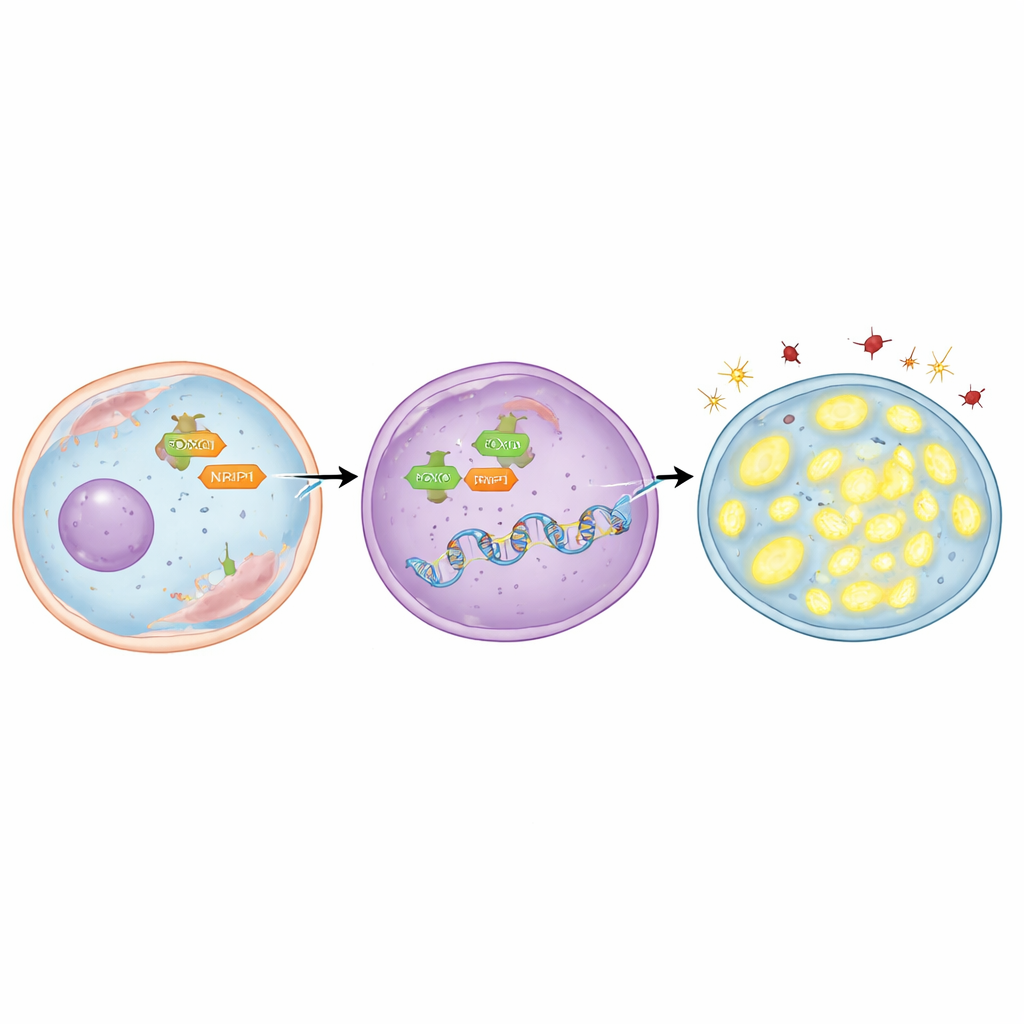
Чтобы выяснить, кто «включает» TFAM, команда сосредоточилась на регуляторном белке FOXO3, который может перемещаться из цитоплазмы в ядро, где принимаются генетические решения. Они обнаружили, что ген TFAM содержит несколько коротких последовательностей ДНК, к которым FOXO3 может прикрепляться. С помощью как компьютерного моделирования, так и лабораторных методов картирования контактов белок–ДНК показали, что FOXO3 напрямую связывается с этими участками. В радиорезистентных клетках легкого FOXO3 был в избытке и сосредоточен в ядре. При экспериментальном снижении уровня FOXO3 уровни TFAM падали, накапливались повреждающие молекулы, митохондрии теряли ДНК, и после облучения больше клеток погибало. Наоборот, применение соединения, которое стимулировало перемещение FOXO3 в ядро, повышало TFAM, сохраняло митохондрии, снижало повреждения и делало клетки труднее убиваемыми — если только TFAM одновременно не блокировали.
Белок-партнер, усиливающий защитную реакцию
История не заканчивается на FOXO3. Исследователи также изучили NRIP1, вспомогательный белок, который взаимодействует со многими регуляторами генов в раке. Они обнаружили, что NRIP1 физически взаимодействует с FOXO3 и что это партнерство сильнее в радиорезистентных клетках. В одной клеточной линии рака легкого, естественно лишенной функционального NRIP1, уровни TFAM были относительно низкими; восстановление нормального NRIP1 повышало TFAM без изменения общего количества FOXO3. В радиорезистентных клетках, экспрессирующих NRIP1, снижение NRIP1 уменьшало TFAM, увеличивало окислительный стресс, снижало количество митохондриальной ДНК и приводило к большему числу погибающих клеток после облучения. Важно, что NRIP1 не изменял то, сколько FOXO3 попадало в ядро; вместо этого он действовал как коактиватор, делая FOXO3 более эффективным в включении TFAM уже после его транслокации в ядро.
Доказательства на опухолях в живых организмах
Чтобы проверить, имеют ли эти молекулярные события значение в целом организме, команда имплантировала радиорезистентные клетки рака легкого мышам для формирования опухолей. Когда FOXO3 был стабильно снижен в этих клетках до имплантации, образующиеся опухоли росли медленнее. Добавление лучевой терапии на фоне снижения FOXO3 еще больше уменьшало опухоли, не нанося вреда общему здоровью животных. Эти опухоли с дефицитом FOXO3 демонстрировали более высокий окислительный стресс, меньше митохондриальной ДНК, сильнее признаки гибели клеток и значительно более низкий уровень TFAM. В совокупности эти данные подтверждают идею о том, что экспрессия TFAM, управляемая FOXO3 и усиленная NRIP1, помогает опухолям поддерживать функциональные митохондрии и выживать при облучении в живой системе.
Что это значит для будущего лечения рака легкого
Для неспециалистов вывод таков: некоторые раки легкого становятся устойчивыми к радиации, укрепляя свои клеточные энергетические центры. Трио действующих лиц — FOXO3, перемещающийся в ядро, NRIP1, помогающий ему работать, и TFAM, укрепляющий митохондрии — образует защитную цепь, позволяющую опухолевым клеткам исправлять повреждения и продолжать функционировать. Блокируя активность FOXO3, нарушая его взаимодействие с NRIP1 или непосредственно снижая TFAM, будущие терапии могут лишить опухоль этой скрытой брони. Такие подходы способны повысить эффективность стандартного облучения, потенциально позволяя применять меньшие дозы или обеспечивать лучшее подавление опухоли с меньшим числом неудач лечения.
Цитирование: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Ключевые слова: немелкоклеточный рак легкого, радиорезистентность, митохондрии, FOXO3, TFAM