Clear Sky Science · nl
NRIP1 activeert kern-getransloceerde FOXO3 om TFAM-expressie op te voeren en radioresistentie te bevorderen bij niet-kleincellig longkanker
Waarom het beter laten werken van longkankerbehandelingen belangrijk is
Radiotherapie is een pijler in de behandeling van niet-kleincellige longkanker, de meest voorkomende vorm van longkanker. Toch leren veel tumoren na verloop van tijd om straling te overleven, waardoor de ziekte kan terugkeren of uitzaaien. Deze studie stelt een eenvoudige maar cruciale vraag: wat gebeurt er binnenin kankercellen waardoor sommige van hen straling kunnen weerstaan, en kunnen die interne mechanismen tegen de tumor worden gekeerd om de behandeling effectiever te maken?
Hoe kankercellen de schade door straling ontwijken
Straling doodt kankercellen grotendeels door het veroorzaken van uitbarstingen van schadelijke moleculen die reactieve zuurstofsoorten worden genoemd en door het breken van DNA. Deze aanvallen zijn nauw verbonden met de energiecentrales van de cel, de mitochondriën. De onderzoekers merkten dat radioresistente longkankercellen niet alleen beter overleven na bestraling, maar ook meer mitochondriaal DNA en hogere niveaus hebben van een sleutelproteïne in mitochondriën genaamd TFAM, dat helpt bij het kopiëren en beschermen van mitochondriaal DNA. Wanneer deze resistente cellen werden vergeleken met hun oorspronkelijke, niet-resistente tegenhangers, vertoonden ze minder oxidatieve schade, minder geprogrammeerde celdood en duidelijk hogere TFAM-niveaus, wat TFAM aanwijst als een centraal schild dat kankercellen helpt behandeling te doorstaan.
Schakelaars in de celkern die dit schild versterken
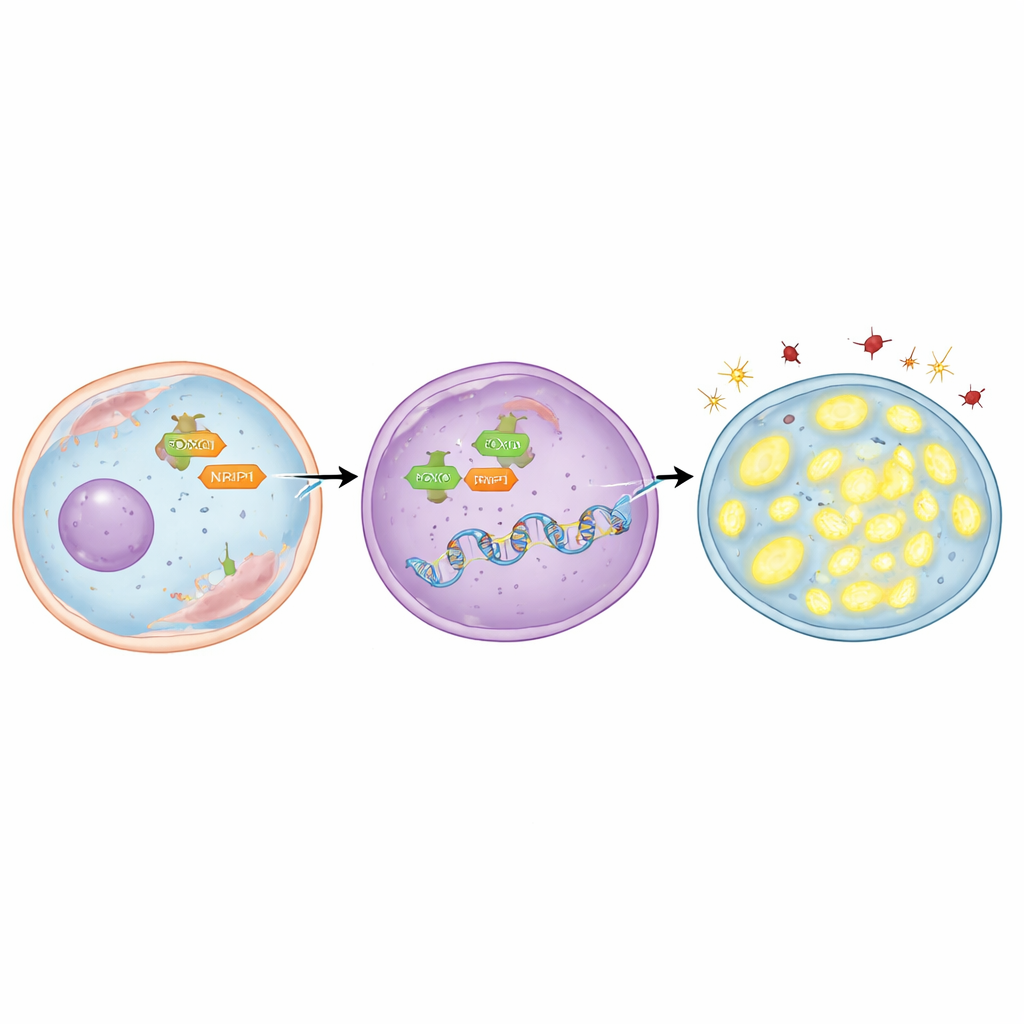
Om te ontdekken wie TFAM “aanzet”, richtte het team zich op een regulerend eiwit genaamd FOXO3, dat kan verschuiven van het vochtige deel van de cel naar de kern, waar genetische beslissingen worden gemaakt. Ze ontdekten dat het TFAM-gen meerdere korte DNA-sequenties bevat waaraan FOXO3 zich kan hechten. Met behulp van zowel computermodellen als laboratoriumtechnieken die eiwit–DNA-contacten in kaart brengen, lieten ze zien dat FOXO3 rechtstreeks aan deze regio’s bindt. In radioresistente longkankercellen werd FOXO3 in hogere hoeveelheden en geconcentreerd in de kern aangetroffen. Wanneer FOXO3 experimenteel werd verminderd, daalden TFAM-niveaus, bouwden schadelijke moleculen zich op, verloren mitochondriën DNA en stierven meer kankercellen na bestraling. Omgekeerd verhoogde het gebruik van een verbinding die FOXO3 naar de kern stuurt TFAM, beschermde mitochondriën, verlaagde schade en maakte cellen moeilijker te doden—tenzij TFAM zelf gelijktijdig werd geblokkeerd.
Een hulp-eiwit dat de beschermende respons versterkt
Het verhaal stopt niet bij FOXO3. De onderzoekers onderzochten ook NRIP1, een helper-eiwit dat samenwerkt met veel genregulatoren in kanker. Ze vonden dat NRIP1 fysiek interageert met FOXO3 en dat deze samenwerking sterker is in radioresistente cellen. In één longkankercellijn die van nature geen functioneel NRIP1 had, waren TFAM-niveaus relatief laag; het herstellen van normaal NRIP1 verhoogde TFAM zonder de totale hoeveelheid FOXO3 te veranderen. In radioresistente cellen die NRIP1 wel tot expressie brachten, leidde het verminderen van NRIP1 tot lagere TFAM-niveaus, verhoogde oxidatieve stress, minder mitochondriaal DNA en meer celdood na bestraling. Belangrijk is dat NRIP1 niet veranderde hoeveel FOXO3 de kern bereikte; in plaats daarvan fungeerde het als co-activator, waardoor FOXO3 beter in staat was TFAM aan te zetten zodra het eenmaal aanwezig was.
Bewijs uit tumoren in levende dieren
Om te testen of deze moleculaire gebeurtenissen relevant zijn in een heel organisme, plaatste het team radioresistente longkankercellen in muizen om tumoren te vormen. Wanneer FOXO3 stabiel werd verminderd in deze cellen vóór implantatie, groeiden de resulterende tumoren langzamer. Het toevoegen van radiotherapie bovenop FOXO3-reductie verkleinde tumoren nog verder, zonder de algehele gezondheid van de dieren te schaden. Deze FOXO3-deficiënte tumoren vertoonden meer oxidatieve stress, minder mitochondriaal DNA, sterkere tekenen van celdood en aanzienlijk lagere TFAM-niveaus. Samen ondersteunen deze bevindingen het idee dat door FOXO3 aangedreven TFAM-expressie, versterkt door NRIP1, tumoren helpt robuuste mitochondriën te behouden en straling te weerstaan in een levend systeem.
Wat dit betekent voor toekomstige behandeling van longkanker
Voor niet-specialisten is de conclusie dat sommige longkankers radiatiebestendiger worden door hun cellulaire energiecentrales te versterken. Een trio van spelers—FOXO3 dat naar de kern verhuist, NRIP1 dat helpt bij de werking en TFAM dat de mitochondriën versterkt—vormt een beschermend circuit dat tumorcellen in staat stelt schade te repareren en door te gaan. Door de activiteit van FOXO3 te blokkeren, de samenwerking met NRIP1 te verstoren of TFAM direct te verlagen, zouden toekomstige therapieën tumoren deze verborgen bescherming kunnen ontnemen. Zulke strategieën kunnen standaardbestraling effectiever maken, mogelijk lagere doses toelaten of betere tumorkontrole met minder behandeluitval opleveren.
Bronvermelding: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Trefwoorden: niet-kleincellig longkanker, radioresistentie, mitochondriën, FOXO3, TFAM