Clear Sky Science · sv
NRIP1 samaktiverar nukleärt translocerat FOXO3 för att uppreglera TFAM-uttryck och främja radioresistens i icke-småcellig lungcancer
Varför det spelar roll att förbättra behandlingar mot lungcancer
Strålbehandling är en hörnsten i behandlingen av icke-småcellig lungcancer, den vanligaste typen av lungcancer. Många tumörer lär sig dock med tiden att överleva strålning, vilket gör att sjukdomen kan återkomma eller sprida sig. Denna studie ställer en enkel men central fråga: vad händer inne i cancercellerna som gör att några av dem klarar strålningen, och kan dessa inre mekanismer vändas mot tumören för att göra behandlingen mer effektiv?
Hur cancerceller undflyr strålningsskador
Strålning dödar i huvudsak cancerceller genom att generera svall av skadliga molekyler, så kallade reaktiva syrearter, och genom att bryta DNA. Dessa angrepp är nära kopplade till cellens kraftstationer, mitokondrierna. Forskarna noterade att radioresistenta lungcancerceller inte bara överlever bättre efter strålning utan också har mer mitokondriellt DNA och högre nivåer av ett nyckelprotein i mitokondrierna, TFAM, som hjälper till att kopiera och skydda mitokondriellt DNA. När dessa resistenta celler jämfördes med sina ursprungliga, icke-resistenta motsvarigheter, visade de mindre oxidativ skada, mindre programmerad celldöd och tydligt högre TFAM-nivåer, vilket pekar på TFAM som en central sköld som hjälper cancerceller att stå emot behandlingen.
Växlar inne i cellkärnan som förstärker detta skydd
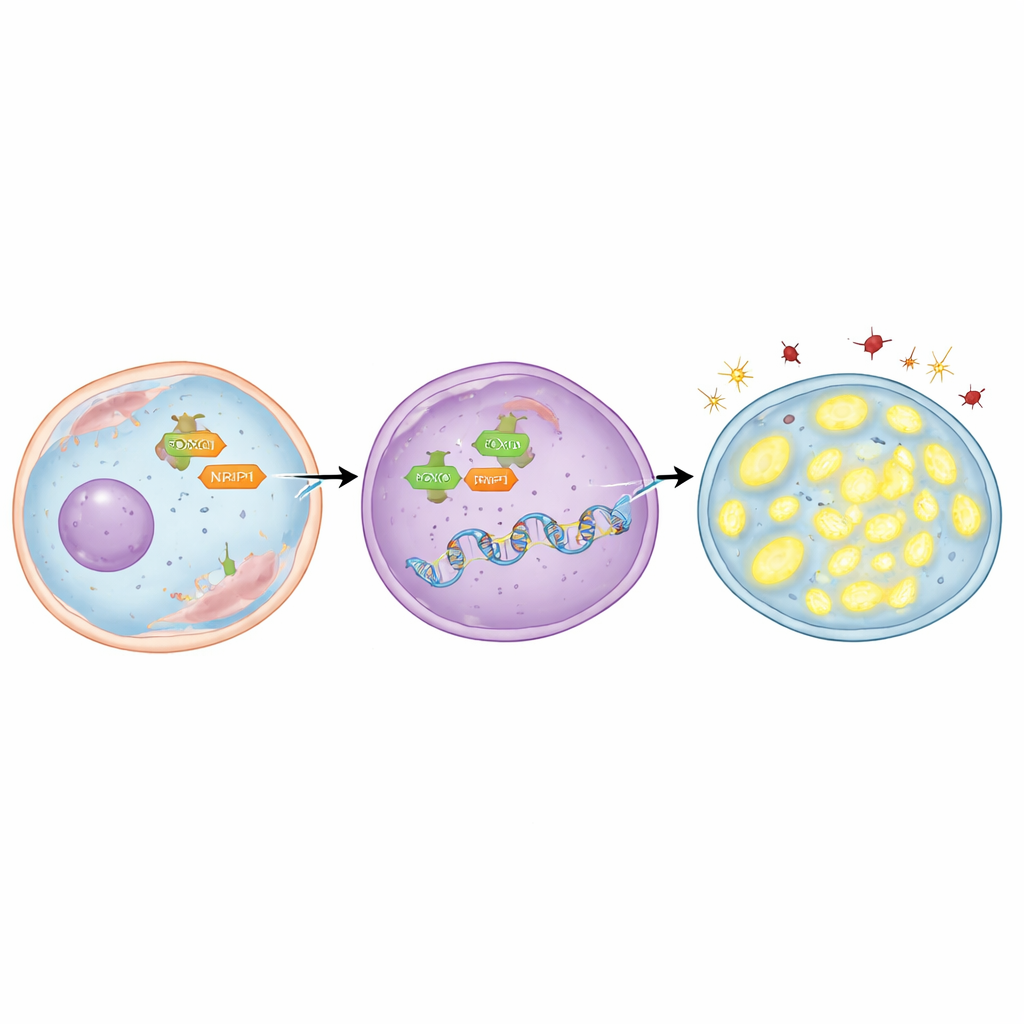
För att ta reda på vem som slår på TFAM fokuserade teamet på ett reglerande protein kallat FOXO3, som kan röra sig från cellens vätskeinnehåll in i kärnan där genetiska beslut fattas. De upptäckte att TFAM-genen innehåller flera korta DNA-sekvenser som FOXO3 kan haka i. Genom både datormodellering och laboratorietekniker som kartlägger protein–DNA-kontakter visade de att FOXO3 binder direkt till dessa regioner. I radioresistenta lungcancerceller fanns FOXO3 i högre mängd och var koncentrerad i kärnan. När FOXO3 experimentellt minskades föll TFAM-nivåerna, skadliga molekyler byggdes upp, mitokondrier förlorade DNA och fler cancerceller dog efter strålning. Omvänt ökade ett ämne som driver FOXO3 in i kärnan TFAM, bevarade mitokondrier, minskade skador och gjorde cellerna svårare att döda — om inte TFAM samtidigt blockerades.
Ett hjälpprotein som förstärker det skyddande svaret
Berättelsen slutar inte med FOXO3. Forskarna undersökte också NRIP1, ett hjälpprotein som samarbetar med många genregulatorer i cancer. De fann att NRIP1 fysisk interagerar med FOXO3 och att detta partnerskap är starkare i radioresistenta celler. I en linskategori av lungcancerceller som naturligt saknade fungerande NRIP1 var TFAM-nivåerna relativt låga; att återställa normal NRIP1 ökade TFAM utan att förändra den totala mängden FOXO3. I radioresistenta celler som uttryckte NRIP1 gav nedslående av NRIP1 lägre TFAM, ökade oxidativ stress, minskat mitokondrie-DNA och fler celler som gick i död efter strålning. Viktigt är att NRIP1 inte förändrade hur mycket FOXO3 som nådde kärnan; istället agerade det som en samaktivator och gjorde FOXO3 bättre på att slå på TFAM när FOXO3 väl satt på plats.
Bevis från tumörer i levande djur
För att testa om dessa molekylära händelser spelar roll i en hel organism implanterade teamet radioresistenta lungcancerceller i möss för att bilda tumörer. När FOXO3 stabilt reducerades i dessa celler före implantation växte de resulterande tumörerna långsammare. Att lägga till strålbehandling ovanpå FOXO3-reduktionen krympte tumörerna ännu mer, utan att skada djurens allmänna hälsa. Dessa FOXO3-bristfälliga tumörer visade mer oxidativ stress, mindre mitokondrie-DNA, starkare tecken på celldöd och avsevärt lägre TFAM-nivåer. Tillsammans stöder dessa fynd idén att FOXO3-driven TFAM-expression, förstärkt av NRIP1, hjälper tumörer att bibehålla robusta mitokondrier och stå emot strålning i ett levande system.
Vad detta betyder för framtida behandling av lungcancer
För icke-specialister är slutsatsen att vissa lungcancerformer blir stråltåliga genom att förstärka sina cellulära kraftverk. En trio av aktörer — FOXO3 som flyttar in i kärnan, NRIP1 som hjälper det att fungera, och TFAM som stärker mitokondrierna — bildar en skyddscirkel som låter tumörceller reparera skador och fortsätta växa. Genom att blockera FOXO3:s aktivitet, störa dess samarbete med NRIP1 eller direkt sänka TFAM kan framtida terapier ta ifrån tumörer denna dolda rustning. Sådana strategier kan göra standardstrålning mer effektiv, vilket möjligen tillåter lägre doser eller bättre tumörkontroll med färre behandlingsmisslyckanden.
Citering: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Nyckelord: icke-småcellig lungcancer, radioresistens, mitokondrier, FOXO3, TFAM