Clear Sky Science · tr
NRIP1, nükleer translöke olmuş FOXO3’ü ortak olarak aktive ederek TFAM ekspresyonunu artırır ve küçük hücre dışı olmayan akciğer kanserinde radyorezistansı destekler
Akciğer kanseri tedavilerini daha etkili hale getirmenin önemi
Radyoterapi, akciğer kanserlerinin en yaygın türü olan küçük hücre dışı akciğer kanserinin tedavisinde temel bir yaklaşımdır. Ancak birçok tümör zamanla radyasyona karşı hayatta kalmayı öğrenir ve bu da hastalığın nüks etmesine veya yayılmasına olanak verir. Bu çalışma basit ama hayati bir soruyu soruyor: bazı kanser hücrelerinin radyasyonu atlatmasına izin veren hücre içi süreçlerde neler oluyor ve bu iç mekanizmalar tedaviyi daha etkili kılmak için tümöre karşı kullanılabilir mi?
Kanser hücreleri radyasyonun verdiği zarardan nasıl sıyrılıyor
Radyasyon, kanser hücrelerini büyük ölçüde reaktif oksijen türleri adı verilen zararlı moleküllerin ani artışlarını oluşturarak ve DNA kırıkları yaratarak öldürür. Bu saldırılar hücrenin enerji istasyonları olan mitokondrilerle yakından bağlantılıdır. Araştırmacılar, radyorezistan akciğer kanseri hücrelerinin yalnızca radyasyon sonrası daha iyi hayatta kalmakla kalmadığını, aynı zamanda daha fazla mitokondriyal DNA’ya ve mitokondriyal DNA’yı kopyalayan ve koruyan anahtar bir protein olan TFAM seviyelerinin daha yüksek olduğuna dikkat etti. Bu dirençli hücreler orijinal, dirençsiz muadilleriyle karşılaştırıldığında daha az oksidatif hasar, daha az programlı hücre ölümü ve belirgin şekilde daha yüksek TFAM seviyeleri gösterdi; bu da TFAM’i hücrelerin tedaviye dayanmasına yardımcı olan merkezi bir kalkan olarak işaretliyor.
Bu kalkanı güçlendiren çekirdek içi anahtarlar
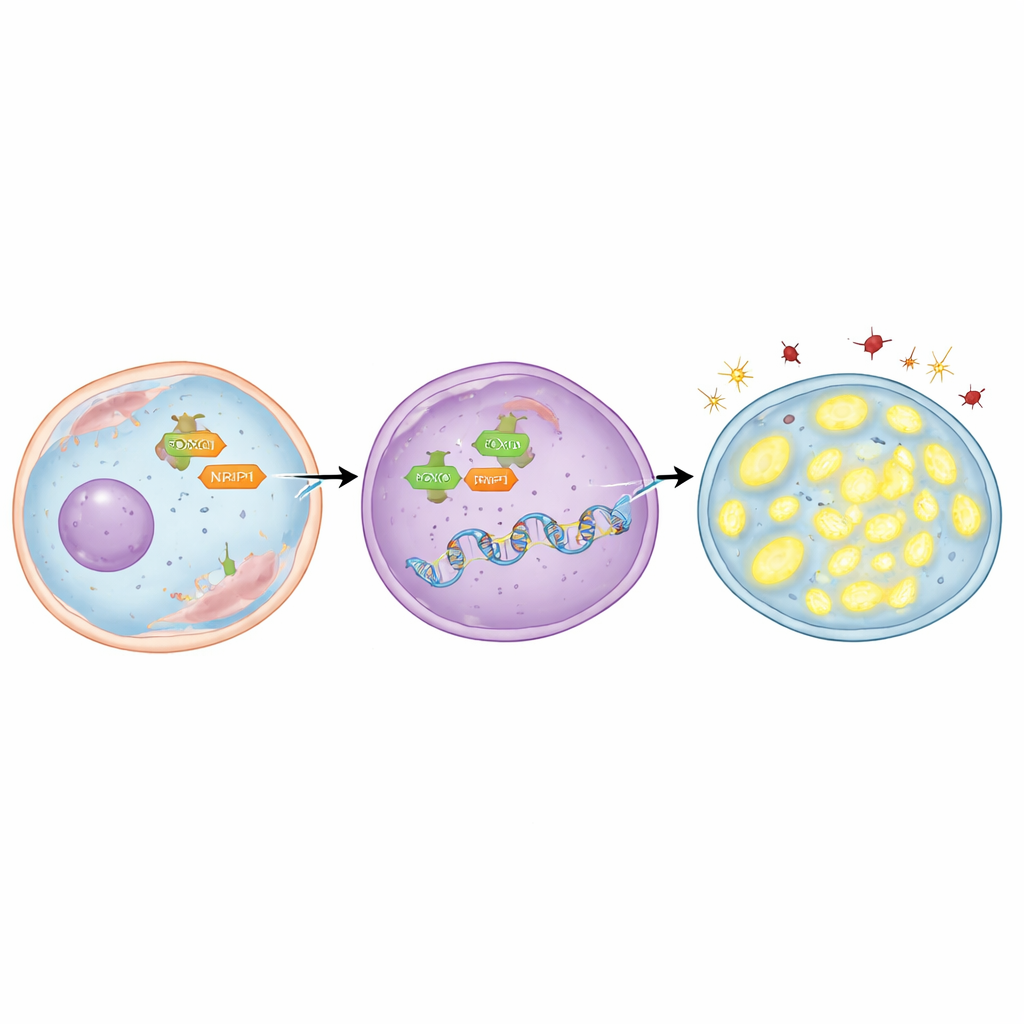
TFAM’ı kimin “açtığını” bulmak için ekip, hücrenin sulu içinden çekirdeğe geçebilen ve genetik kararların alındığı yerde etkinlik gösteren düzenleyici bir protein olan FOXO3’e odaklandı. TFAM geninin FOXO3’ün bağlanabileceği birkaç kısa DNA dizisi içerdiğini keşfettiler. Hem bilgisayar modellemeleri hem de protein–DNA temaslarını haritalayan laboratuvar teknikleri kullanarak FOXO3’ün bu bölgelerle doğrudan bağlandığını gösterdiler. Radyorezistan akciğer kanseri hücrelerinde FOXO3 daha yüksek miktarlarda bulundu ve çekirdekte yoğunlaştı. FOXO3 deneysel olarak azaltıldığında TFAM seviyeleri düştü, zararlı moleküller birikti, mitokondriler DNA kaybetti ve radyasyon sonrası daha fazla kanser hücresi öldü. Buna karşılık, FOXO3’ü çekirdeğe yönlendiren bir bileşik kullanmak TFAM’ı artırdı, mitokondrileri korudu, hasarı azalttı ve hücreleri öldürmeyi zorlaştırdı—ancak TFAM eş zamanlı olarak bloke edilirse bu etki ortadan kalktı.
Korumayı güçlendiren bir yardımcı protein
Hikâye FOXO3 ile bitmiyor. Araştırmacılar ayrıca kanserde birçok gen düzenleyicisiyle ortaklık yapan bir yardımcı protein olan NRIP1’i inceledi. NRIP1’in fiziksel olarak FOXO3 ile etkileştiğini ve bu ortaklığın radyorezistan hücrelerde daha güçlü olduğunu buldular. Doğal olarak işlevsel NRIP1’den yoksun olan bir akciğer kanseri hücre hattında TFAM seviyeleri nispeten düşüktü; normal NRIP1’i geri kazandırmak TFAM’ı FOXO3’ün toplam miktarını değiştirmeden yükseltti. NRIP1 ifade eden radyorezistan hücrelerde NRIP1’in baskılanması TFAM’ı azalttı, oksidatif stresi artırdı, mitokondriyal DNA’yı düşürdü ve radyasyon sonrası daha fazla hücrenin ölümüne yol açtı. Önemli olarak NRIP1, FOXO3’ün çekirdeğe ulaşan miktarını değiştirmedi; bunun yerine bir ortak aktivatör olarak görev yaparak FOXO3 çekirdekte bulunduğunda TFAM’ı daha etkili şekilde açmasını sağladı.
Canlı hayvanlardaki tümörlerden elde edilen kanıtlar
Bu moleküler olayların bir bütün organizmada önemli olup olmadığını test etmek için ekip, radyorezistan akciğer kanseri hücrelerini farelere implante ederek tümörler oluşturdu. Bu hücrelerde FOXO3 stabil şekilde azaltıldığında, oluşan tümörler daha yavaş büyüdü. FOXO3 azaltımına radyoterapi eklemek tümörleri daha da küçülttü ve hayvanların genel sağlığına zarar vermedi. Bu FOXO3-eksik tümörler daha fazla oksidatif stres, daha az mitokondriyal DNA, daha güçlü hücre ölümü belirtileri ve belirgin derecede düşük TFAM seviyeleri gösterdi. Birlikte bu bulgular, NRIP1 tarafından güçlendirilen FOXO3 kaynaklı TFAM ekspresyonunun tümörlerin sağlam mitokondrileri korumasına ve canlı bir sistemde radyasyona dayanmasına yardımcı olduğunu destekliyor.
Gelecekteki akciğer kanseri tedavileri için anlamı
Uzman olmayanlar için çıkarılacak ders, bazı akciğer kanserlerinin hücresel enerji santrallerini güçlendirerek radyasyona karşı sertleştiğidir. Çekirdeğe geçen FOXO3, ona yardımcı olan NRIP1 ve mitokondrileri güçlendiren TFAM’dan oluşan üçlü bir birlik, tümör hücrelerinin hasarı onarmasına ve devam etmesine izin veren koruyucu bir devre oluşturur. FOXO3’ün aktivitesini engelleyerek, NRIP1 ile ortaklığını bozarak veya doğrudan TFAM’ı düşürerek gelecekteki terapiler tümörlerden bu gizli zırhı soyabilir. Bu tür stratejiler standart radyoterapinin daha etkili olmasını sağlayabilir; potansiyel olarak daha düşük dozlarla veya daha az tedavi başarısızlığıyla daha iyi tümör kontrolü mümkün olabilir.
Atıf: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, radyorezistans, mitokondri, FOXO3, TFAM