Clear Sky Science · he
NRIP1 מעלה שעתוק של FOXO3 שעובר לגרעין כדי להגביר את ביטוי TFAM ולקדם עמידות לקרינה בסרטן ריאות שאינו תאי קטן
מדוע חשוב לשפר את הטיפולים בסרטן ריאות
הקרנות מהוות אב-סיס בטיפול בסרטן ריאות שאינו תאי קטן, הסוג הנפוץ ביותר של סרטן הריאה. עם זאת, גידולים רבים לומדים בהדרגה לשרוד קרינה, מה שמאפשר למחלה לשוב או להתפשט. המחקר הזה בוחן שאלה פשוטה אך מכרעת: מה מתרחש בתוך תאי הסרטן שמאפשר לחלק מהם לעמוד בקרינה, והאם ניתן לנצל את המנגנונים הפנימיים הללו נגד הגידול כדי לשפר את יעילות הטיפול?
איך תאי סרטן מתחמקים מנזק הקרינה
קרינה הורגת תאי סרטן בעיקר על ידי יצירת פרצי מולקולות מזיקות שנקראות מינים פעילי חמצן ופגיעה ב-DNA. ההתקפות האלה קשורות קשר הדוק לתחנות הכוח של התא — המיטוכונדריות. החוקרים הבחינו שתאי סרטן ריאות עמידים לקרינה לא רק שורדים טוב יותר לאחר חשיפה לקרינה, אלא גם מכילים יותר DNA מיטוכונדריאלי ורמות גבוהות יותר של חלבון מיטוכונדריאלי מרכזי בשם TFAM, שמסייע לשכפל ולהגן על ה-DNA המיטוכונדריאלי. בהשוואה לתאים המקוריים הלא-עמידים, התאים העמידים הראו פחות נזק חמצוני, פחות מוות מתוכנת ורמות TFAM באופן מובהק גבוהות יותר, מה שמצביע על TFAM כמגן מרכזי המסייע לתאים החזקים לעמוד בטיפול.
מפסקים בתוך גרעין התא שמחזקים את המגן הזה
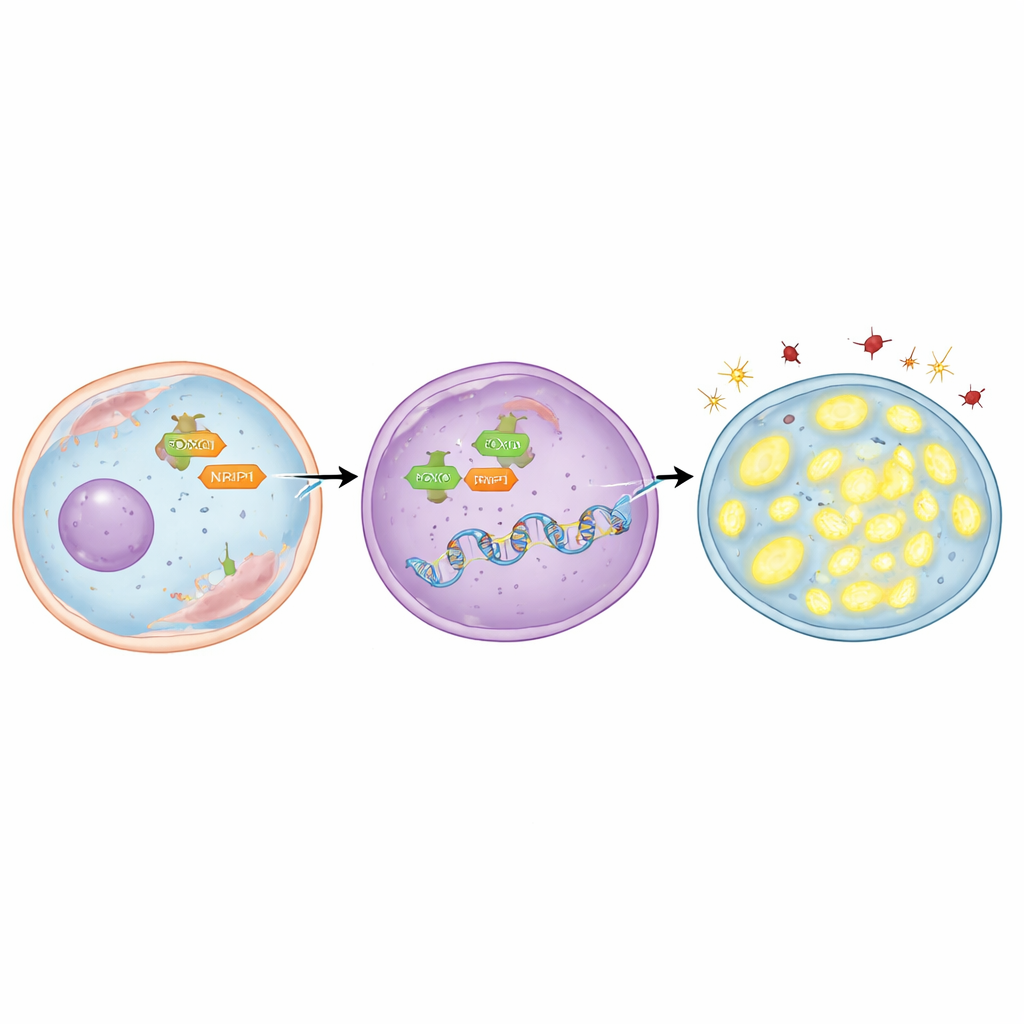
כדי לגלות מי מדליק את TFAM, הצוות התמקד בחלבון בקרה בשם FOXO3, שיכול לעבור מציטופלזמה לגרעין התא, שם מתקבלות ההחלטות הגנטיות. הם גילו שלגן ה-TFAM יש כמה רצפי DNA קצרים שעליהם FOXO3 יכול לקשור. באמצעות הדמיה ממוחשבת וטכניקות מעבדה שממפות מגעים בין חלבון ל-DNA, הראו שה-FOXO3 נקשר ישירות לאזורים אלה. בתאי סרטן ריאות עמידים לקרינה נמצאו רמות גבוהות יותר של FOXO3 והיא הייתה מרוכזת בגרעין. כאשר הפחיתו את FOXO3 בניסוי, רמות TFAM ירדו, חומרים מזיקים הצטברו, המיטוכונדריות איבדו DNA, ועוד תאים מתו לאחר קרינה. לעומת זאת, שימוש במחבר שמניע את FOXO3 לגרעין הגדיל את TFAM, שמר על המיטוכונדריות, הפחית נזק והקשה על השמדת התאים — אלא אם TFAM עצמו נחסם במקביל.
חלבון מסייע שמחזק את התגובה ההגנתית
הסיפור אינו מסתיים ב-FOXO3. החוקרים בחנו גם את NRIP1, חלבון מסייע שמשתף פעולה עם רגולטורים רבים של גנים בסרטן. הם מצאו ש-NRIP1 יוצר אינטראקציה פיזית עם FOXO3 ושהשותפות הזו חזקה יותר בתאים עמידים לקרינה. בקו תאי ריאות אחד שלגביו NRIP1 לא היה תפקודי באופן טבעי, רמות TFAM היו יחסית נמוכות; השבתת NRIP1 הרגיל החזירה את TFAM ללא שינוי בכמות הכוללת של FOXO3. בתאים עמידים שביטאו NRIP1, דיכוי NRIP1 הוריד את TFAM, הגדיל מתח חמצוני, הקטין את ה-DNA המיטוכונדריאלי ודחף יותר תאים למות לאחר קרינה. חשוב לציין ש-NRIP1 לא שינה כמה FOXO3 הגיע לגרעין; במקום זאת הוא פעל כקו-אקטיבטור, שהפך את FOXO3 ליעיל יותר בהפעלת TFAM לאחר שכבר נמצא במקום.
ראיות מגידולים בחיות חיות
כדי לבדוק האם האירועים המולקולריים האלו חשובים במערכת חיה, הצוות השתיל בתימאים תאי סרטן ריאות עמידים לקרינה ויצר גידולים. כאשר FOXO3 הוקטן באופן יציב בתאים אלה לפני ההשתלה, הגידולים שנוצרו גדלו לאט יותר. הוספת הקרנות בנוסף לדיכוי FOXO3 הקטינה את הגידולים עוד יותר, מבלי לגרום לנזק כללי לבריאות החיות. הגידולים הדלים ב-FOXO3 הראו מתח חמצוני גבוה יותר, פחות DNA מיטוכונדריאלי, סימנים חזקים יותר של מוות תאי ורמות TFAM נמוכות בהרבה. יחד, הממצאים האלה תומכים ברעיון שביטוי TFAM מונע על ידי FOXO3 ומוגבר על ידי NRIP1 מסייע לגידולים לשמור על מיטוכונדריות חזקות ולעמוד בקרינה במערכת חיה.
מה המשמעות של זה לטיפול עתידי בסרטן ריאות
ללא-מומחים, המסקנה היא שחלק מסוגי סרטן הריאה מתגבשים לעמידות לקרינה על ידי חיזוק תחנות הכוח התאית שלהם. שלישייה של שחקנים — FOXO3 שנכנס לגרעין, NRIP1 שעוזר לו לפעול, ו-TFAM שמחזקת את המיטוכונדריה — יוצרת מעגל מגן שמאפשר לתאי הגידול לתקן נזקים ולהמשיך לתפקד. על ידי חסימת הפעילות של FOXO3, שיבוש שותפותו עם NRIP1, או הורדה ישירה של TFAM, טיפולים עתידיים עשויים לפשוט מהגידול את השריון הסמוי הזה. אסטרטגיות כאלה יכולות להפוך את הקרינה הסטנדרטית ליעילה יותר, ובפוטנציה לאפשר מינונים נמוכים יותר או שליטה טובה יותר בגידול עם פחות כישלונות בטיפול.
ציטוט: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
מילות מפתח: סרטן ריאות שאינו תאי קטן, עמידות לקרינה, מיטוכונדריה, FOXO3, TFAM