Clear Sky Science · pl
NRIP1 współaktywuje jądrowo przemieszczenie FOXO3 w celu zwiększenia ekspresji TFAM i promowania radiooporności w niedrobnokomórkowym raku płuca
Dlaczego poprawa skuteczności terapii raka płuca ma znaczenie
Radioterapia jest podstawową metodą leczenia niedrobnokomórkowego raka płuca, najczęstszego typu raka płuca. Mimo to wiele guzów z czasem uczy się przetrwać napromienianie, co pozwala chorobie na nawrót lub rozprzestrzenianie się. W tym badaniu postawiono proste, lecz kluczowe pytanie: co dzieje się wewnątrz komórek nowotworowych, że niektóre z nich ignorują działanie promieniowania, i czy te wewnętrzne mechanizmy można wykorzystać przeciw guzowi, aby zwiększyć skuteczność leczenia?
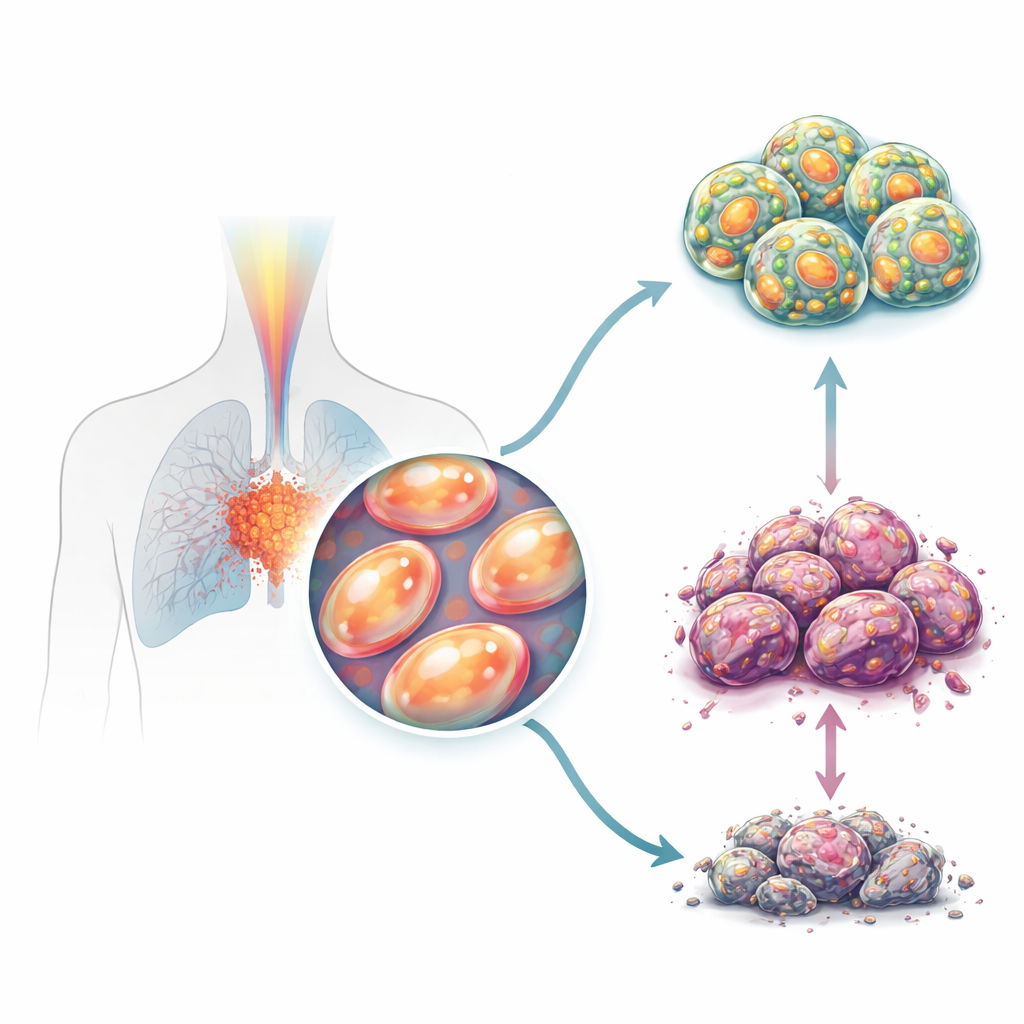
Jak komórki nowotworowe unikają uszkodzeń wywołanych promieniowaniem
Promieniowanie zabija komórki nowotworowe głównie przez wytwarzanie fal szkodliwych cząsteczek zwanych reaktywnymi formami tlenu oraz przez łamanie DNA. Te ataki są ściśle powiązane ze stacjami energetycznymi komórki — mitochondriami. Badacze zauważyli, że radiooporne komórki raka płuca nie tylko lepiej przetrzymują napromienianie, lecz także mają więcej mitochondrialnego DNA i wyższe poziomy kluczowego białka mitochondrialnego TFAM, które pomaga kopiować i chronić DNA mitochondriów. W porównaniu z pierwotnymi, nieodpornymi komórkami, komórki odporne wykazywały mniej uszkodzeń oksydacyjnych, mniej zaprogramowanej śmierci komórkowej i wyraźnie wyższe poziomy TFAM, co wskazuje na TFAM jako centralną tarczę pomagającą komórkom nowotworowym przetrwać leczenie.
Przełączniki w jądrze komórkowym wzmacniające tę tarczę
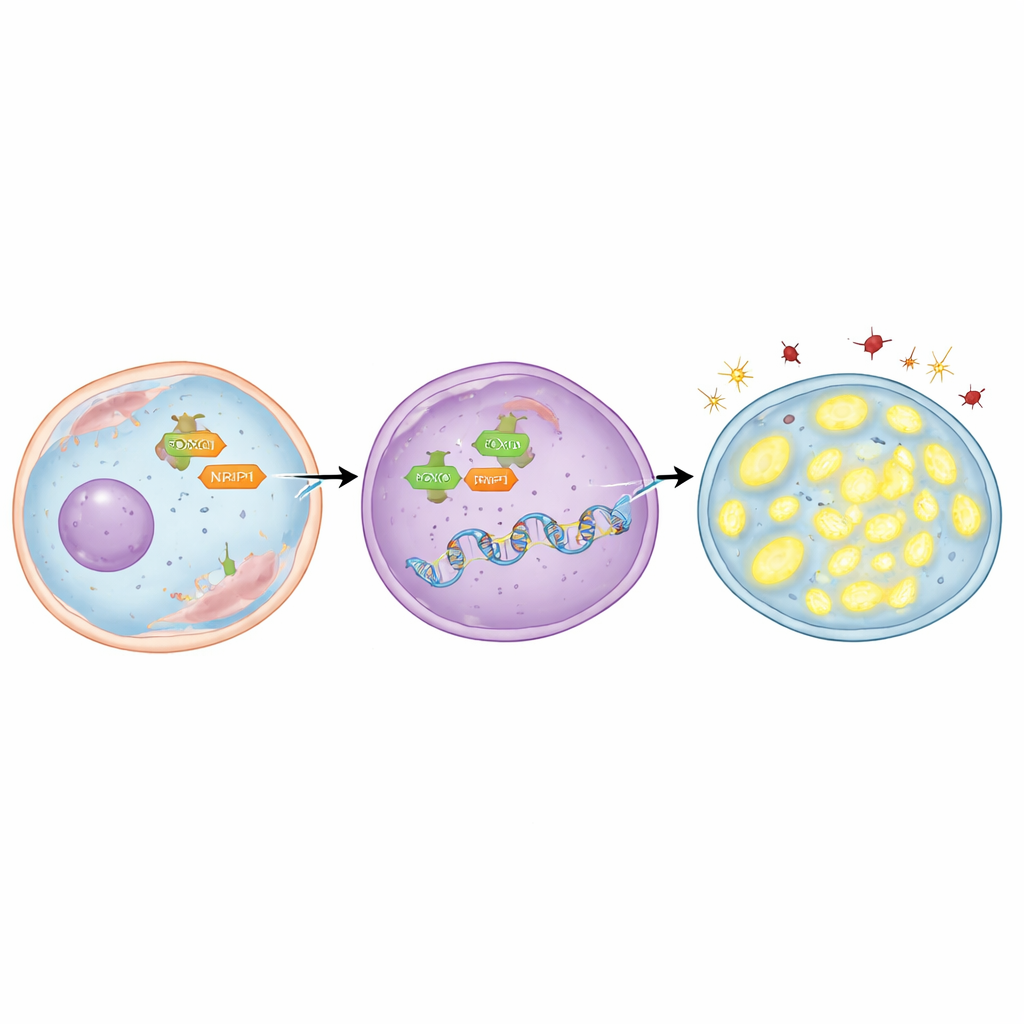
Aby ustalić, kto „włącza" TFAM, zespół skupił się na białku regulacyjnym FOXO3, które może przemieszczać się z cytoplazmy do jądra komórkowego, gdzie zapadają decyzje genetyczne. Odkryli, że gen TFAM zawiera kilka krótkich sekwencji DNA, do których FOXO3 może się przyłączać. Korzystając zarówno z modelowania komputerowego, jak i technik laboratoryjnych mapujących kontakty białko–DNA, pokazali, że FOXO3 bezpośrednio wiąże się z tymi regionami. W radioopornych komórkach raka płuca FOXO3 występował w większych ilościach i koncentrował się w jądrze. Gdy FOXO3 został eksperymentalnie ograniczony, poziomy TFAM spadały, narastały uszkodzenia cząsteczek, mitochondria traciły DNA, a po napromienianiu więcej komórek umierało. Odwrotnie, zastosowanie związku powodującego przemieszczanie FOXO3 do jądra zwiększało poziomy TFAM, chroniło mitochondria, zmniejszało uszkodzenia i utrudniało zabijanie komórek — chyba że jednocześnie blokowano sam TFAM.
Białko pomocnicze wzmacniające odpowiedź ochronną
Opowieść nie kończy się na FOXO3. Badacze zbadali także NRIP1, białko pomocnicze współdziałające z wieloma regulatorami genów w nowotworach. Stwierdzili, że NRIP1 fizycznie oddziałuje z FOXO3 i że to partnerstwo jest silniejsze w komórkach odpornych na promieniowanie. W jednej linii komórek raka płuca, która naturalnie nie miała funkcjonalnego NRIP1, poziomy TFAM były stosunkowo niskie; przywrócenie prawidłowego NRIP1 podniosło TFAM bez zmiany całkowitej ilości FOXO3. W komórkach radioopornych, które wyrażały NRIP1, jego wyciszenie obniżało poziomy TFAM, zwiększało stres oksydacyjny, zmniejszało ilość mitochondrialnego DNA i powodowało większą śmiertelność komórek po napromienianiu. Co istotne, NRIP1 nie zmieniał tego, ile FOXO3 docierało do jądra; działał jako współaktywator, poprawiając zdolność FOXO3 do włączania TFAM, gdy FOXO3 już znajdował się na miejscu.
Dowody z guzów w żywych organizmach
Aby sprawdzić, czy te molekularne zdarzenia mają znaczenie w całym organizmie, zespół wszczepił radiooporne komórki raka płuca do myszy, aby utworzyły guzy. Gdy FOXO3 został trwale zredukowany w tych komórkach przed wszczepieniem, powstałe guzy rosły wolniej. Dodanie radioterapii do redukcji FOXO3 jeszcze bardziej zmniejszyło guzy, nie szkodząc ogólnemu zdrowiu zwierząt. Te nowotwory pozbawione FOXO3 wykazywały więcej stresu oksydacyjnego, mniej mitochondrialnego DNA, silniejsze oznaki śmierci komórek i znacząco niższe poziomy TFAM. Razem wyniki te wspierają ideę, że ekspresja TFAM napędzana przez FOXO3, wzmacniana przez NRIP1, pomaga guzom utrzymać wydajne mitochondria i przeciwstawiać się promieniowaniu w żywym organizmie.
Co to oznacza dla przyszłego leczenia raka płuca
Dla osób niebędących specjalistami wnioskiem jest to, że niektóre raki płuca stają się odporne na promieniowanie, wzmacniając swoje wewnętrzne elektrownie. Trio graczy — FOXO3 przemieszczające się do jądra, NRIP1 wspomagający jego działanie oraz TFAM wzmacniający mitochondria — tworzy ochronny obwód, który pozwala komórkom guza naprawiać uszkodzenia i przetrwać. Blokowanie aktywności FOXO3, zakłócenie jego współpracy z NRIP1 lub bezpośrednie obniżenie TFAM może w przyszłości pozbawić guzy tej ukrytej zbroi. Takie strategie mogą uczynić standardową radioterapię bardziej skuteczną, potencjalnie pozwalając na stosowanie niższych dawek lub lepszą kontrolę guza przy mniejszej liczbie niepowodzeń leczenia.
Cytowanie: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Słowa kluczowe: niedrobnokomórkowy rak płuca, radiooporność, mitochondria, FOXO3, TFAM