Clear Sky Science · es
NRIP1 coactiva a FOXO3 translocado al núcleo para regular al alza la expresión de TFAM y promover la radioresistencia en el cáncer de pulmón no microcítico
Por qué importa mejorar la eficacia de los tratamientos contra el cáncer de pulmón
La radioterapia es uno de los pilares en el tratamiento del cáncer de pulmón no microcítico, el tipo más frecuente de cáncer pulmonar. Sin embargo, muchos tumores aprenden gradualmente a sobrevivir a la radiación, lo que permite que la enfermedad reaparezca o se disemine. Este estudio plantea una pregunta simple pero crucial: ¿qué ocurre dentro de las células cancerosas que permite a algunas de ellas resistir la radiación, y se pueden aprovechar esos mecanismos internos contra el tumor para hacer el tratamiento más eficaz?
Cómo las células cancerosas eluden el daño de la radiación
La radiación mata las células cancerosas principalmente generando oleadas de moléculas dañinas llamadas especies reactivas del oxígeno y rompiendo el ADN. Estos ataques están estrechamente ligados a las centrales energéticas de la célula, las mitocondrias. Los investigadores observaron que las células de cáncer de pulmón radioresistentes no solo sobreviven mejor tras la radiación, sino que además presentan más ADN mitocondrial y niveles más altos de una proteína mitocondrial clave llamada TFAM, que ayuda a copiar y proteger el ADN mitocondrial. Al comparar estas células resistentes con sus contrapartes no resistentes originales, mostraron menos daño oxidativo, menos muerte celular programada y niveles claramente superiores de TFAM, lo que apunta a TFAM como un escudo central que ayuda a las células cancerosas a soportar el tratamiento.
Interruptores en el núcleo celular que refuerzan este escudo
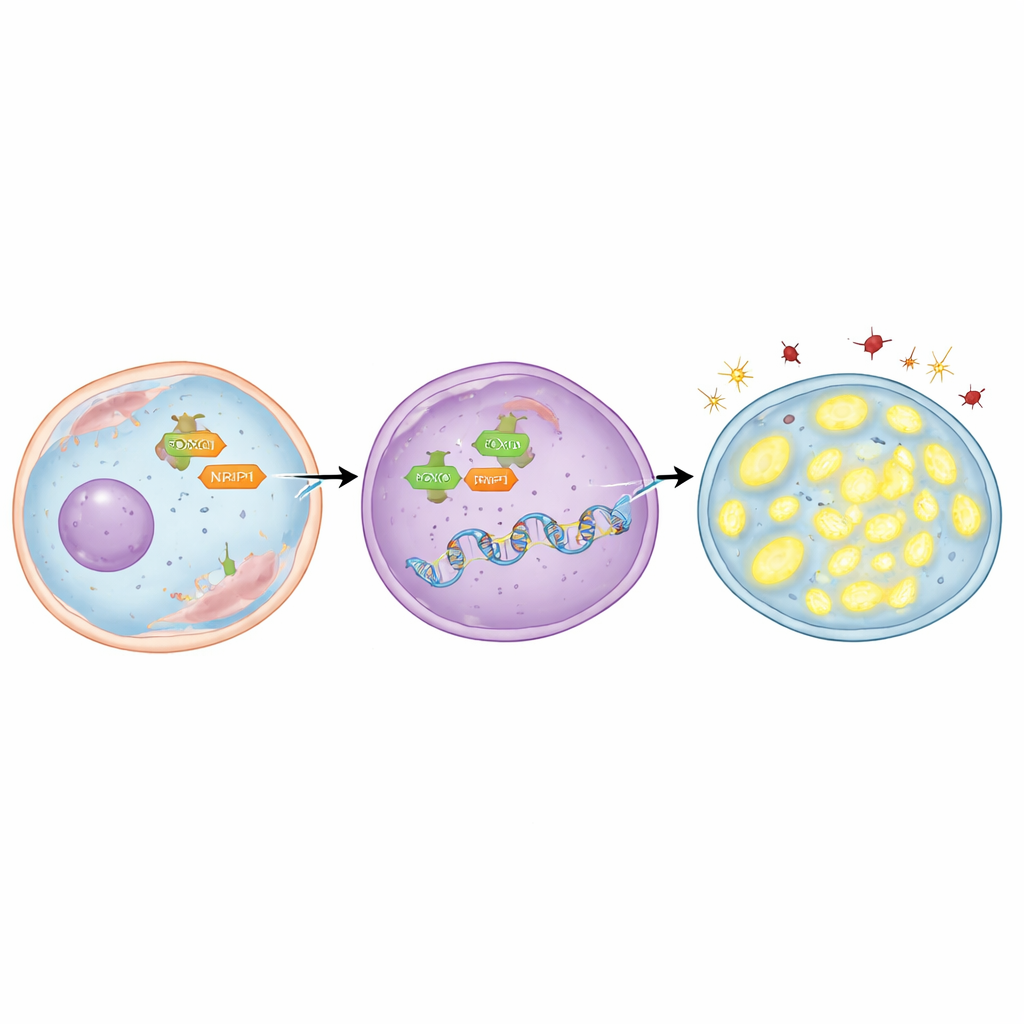
Para averiguar quién «enciende» a TFAM, el equipo se centró en una proteína reguladora llamada FOXO3, que puede trasladarse desde el citoplasma al núcleo celular, donde se toman las decisiones genéticas. Descubrieron que el gen TFAM contiene varias secuencias cortas de ADN a las que FOXO3 puede unirse. Usando tanto modelado por ordenador como técnicas de laboratorio que mapean los contactos proteína–ADN, demostraron que FOXO3 se une directamente a estas regiones. En las células de cáncer de pulmón radioresistentes, se encontró FOXO3 en cantidades mayores y concentrado en el núcleo. Cuando se redujo experimentalmente FOXO3, los niveles de TFAM cayeron, se acumularon moléculas dañadas, las mitocondrias perdieron ADN y más células cancerosas murieron tras la radiación. Por el contrario, usar un compuesto que promueve la entrada de FOXO3 en el núcleo aumentó TFAM, preservó las mitocondrias, disminuyó el daño y dificultó la eliminación de las células—salvo cuando TFAM fue bloqueado simultáneamente.
Una proteína auxiliar que potencia la respuesta protectora
La historia no termina con FOXO3. Los investigadores también examinaron NRIP1, una proteína auxiliar que colabora con muchos reguladores génicos en el cáncer. Encontraron que NRIP1 interactúa físicamente con FOXO3 y que esta asociación es más fuerte en células radioresistentes. En una línea celular de cáncer de pulmón que carecía de NRIP1 funcional de forma natural, los niveles de TFAM eran relativamente bajos; restaurar NRIP1 normal elevó TFAM sin cambiar la cantidad total de FOXO3. En células radioresistentes que sí expresaban NRIP1, reducir NRIP1 disminuyó TFAM, aumentó el estrés oxidativo, redujo el ADN mitocondrial y provocó más muerte celular tras la radiación. Es importante señalar que NRIP1 no cambió cuánto FOXO3 llegaba al núcleo; en su lugar actuó como coactivador, haciendo que FOXO3 fuera más eficaz para activar TFAM una vez situado en el lugar correcto.
Evidencia procedente de tumores en animales vivos
Para comprobar si estos eventos moleculares importan en un organismo completo, el equipo implantó células de cáncer de pulmón radioresistentes en ratones para formar tumores. Cuando FOXO3 se redujo de forma estable en estas células antes de la implantación, los tumores resultantes crecieron más despacio. Añadir radioterapia sobre la reducción de FOXO3 disminuyó aún más los tumores, sin perjudicar la salud general de los animales. Estos tumores deficientes en FOXO3 mostraron más estrés oxidativo, menos ADN mitocondrial, signos más claros de muerte celular y niveles sustancialmente menores de TFAM. En conjunto, estos hallazgos respaldan la idea de que la expresión de TFAM impulsada por FOXO3, potenciada por NRIP1, ayuda a los tumores a mantener mitocondrias robustas y a resistir la radiación en un sistema vivo.
Qué significa esto para el futuro tratamiento del cáncer de pulmón
Para el público general, la conclusión es que algunos cánceres de pulmón se vuelven resistentes a la radiación reforzando sus centrales celulares. Un trío de actores—FOXO3 que se traslada al núcleo, NRIP1 que le ayuda a funcionar y TFAM que refuerza las mitocondrias—forma un circuito protector que permite a las células tumorales reparar el daño y seguir adelante. Al bloquear la actividad de FOXO3, interrumpir su asociación con NRIP1 o reducir directamente TFAM, las terapias futuras podrían despojar a los tumores de esta armadura oculta. Tales estrategias podrían hacer que la radiación estándar sea más efectiva, permitiendo potencialmente dosis más bajas o un mejor control tumoral con menos fracasos terapéuticos.
Cita: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Palabras clave: cáncer de pulmón no microcítico, radioresistencia, mitocondrias, FOXO3, TFAM