Clear Sky Science · pt
NRIP1 co-ativa FOXO3 translocado ao núcleo para aumentar a expressão de TFAM e promover radioresistência no câncer de pulmão não pequenas células
Por que é importante melhorar a eficácia dos tratamentos contra o câncer de pulmão
A radioterapia é um pilar no tratamento do câncer de pulmão não pequenas células, o tipo mais comum de câncer de pulmão. No entanto, muitos tumores gradualmente aprendem a sobreviver à radiação, permitindo que a doença retorne ou se espalhe. Este estudo faz uma pergunta simples, porém crucial: o que acontece dentro das células cancerosas que permite que algumas delas resistam à radiação, e essas máquinas internas podem ser usadas contra o tumor para tornar o tratamento mais eficaz?
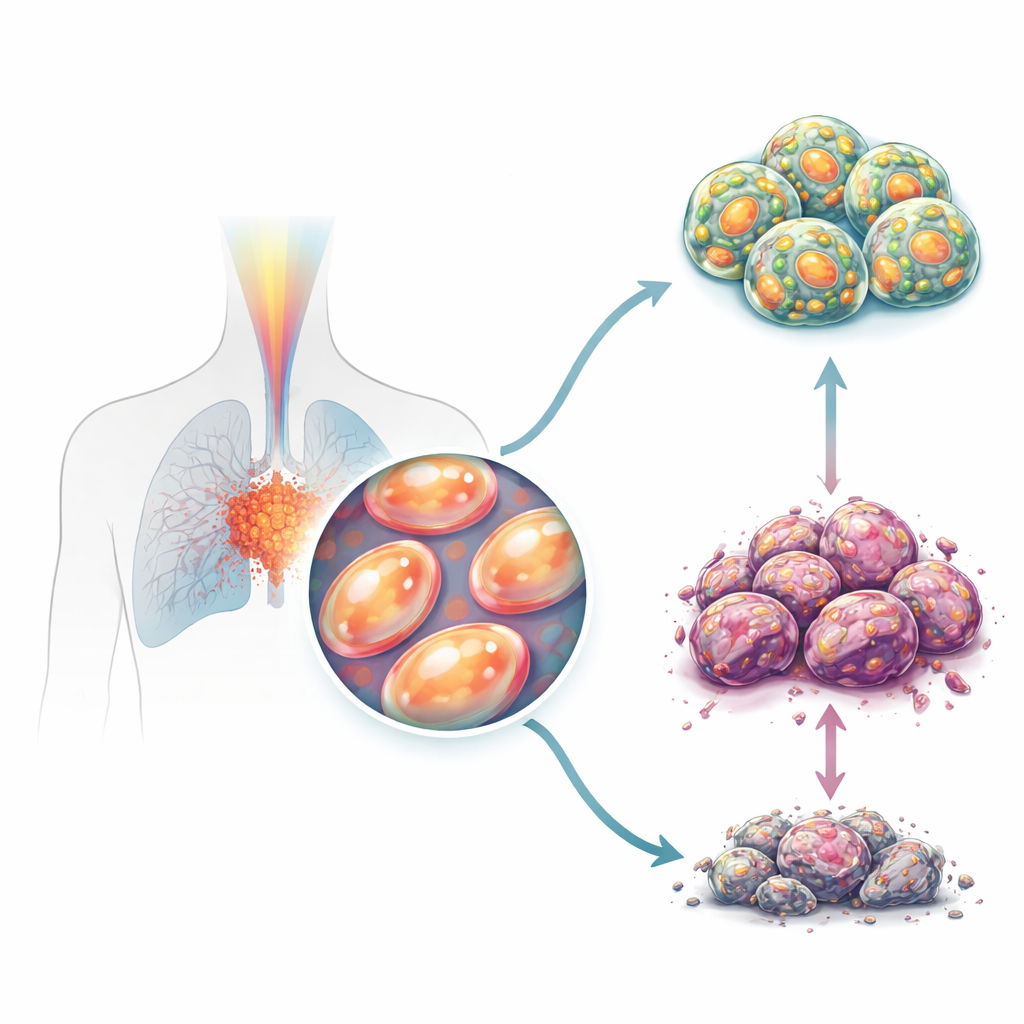
Como as células cancerosas evitam os danos causados pela radiação
A radiação mata células cancerosas em grande parte gerando explosões de moléculas nocivas chamadas espécies reativas de oxigênio e quebrando o DNA. Esses ataques estão intimamente ligados às estações de energia da célula, as mitocôndrias. Os pesquisadores observaram que células de câncer de pulmão radioresistentes não apenas sobrevivem melhor após a radiação, mas também têm mais DNA mitocondrial e níveis mais altos de uma proteína mitocondrial chave chamada TFAM, que ajuda a copiar e proteger o DNA mitocondrial. Quando essas células resistentes foram comparadas com suas contrapartes originais, não resistentes, mostraram menos dano oxidativo, menos morte celular programada e níveis claramente mais altos de TFAM, apontando TFAM como um escudo central que ajuda as células tumorais a resistir ao tratamento.
Interruptores no núcleo celular que fortalecem esse escudo
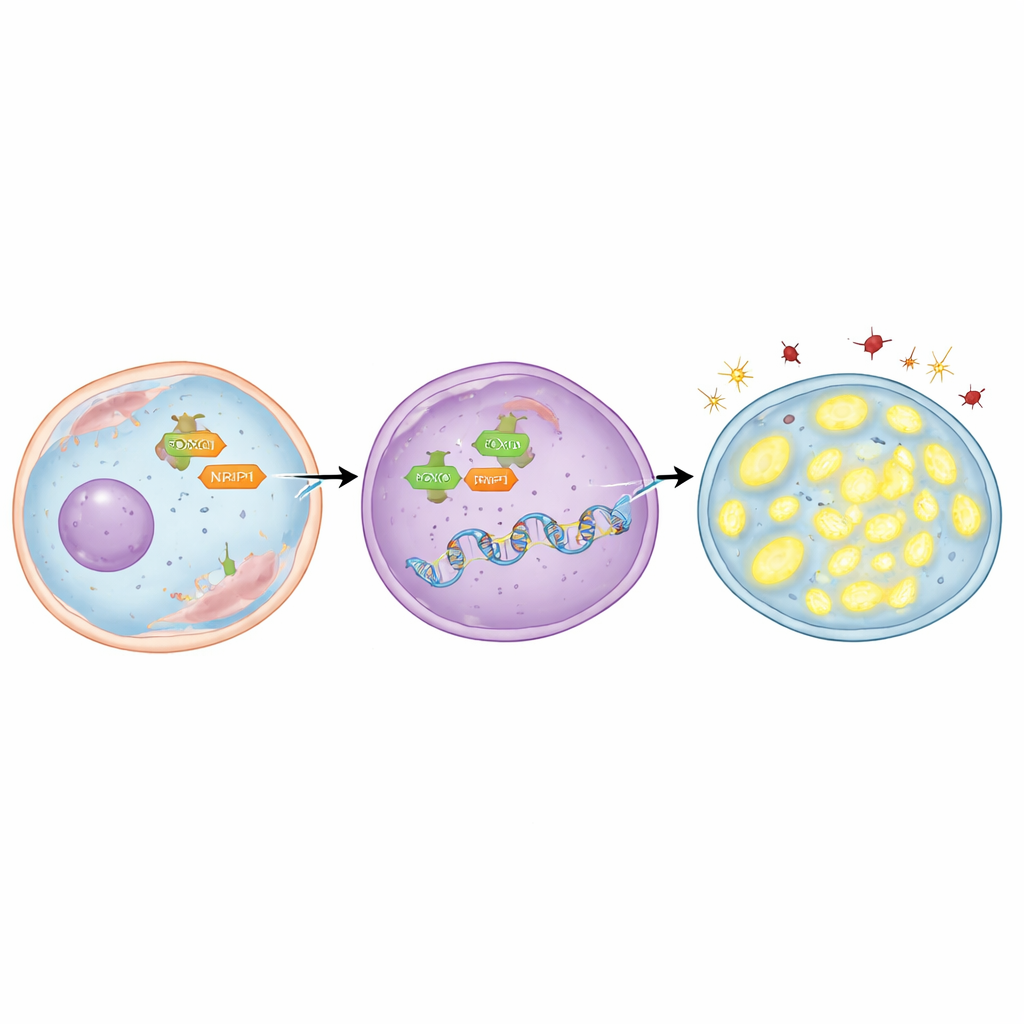
Para descobrir quem ativa o TFAM, a equipe se concentrou em uma proteína reguladora chamada FOXO3, que pode mover-se do citosol para o núcleo, onde são tomadas decisões genéticas. Eles descobriram que o gene TFAM contém várias sequências curtas de DNA às quais o FOXO3 pode se ligar. Usando tanto modelagem computacional quanto técnicas laboratoriais que mapeiam contatos proteína–DNA, mostraram que o FOXO3 se liga diretamente a essas regiões. Em células de câncer de pulmão radioresistentes, o FOXO3 foi encontrado em quantidades maiores e concentrado no núcleo. Quando o FOXO3 foi reduzido experimentalmente, os níveis de TFAM caíram, moléculas danificadas se acumularam, as mitocôndrias perderam DNA e mais células tumorais morreram após a radiação. Por outro lado, usar um composto que leva o FOXO3 para o núcleo aumentou o TFAM, preservou as mitocôndrias, diminuiu os danos e tornou as células mais difíceis de matar — a menos que o próprio TFAM fosse bloqueado simultaneamente.
Uma proteína auxiliar que amplifica a resposta protetora
A história não termina com o FOXO3. Os pesquisadores também examinaram NRIP1, uma proteína auxiliar que faz parceria com muitos reguladores gênicos no câncer. Eles descobriram que NRIP1 interage fisicamente com o FOXO3 e que essa parceria é mais forte em células radioresistentes. Em uma linhagem de câncer de pulmão que naturalmente não possuía NRIP1 funcional, os níveis de TFAM eram relativamente baixos; restaurar o NRIP1 normal aumentou o TFAM sem alterar a quantidade total de FOXO3. Em células radioresistentes que expressavam NRIP1, reduzir o NRIP1 diminuiu o TFAM, aumentou o estresse oxidativo, reduziu o DNA mitocondrial e levou mais células à morte após a radiação. Importante, NRIP1 não alterou quanto FOXO3 chegava ao núcleo; em vez disso, atuou como um coativador, tornando o FOXO3 mais eficaz em ativar o TFAM uma vez que já estivesse no lugar.
Evidência a partir de tumores em animais vivos
Para testar se esses eventos moleculares importam em um organismo inteiro, a equipe implantou células de câncer de pulmão radioresistentes em camundongos para formar tumores. Quando o FOXO3 foi reduzido de forma estável nessas células antes da implantação, os tumores resultantes cresceram mais lentamente. Adicionar radioterapia ao redor da redução de FOXO3 encolheu ainda mais os tumores, sem prejudicar a saúde geral dos animais. Esses tumores deficientes em FOXO3 apresentaram mais estresse oxidativo, menos DNA mitocondrial, sinais mais fortes de morte celular e níveis substancialmente mais baixos de TFAM. Em conjunto, esses achados sustentam a ideia de que a expressão de TFAM dirigida por FOXO3, potenciada por NRIP1, ajuda os tumores a manter mitocôndrias robustas e resistir à radiação em um sistema vivo.
O que isso significa para o futuro do tratamento do câncer de pulmão
Para não especialistas, a conclusão é que alguns cânceres de pulmão se tornam resistentes à radiação reforçando suas usinas celulares. Um trio de atores — FOXO3 movendo-se para o núcleo, NRIP1 ajudando seu funcionamento e TFAM fortalecendo as mitocôndrias — forma um circuito de proteção que permite às células tumorais reparar danos e continuar. Ao bloquear a atividade do FOXO3, interromper sua parceria com NRIP1 ou diminuir diretamente o TFAM, terapias futuras podem despojar os tumores dessa armadura oculta. Essas estratégias poderiam tornar a radioterapia padrão mais eficaz, potencialmente permitindo doses mais baixas ou melhor controle tumoral com menos falhas no tratamento.
Citação: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
Palavras-chave: câncer de pulmão não pequenas células, radioresistência, mitocôndrias, FOXO3, TFAM