Clear Sky Science · ar
NRIP1 ينشط FOXO3 المنقول نووياً لرفع تعبير TFAM وتعزيز المقاومة للإشعاع في سرطان الرئة غير صغير الخلايا
لماذا يهم تحسين فعالية علاجات سرطان الرئة
العلاج بالأشعة هو ركيزة أساسية في معالجة سرطان الرئة غير صغير الخلايا، وهو النوع الأكثر شيوعاً من سرطان الرئة. ومع ذلك، تتعلم العديد من الأورام تدريجياً النجاة من الإشعاع، مما يسمح للمرض بالعودة أو الانتشار. تطرح هذه الدراسة سؤالاً بسيطاً لكنه بالغ الأهمية: ما الذي يحدث داخل الخلايا السرطانية ما يسمح لبعضها بتجاهل الإشعاع، وهل يمكن استغلال هذه الآليات الداخلية ضد الورم لجعل العلاج أكثر فعالية؟
كيف تتفادى الخلايا السرطانية ضرر الإشعاع
يقتل الإشعاع الخلايا السرطانية في الأساس عن طريق توليد دفعات من الجزيئات الضارة المسماة أنواع الأكسجين التفاعلية وإلحاق شقوق في الحمض النووي. وترتبط هذه الهجمات ارتباطاً وثيقاً بمحطات طاقة الخلية، أي الميتوكوندريا. لاحظ الباحثون أن خلايا سرطان الرئة المقاومة للإشعاع لا تنجو بشكل أفضل بعد التعرض فحسب، بل تحتوي أيضاً على كمية أكبر من الحمض النووي الميتوكوندري ومستويات أعلى من بروتين ميتوكوندري رئيسي يُدعى TFAM، الذي يساعد في نسخ وحماية الحمض النووي الميتوكوندري. عندما قورنّت هذه الخلايا المقاومة بنظيراتها الأصلية غير المقاومة، أظهرت تلفاً أكسدة أقل، ومعدلات أقل من الموت المبرمج، ومستويات TFAM أعلى بوضوح، مما يشير إلى أن TFAM يشكل درعاً مركزياً يساعد الخلايا السرطانية على تحمل العلاج.
مفاتيح داخل نواة الخلية تقوّي هذا الدرع
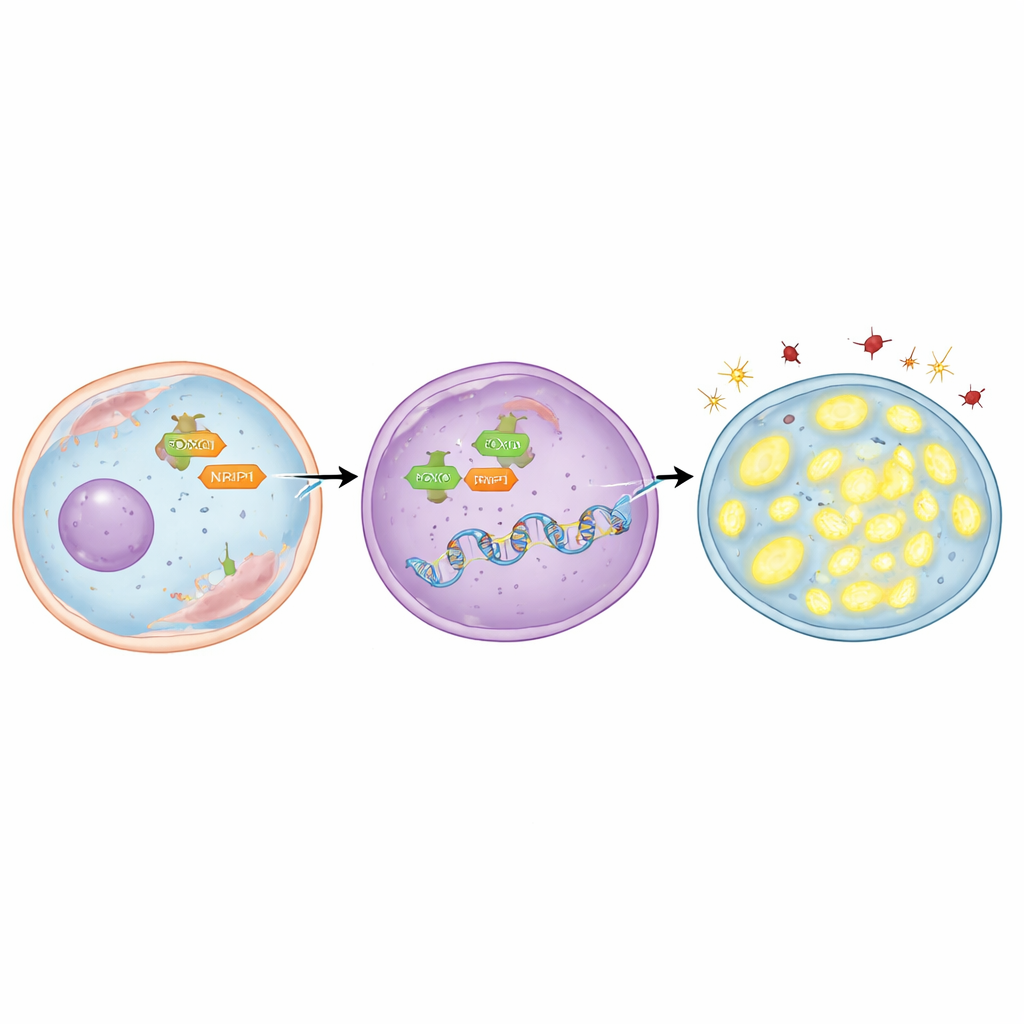
للكشف عمن "يُشغّل" TFAM، ركز الفريق على بروتين تنظيمي يُدعى FOXO3، الذي يمكنه الانتقال من السيتوبلازم إلى النواة حيث تُتخذ القرارات الجينية. اكتشفوا أن جين TFAM يحتوي على عدة مقاطع قصيرة من الحمض النووي يمكن لـ FOXO3 الارتباط بها. باستخدام النمذجة الحاسوبية وتقنيات مختبرية ترسم تَواصُلات البروتين–الحمض النووي، أظهروا أن FOXO3 يربط هذه المناطق بشكل مباشر. في خلايا سرطان الرئة المقاومة للإشعاع وُجدت كميات أعلى من FOXO3 وكان مركّزاً داخل النواة. عندما تم تقليل FOXO3 تجريبياً، انخفضت مستويات TFAM، وتراكمت الجزيئات المتضررة، وفقدت الميتوكوندريا حمضها النووي، وماتت مزيد من الخلايا بعد الإشعاع. وعلى العكس، فإن استخدام مركب يدفع FOXO3 إلى النواة زاد TFAM وحافظ على الميتوكوندريا وخفف الضرر وجعل الخلايا أصعب في القتل — إلا إذا تم حجب TFAM نفسه في الوقت ذاته.
بروتين مساعد يعزز الاستجابة الوقائية
القصة لا تتوقف عند FOXO3. فحص الباحثون أيضاً NRIP1، وهو بروتين مساعد يتعاون مع العديد من منظمات الجينات في السرطان. وجدوا أن NRIP1 يتفاعل جسدياً مع FOXO3 وأن هذه الشراكة أقوى في الخلايا المقاومة للإشعاع. في أحد خطوط خلايا سرطان الرئة التي كانت تفتقر طبيعياً إلى NRIP1 الوظيفي، كانت مستويات TFAM منخفضة نسبياً؛ وإعادة NRIP1 إلى وضعها الطبيعي رفعت TFAM دون تغيير الكمية الكلية لـ FOXO3. في الخلايا المقاومة التي كانت تعبر عن NRIP1، أدى خفض NRIP1 إلى تقليل TFAM، وزيادة الإجهاد التأكسدي، وانخفاض الحمض النووي الميتوكوندري، ودفع المزيد من الخلايا نحو الموت بعد الإشعاع. ومن المهم أن NRIP1 لم يغير مقدار FOXO3 الذي يصل إلى النواة؛ بل عمل كمساهم-مُنشّط، مما جعل FOXO3 أفضل في تشغيل TFAM بمجرد تواجده في موضعه.
دليل من أورام في حيوانات حية
لاختبار ما إذا كانت هذه الأحداث الجزيئية مهمة في كائن حي كامل، زرع الفريق خلايا سرطان رئة مقاومة للإشعاع في فئران لتكوين أورام. عندما تم تقليل FOXO3 بشكل ثابت في هذه الخلايا قبل الزرع، نمت الأورام الناتجة ببطء أكبر. وأدى إضافة العلاج بالإشعاع إلى خفض حجم الأورام بشكل أكبر، دون الإضرار بالصحة العامة للحيوانات. أظهرت هذه الأورام الناقصة FOXO3 مزيداً من الإجهاد التأكسدي، وكمية أقل من الحمض النووي الميتوكوندري، وعلامات أقوى للموت الخلوي، ومستويات TFAM أقل بكثير. تدعم هذه النتائج معاً فكرة أن تعبير TFAM الذي يقوده FOXO3، والمعزز بواسطة NRIP1، يساعد الأورام على الحفاظ على ميتوكوندريا قوية ومقاومة للإشعاع في نظام حي.
ما يعنيه هذا لعلاج سرطان الرئة في المستقبل
بالنسبة لغير المتخصصين، الخلاصة هي أن بعض سرطانات الرئة تصبح أكثر صلابة أمام الإشعاع عن طريق تقوية محطات طاقتها الخلوية. يشكل ثلاثي العوامل — انتقال FOXO3 إلى النواة، ومساعدة NRIP1 له على العمل، وTFAM الذي يقوّي الميتوكوندريا — دائرة وقائية تتيح لخلايا الورم إصلاح الضرر والمضي قدماً. من خلال حجب نشاط FOXO3، أو تعطيل شراكته مع NRIP1، أو خفض TFAM مباشرة، قد تتمكن العلاجات المستقبلية من تجريد الأورام من هذه الدرع الخفي. يمكن أن تجعل مثل هذه الاستراتيجيات الإشعاع القياسي أكثر فعالية، مما قد يسمح بجرعات أقل أو بتحكم أفضل في الورم مع فشل علاجي أقل.
الاستشهاد: Zha, Y., Huang, H., Liu, Y. et al. NRIP1 co-activates nuclear translocated FOXO3 to upregulate TFAM expression and promote radioresistance in non-small cell lung cancer. Cell Death Discov. 12, 196 (2026). https://doi.org/10.1038/s41420-026-03028-8
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, المقاومة للإشعاع, الميتوكوندريا, FOXO3, TFAM