Clear Sky Science · zh
BACH2将β1-肾上腺素能受体/β-arrestin1信号连接到MIAT以抑制心脏成纤维细胞激活和心肌细胞凋亡
这项心脏研究为何重要
心肌梗死和慢性心力衰竭仍然是主要死亡原因之一,部分原因在于受损的心肌被瘢痕组织取代,重要的心脏细胞也会死亡。本研究发现了心脏细胞内一个此前未知的安全开关:它可被一种常用的β受体阻滞剂激活,并进而抑制与纤维化和细胞死亡相关的有害RNA信号。理解这一内在保护通路,或能为更精准的治疗指明方向,从而延长并改善受损心脏的功能。
衰竭心脏中的有害信息
当心脏某部分缺血时,大量收缩性心肌细胞(心肌细胞)死亡,并被称为成纤维细胞的支持细胞产生的僵硬瘢痕取代。早期研究鉴定出一种名为MIAT的长链非编码RNA,其像有毒信息一样:它促进有利于瘢痕形成和程序性细胞死亡的基因表达。MIAT在多种人类心脏疾病和多种动物心脏损伤模型中升高,而在小鼠中阻断MIAT可改善心肌梗死后的心脏功能。然而直到现在,科学家尚不清楚是什么调控MIAT本身,以及常用心脏药物如何影响它。
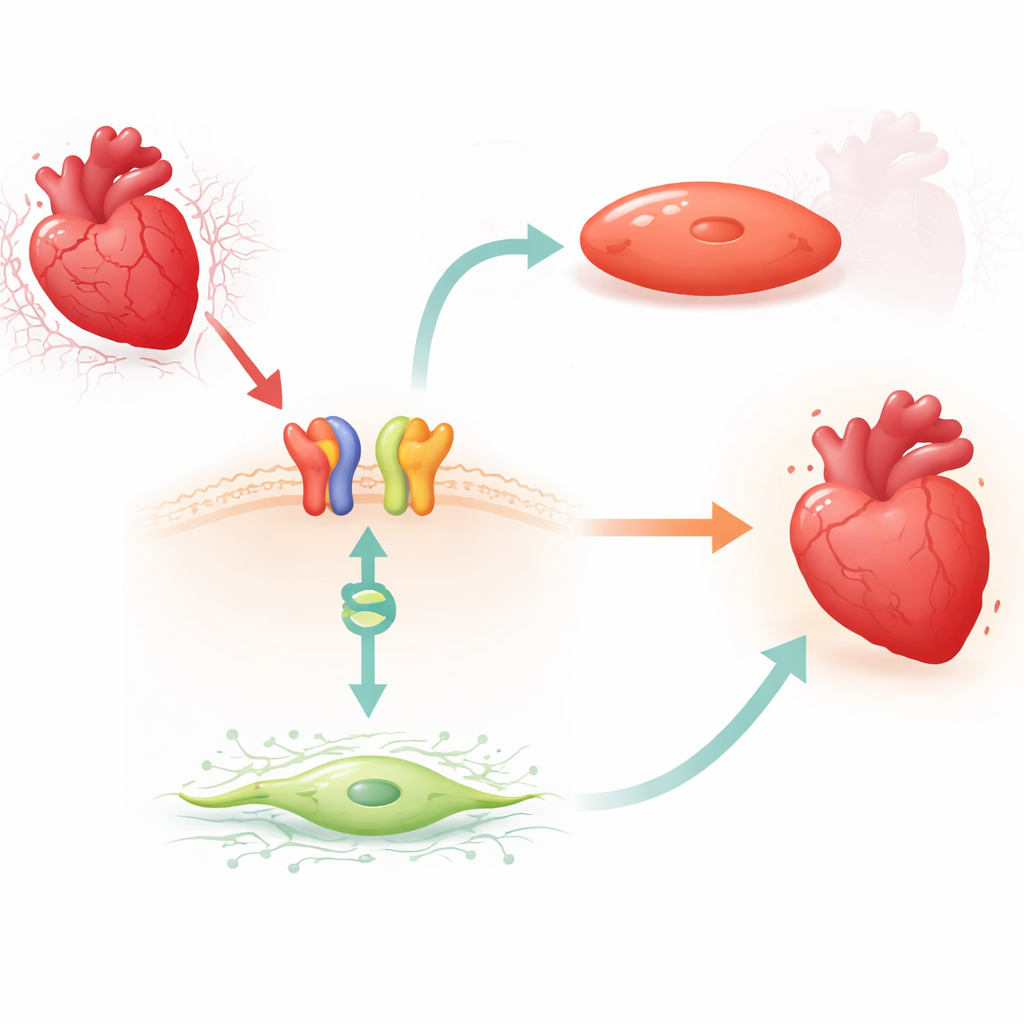
从表面信号到基因开关的药物激活联结
研究人员聚焦于卡维地洛(carvedilol),一种广泛使用的β受体阻滞剂,可通过β1-肾上腺素受体和一种名为β-arrestin1的适配蛋白触发保护性信号通路。在小鼠中,他们发现短期卡维地洛处理持续降低左心室中的MIAT水平,但这一效应仅在β1受体和β-arrestin1存在时出现。成人人人心脏成纤维细胞以及暴露于体外低氧再氧模型的人和啮齿类心肌细胞中也出现了类似的MIAT降低。在这些系统中,应激会上调MIAT,而卡维地洛能逆转这种上升,表明该药物利用了对这一有害RNA的天然制动机制。
抑制有害RNA的守护蛋白
进一步研究中,团队在细胞核内寻找能够与β-arrestin1配对的DNA结合蛋白。他们锁定了转录因子BACH2,此前曾与对其他形式心脏损伤的保护相关,但在该背景下尚未被研究。通过生化结合实验,他们证明BACH2能够结合MIAT启动子中的保守序列——即驱动MIAT产生的调控区。在人心脏成纤维细胞和心肌细胞中,增加BACH2可降低MIAT水平,而沉默BACH2则提高MIAT。重要的是,来自晚期心力衰竭患者的心脏以及心肌梗死后的小鼠心脏显示出相同模式:当MIAT高表达时,BACH2水平较低。小鼠中卡维地洛处理以β1和β-arrestin1依赖的方式提高了BACH2表达,将表面药物信号与这一核内基因开关联系起来。
保护心脏细胞免受纤维化和死亡
接着,团队探究BACH2对心脏支持细胞和肌肉细胞的实际作用。在培养的人心脏成纤维细胞中,丧失BACH2会增强纤维化标志物、促进细胞增殖并增强细胞迁移——这些行为有利于瘢痕堆积,而额外表达BACH2则抑制这些纤维化特征。在人和小鼠心肌细胞中,下调BACH2导致更多细胞死亡和凋亡相关酶活性增加,同时天然的存活蛋白水平下降。过表达BACH2则产生相反效果,在应激下保护细胞存活。总体上,这些实验支持这样一个模型:卡维地洛激活β1受体和β-arrestin1,二者在细胞核中与BACH2协同作用以抑制MIAT,从而限制纤维化和细胞损失。
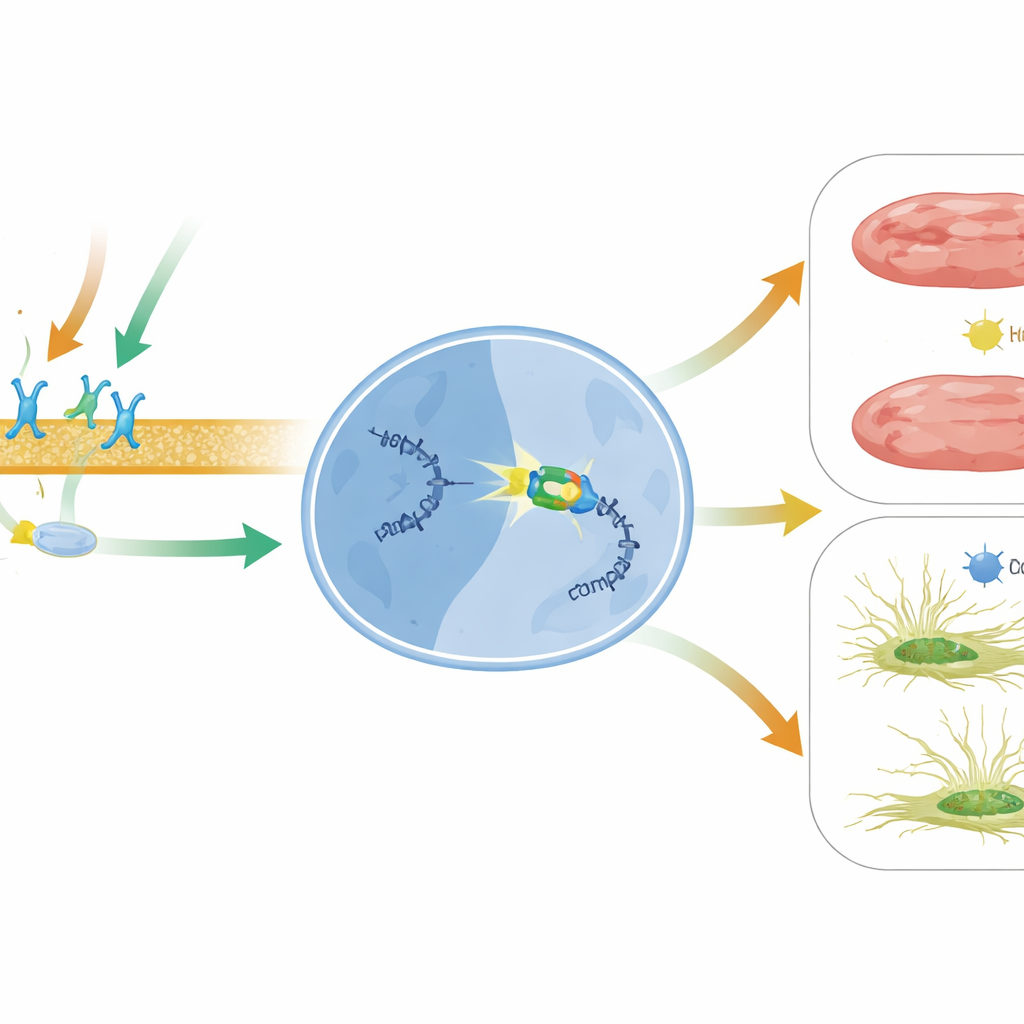
这对未来心脏治疗意味着什么
简而言之,这项工作揭示了衰竭心脏内一个新的保护轴:药物触发的β1受体与β-arrestin1信号开启BACH2,BACH2随后关闭推动瘢痕形成和细胞死亡的有害MIAT信息。鉴于MIAT在多种人类心脏疾病中升高,甚至可以作为循环中的潜在心脏损伤标志物,靶向BACH2–MIAT通路可能成为对当前疗法的有益补充。增强BACH2活性、用像卡维地洛这类药物精细调节β-arrestin1偏倚信号,或直接用RNA为基础的工具沉默MIAT,未来或有助于防止受损心脏僵硬和衰竭。
引用: Moukette, B., Teoh, Jp., Hashmi, W.J. et al. BACH2 links β1-adrenergic receptor/β-arrestin1 signaling to MIAT to inhibit cardiac fibroblast activation and cardiomyocyte apoptosis. Cell Death Discov. 12, 127 (2026). https://doi.org/10.1038/s41420-026-02985-4
关键词: 心力衰竭, 心脏纤维化, 长链非编码RNA, β受体阻滞剂治疗, 心肌细胞凋亡