Clear Sky Science · he
BACH2 מקשר בין איתות קולטני β1‑אדרנרגיים/β‑arrestin1 ל‑MIAT לעיכוב הפעלת פיברובלסטים לבביים ומתאופטוזה של קרדיומיוציטים
מדוע המחקר הלבבי הזה חשוב
תקיעות לב וכשל לב כרוני נשארים סיבות עיקריות לתמותה, חלקית משום ששריר לב שנפגע מוחלף ברקמת צלקת ותאי לב חיוניים מתים. מחקר זה חושף מתג בטיחות פנימי בתאי הלב שמופעל על‑ידי תרופה חוסמת בטא נפוצה, ובתגובה כבה אות RNA מזיק המקושר לצלקת ולמוות תאי. הבנת המסלול המולד הזה עשויה להצביע על דרכים מדויקות יותר לטיפול שישמרו על פעילות הלב הפגוע זמן רב וטוב יותר.
מסר מזיק בלב לכוד
כאשר חלק מהלב נותר ללא אספקת דם, תאים רבים של שריר המאמץ (קרדיומיוציטים) מתים ומוחלפים בצלקת קשיחה שמיוצרת על‑ידי תאי תמיכה הנקראים פיברובלסטים. מחקרים קודמים זיהו RNA לא מקודד ארוך בשם MIAT הפועל כמעט כמידע רעיל: הוא מחזק גנים המקדמים צלקת ומוות מתוכנת של תאים. רמות MIAT עולות במגוון מחלות לב בבני אדם ובמודלים בעלי חיים של פגיעה לבבית, וחסימה של MIAT בעכברים משפרת תפקוד לב אחרי התקף. עם זאת, עד כה לא היה ידוע מה שולט ב‑MIAT בעצמו או כיצד תרופות לב סטנדרטיות עשויות להשפיע עליו.
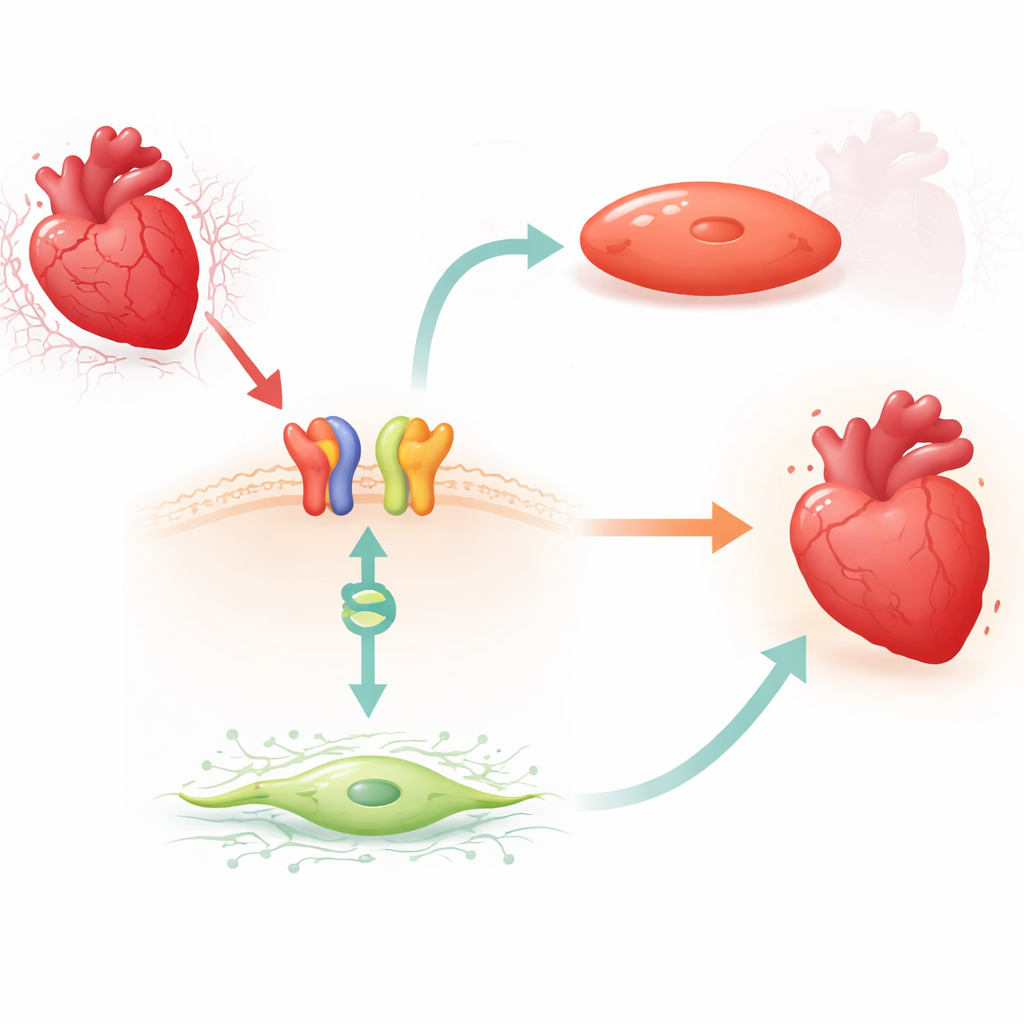
קשר שמופעל על‑ידי תרופה מאותת משטח אל מתג גנים
החוקרים התרכזו ב‑carvedilol, חוסם בטא נפוץ שמסוגל להפעיל מסלול הגנתי דרך קולטני β1‑אדרנרגיים וחלבון מתווך בשם β‑arrestin1. בעכברים הם גילו שטיפול קצר ב‑carvedilol הוריד בעקביות את רמות MIAT בחדר שמאל, אך רק כאשר נוכחו קולטני β1 ו‑β‑arrestin1. ירידות דומות ב‑MIAT נצפו בפיברובלסטים לבביים בוגרים של בני אדם ובתאי שריר לב של אדם וחיה שנחשפו למודל מעבדה של היפוקסיה ושלחזור חמצן. בכל המערכות הללו, לחץ העלה את MIAT, בעוד carvedilol הפך עלייה זו, מה שמרמז שהתרופה מנצלת בלם טבעי על ה‑RNA המזיק.
חלבון המגן השותק את ה‑RNA המזיק
בהמשך, הצוות חיפש חלבון קשור‑DNA שיכול לשתף פעולה עם β‑arrestin1 בגרעין התא. הם התמקדו ב‑BACH2, גורם שעתוק שנקשר בעבר להגנה מפגיעות לב אחרות אך לא נחקר בהקשר זה. באמצעות בדיקות קשירה ביוכימיות הראו כי BACH2 נקשר לחלופות שימור בקידום (promoter) של MIAT, אזור הבקרה המפעיל את ייצור ה‑MIAT. בפיברובלסטים לבביים אנושיים ובקרדיומיוציטים, הגברה של BACH2 הפחיתה רמות MIAT, בעוד השתקת BACH2 העלתה את MIAT. חשוב מכך, לבבות של חולים עם אי‑ספיקת לב מתקדמת ובעכברים אחרי התקף לב הראו את אותו דפוס: רמות BACH2 היו נמוכות כאשר MIAT היה גבוה. טיפול ב‑carvedilol בעכברים העלה את ביטוי BACH2 באופן התלוי ב‑β1 וב‑β‑arrestin1, וקישר את האות המופעל מהמשטח למתג הגנטי בגרעין.
הגנה על תאי הלב מפני צלקת ומוות
הצוות בחן מה BACH2 עושה בפועל לתאי תמיכה ושריר לב. בתרבית פיברובלסטים לבביים אנושיים, אובדן BACH2 הגביר סמנים של פיברוזיס, הגדיל את גדילת התאים והגביר נדידת תאים—התנהגויות המקדמות הצטברות צלקת—בעוד BACH2 עודף דכא תכונות פיברוטיות אלו. בקרדיומיוציטים של אדם ועכבר, הורדת BACH2 הובילה ליותר תאים מתים ולפעילות גבוהה יותר של אנזימים מקושרי מוות, לצד רמות נמוכות יותר של חלבוני הישרדות טבעיים. הבעה מופרזת של BACH2 הניבה את ההשפעות ההפוכות ושמרה על הישרדות התאים תחת לחץ. ניסויים אלה תומכים במודל שבו carvedilol מפעיל קולטני β1 ו‑β‑arrestin1, ששם משתפים פעולה עם BACH2 בגרעין כדי לכבות את MIAT, וכך מצמצמים צלקת ואובדן תאים.
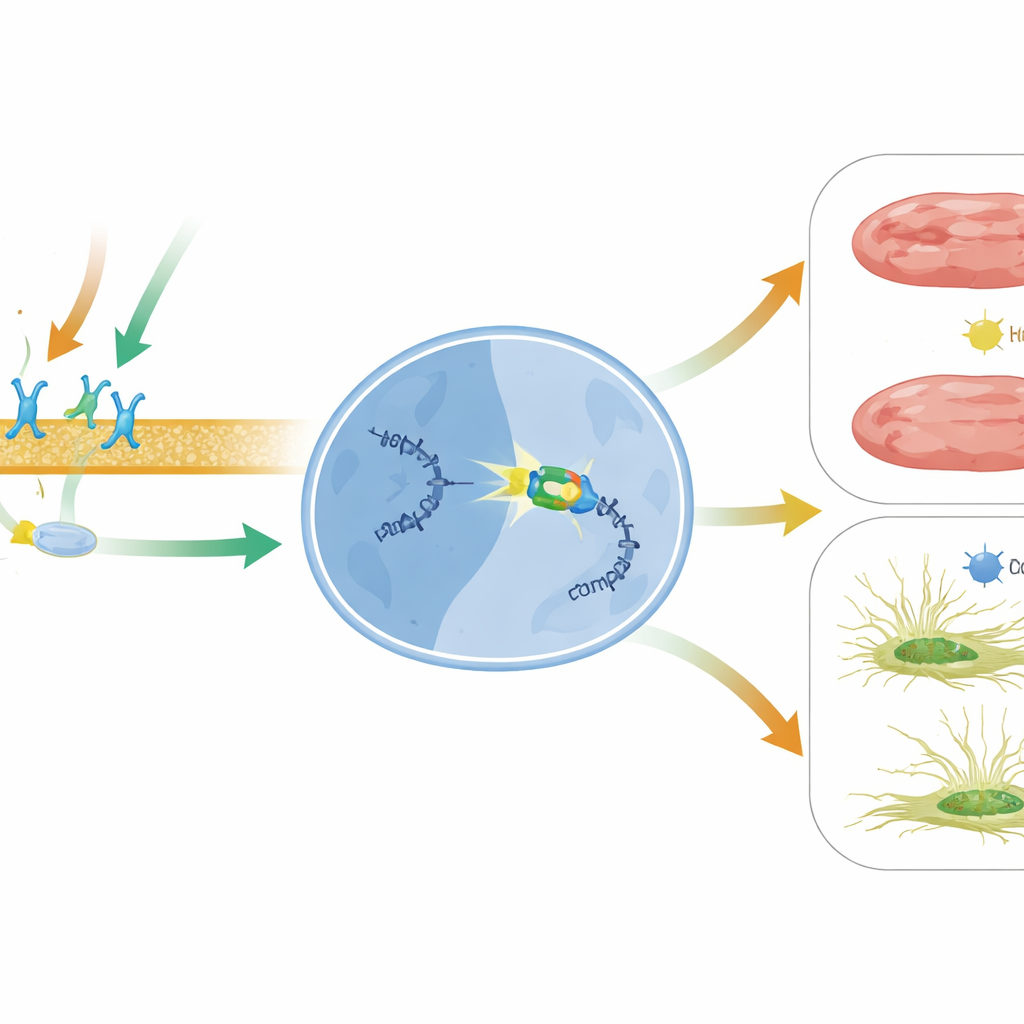
מה משמעות הדבר לטיפולים לבביים בעתיד
במילים פשוטות, עבודה זו חושפת ציר מגן חדש בלב הנכשל: אות מ‑β1 ו‑β‑arrestin1 שמופעל על‑ידי תרופה מדליק את BACH2, שמכבה את מסר ה‑MIAT המזיק המקדם יצירת צלקת ומוות תאי. מאחר ש‑MIAT מוגבר במחלות לב שונות בבני אדם ואף מופיע במחזור הדם כסמן פוטנציאלי לנזק לבבי, ייתכן כי ייעוד מסלול BACH2–MIAT ישלים טיפולים קיימים. אסטרטגיות להגברת פעילות BACH2, כיוונון איתות מוטה‑β‑arrestin1 עם תרופות כגון carvedilol, או השתקה ישירה של MIAT בעזרת כלים מבוססי RNA עשויים בעתיד לסייע במניעת התקשות וכשל של לב פגוע.
ציטוט: Moukette, B., Teoh, Jp., Hashmi, W.J. et al. BACH2 links β1-adrenergic receptor/β-arrestin1 signaling to MIAT to inhibit cardiac fibroblast activation and cardiomyocyte apoptosis. Cell Death Discov. 12, 127 (2026). https://doi.org/10.1038/s41420-026-02985-4
מילות מפתח: אי־ספיקת לב, צלקת לבבית, RNA לא מקודד ארוך, תרופות חוסמי בטא, אפופטוזיס של קרדיומיוציטים