Clear Sky Science · ar
BACH2 يربط إشارات مستقبل β1-الأدرينيرجي/β-arrestin1 بـ MIAT لكبح تنشيط الأرومات الليفية القلبية وموت الخلايا القلبية المبرمج
لماذا تهم هذه الدراسة القلبية
لا تزال النوبات القلبية وفشل القلب المزمن من الأسباب الرئيسية للوفاة، جزئياً لأن أنسجة القلب المصابة تُستبدل بأنسجة ندبية وتُفقد خلايا قلبية حيوية. تكشف هذه الدراسة عن مفتاح أمان داخلي غير معروف سابقاً داخل خلايا القلب يُفَعَّل بواسطة دواء شائع من مضادات بيتا، ويوقِف بدوره إشارة RNA ضارة مرتبطة بالتندب وموت الخلايا. قد يوجّه فهم هذا المسار الوقائي المدمج نحو علاجات أكثر دقة تحافظ على عمل القلوب التالفة لفترة أطول وبكفاءة أكبر.
رسالة ضارة في القلوب الفاشلة
عندما يُحرم جزء من القلب من الدم، تموت العديد من خلايا العضلة العاملة (المُحَرّكات القلبية) وتُستبدل بنسيج ندبي صلب تصنعه خلايا داعمة تُسمى الأرومات الليفية. كشفت أبحاث سابقة عن RNA طويل غير مشفر يُدعى MIAT يعمل كرسالة سامة: يعزّز جينات تشجّع التندب والموت الخلوي المبرمج. ترتفع مستويات MIAT في عدة أمراض قلبية بشرية وفي نماذج حيوانية متعددة لإصابة القلب، بينما يؤدي حجب MIAT في الفئران إلى تحسن وظيفة القلب بعد النوبة القلبية. ومع ذلك، لم يعرف العلماء حتى الآن ما الذي يتحكم في MIAT بنفسه أو كيف يمكن للأدوية القلبية القياسية أن تؤثر عليه.
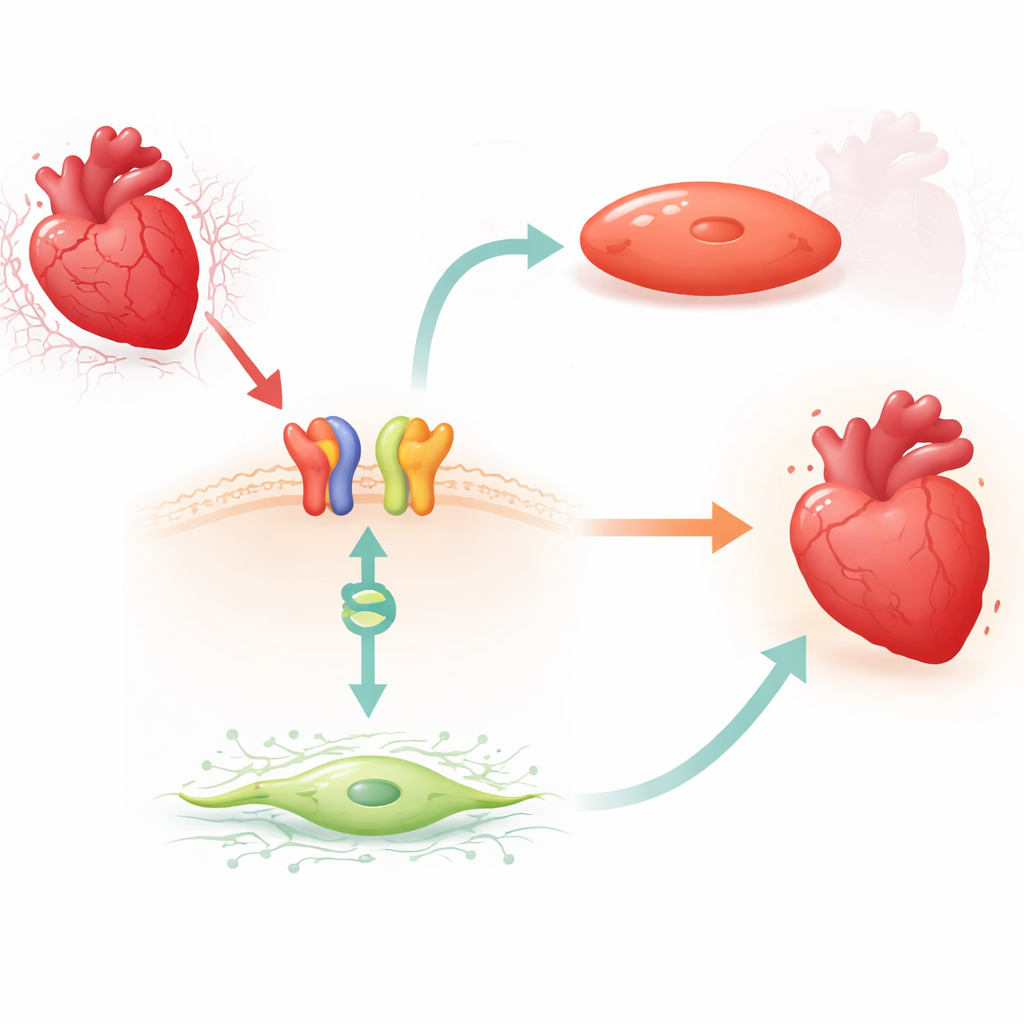
حلقة دوائية مفعلة من الإشارة السطحية إلى مفتاح الجين
ركز الباحثون على الكارفيديلول، وهو مضاد بيتا واسع الاستخدام يمكن أن يُحفّز مسار إشاري وقائي عبر مستقبل β1-الأدرينيرجي وبروتين موصل يُسمى β-arrestin1. في الفئران، وجدوا أن علاجاً قصيراً بالكارفيديلول خفض باستمرار مستويات MIAT في البطين الأيسر، لكن فقط عندما كانت مستقبلات β1 وβ-arrestin1 موجودة. حدثت تقلُّصات مماثلة في MIAT في الأرومات الليفية القلبية البشرية البالغة وفي خلايا عضلة القلب البشرية والقوارض المعرَّضة لنموذج مختبري لانخفاض الأكسجين ثم إعادة الأكسجة. عبر هذه الأنظمة، زاد الإجهاد من MIAT بينما عكس الكارفيديلول هذا الارتفاع، مما يشير إلى أن الدواء يستغل فرملة طبيعية على هذا الـ RNA الضار.
البروتين الحارس الذي يسكّن الـ RNA الضار
بالتعمق أكثر، بحث الفريق عن بروتين رابط للحمض النووي يمكن أن يتعاون مع β-arrestin1 في نواة الخلية. ركزوا على BACH2، عامل نسخ رُبط سابقاً بالحماية ضد أشكال أخرى من إصابة القلب لكنه لم يدرس في هذا السياق. باستخدام اختبارات الترابط الكيميائية الحيوية، أظهروا أن BACH2 يرتبط بمقاطع محفوظة في محفز MIAT، المنطقة الضابطة التي تقود إنتاج MIAT. في أرومات ليفية قلبية بشرية وقلبيات، أدى تعزيز BACH2 إلى خفض مستويات MIAT، بينما رفع تعطيل BACH2 مستويات MIAT. والأهم من ذلك، أظهرت قلوب المرضى المصابين بفشل قلبي متقدّم وقلوب الفئران بعد النوبة القلبية نفس النمط: مستويات BACH2 كانت منخفضة عندما كان MIAT عالياً. رفع علاج الكارفيديلول لتعبير BACH2 في الفئران كان معتمداً على β1 وβ-arrestin1، رابطاً إشارة الدواء السطحية بهذا المفتاح الجيني النووي.
حماية خلايا القلب من التندب والموت
سأل الفريق بعد ذلك ماذا يفعل BACH2 فعلياً لخلايا الدعم والعضلة القلبية. في أرومات ليفية قلبية بشرية مزروعة، أدى فقدان BACH2 إلى زيادة مؤشرات التليف، وزيادة نمو الخلايا، وتعزيز هجرة الخلايا—سلوكيات تُفضّل تراكم الندب—بينما قلّل وجود BACH2 الزائد هذه السمات الليفية. في القلبيات البشرية والفأرية، أدى خفض BACH2 إلى ازدياد الخلايا الميتة وارتفاع نشاط إنزيمات مرتبطة بالموت، إلى جانب انخفاض مستويات بروتينات البقاء الطبيعية. على النقيض، كان لزيادة تعبير BACH2 آثار معاكسة، محافظة على بقاء الخلايا تحت الإجهاد. تدعم هذه التجارب نموذجاً تفصيلياً مفاده أن الكارفيديلول ينشّط مستقبلات β1 وβ-arrestin1، التي تتعاون بعد ذلك مع BACH2 في النواة لإخماد MIAT ومن ثم الحد من التندب وفقدان الخلايا.
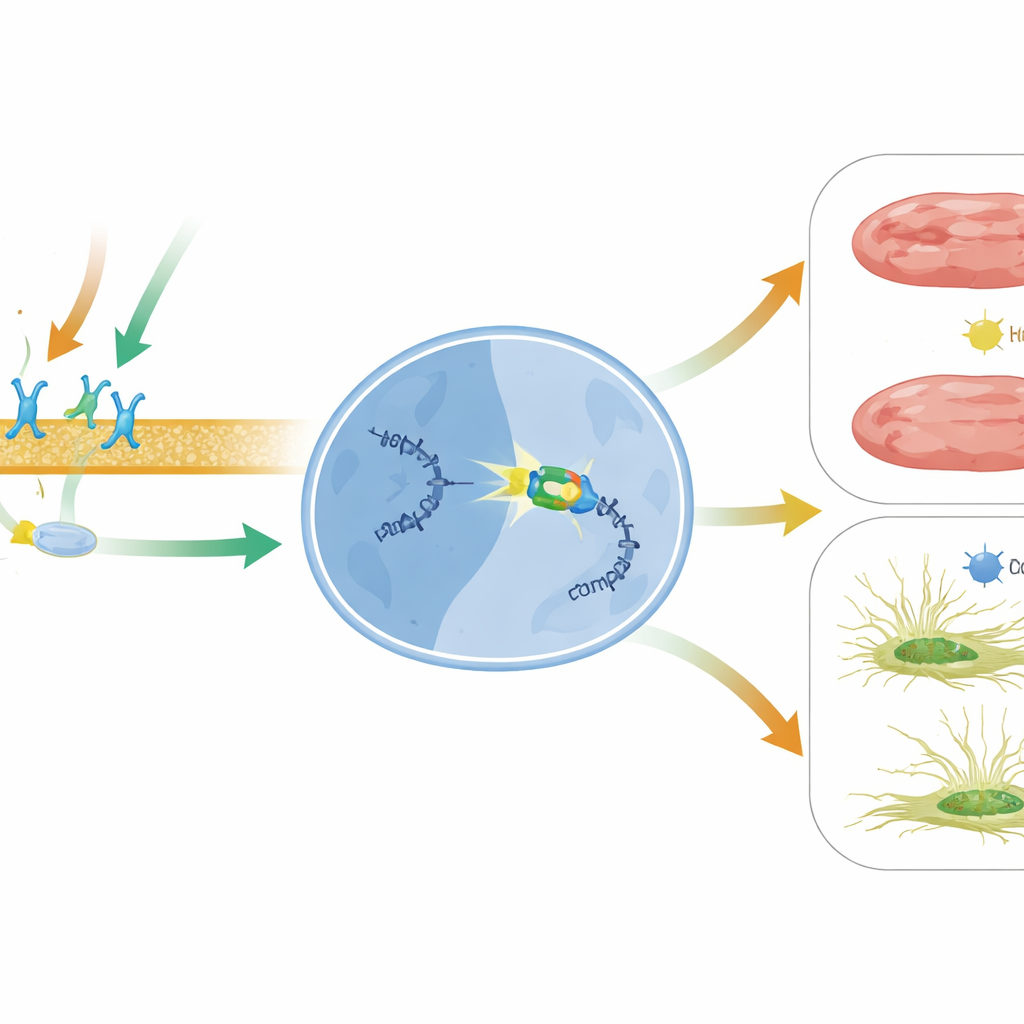
ماذا قد يعني هذا لعلاجات القلب المستقبلية
بعبارات بسيطة، تكشف هذه الدراسة عن محور وقائي جديد داخل القلب الفاشل: إشارة مستقبل β1 المحفزة دوائياً وβ-arrestin1 تشغّل BACH2، الذي يطفئ بدوره رسالة MIAT الضارة التي تشجّع تكوين الندب وموت الخلايا. وبما أن MIAT مرتفعة في عدة أمراض قلبية بشرية وحتى تتداول في الدم كمؤشر محتمل لتضرر القلب، فقد يكمل استهداف محور BACH2–MIAT العلاجات الحالية. قد تساعد استراتيجيات تعزِّز نشاط BACH2، أو تضبط بدقّة إشارات β-arrestin1 المنحازة بأدوية مثل الكارفيديلول، أو تسكت MIAT مباشرة بأدوات قائمة على الـ RNA في المستقبل على منع تصلّب القلوب التالفة وفشلها.
الاستشهاد: Moukette, B., Teoh, Jp., Hashmi, W.J. et al. BACH2 links β1-adrenergic receptor/β-arrestin1 signaling to MIAT to inhibit cardiac fibroblast activation and cardiomyocyte apoptosis. Cell Death Discov. 12, 127 (2026). https://doi.org/10.1038/s41420-026-02985-4
الكلمات المفتاحية: فشل القلب, تليف قلبي, حمض نووي ريبوزي طويل غير مشفر, علاج بمضادات بيتا, موت خلايا القلب المبرمج