Clear Sky Science · tr
BACH2, β1-adrenerjik reseptör/β-arrestin1 sinyalini MIAT ile bağlayarak kardiyak fibroblast aktivasyonunu ve kardiyomiyosit apoptozunu engelliyor
Bu kalp çalışması neden önemli
Kalp krizleri ve kronik kalp yetmezliği, yaralanmış kalp kasının skar dokusu ile yer değiştirmesi ve yaşamsal kalp hücrelerinin ölmesi nedeniyle hâlâ başlıca ölüm nedenleri arasındadır. Bu çalışma, yaygın bir beta‑bloker ilaç tarafından açılan ve zararlı bir skar ve hücre ölümü sinyalini kapatan hücre içi daha önce bilinmeyen bir güvenlik anahtarını ortaya çıkarıyor. Bu yerleşik koruyucu yolun anlaşılması, hasarlı kalplerin daha uzun ve daha iyi çalışmasını sağlayacak daha hassas tedavilere işaret edebilir.
Başarısız kalplerde zararlı bir mesaj
Kalbin bir bölgesi kana mahrum kaldığında birçok çalışan kas hücresi (kardiyomiyosit) ölür ve destek hücreleri olan fibroblastlar tarafından oluşturulan sert skar ile yer değiştirir. Önceki araştırmalar, MIAT adlı uzun kodlamayan bir RNAnın toksik bir mesaj gibi davrandığını; skarlaşmayı ve programlı hücre ölümünü destekleyen genleri artırdığını ortaya koydu. MIAT düzeyleri çeşitli insan kalp hastalıklarında ve çok sayıda hayvan modelinde yükselir; farelerde MIAT bloke edildiğinde kalp krizi sonrası kalp fonksiyonu iyileşir. Ancak şimdiye kadar MIAT’ı neyin kontrol ettiği veya standart kalp ilaçlarının MIAT üzerinde nasıl etkili olabileceği bilinmiyordu.
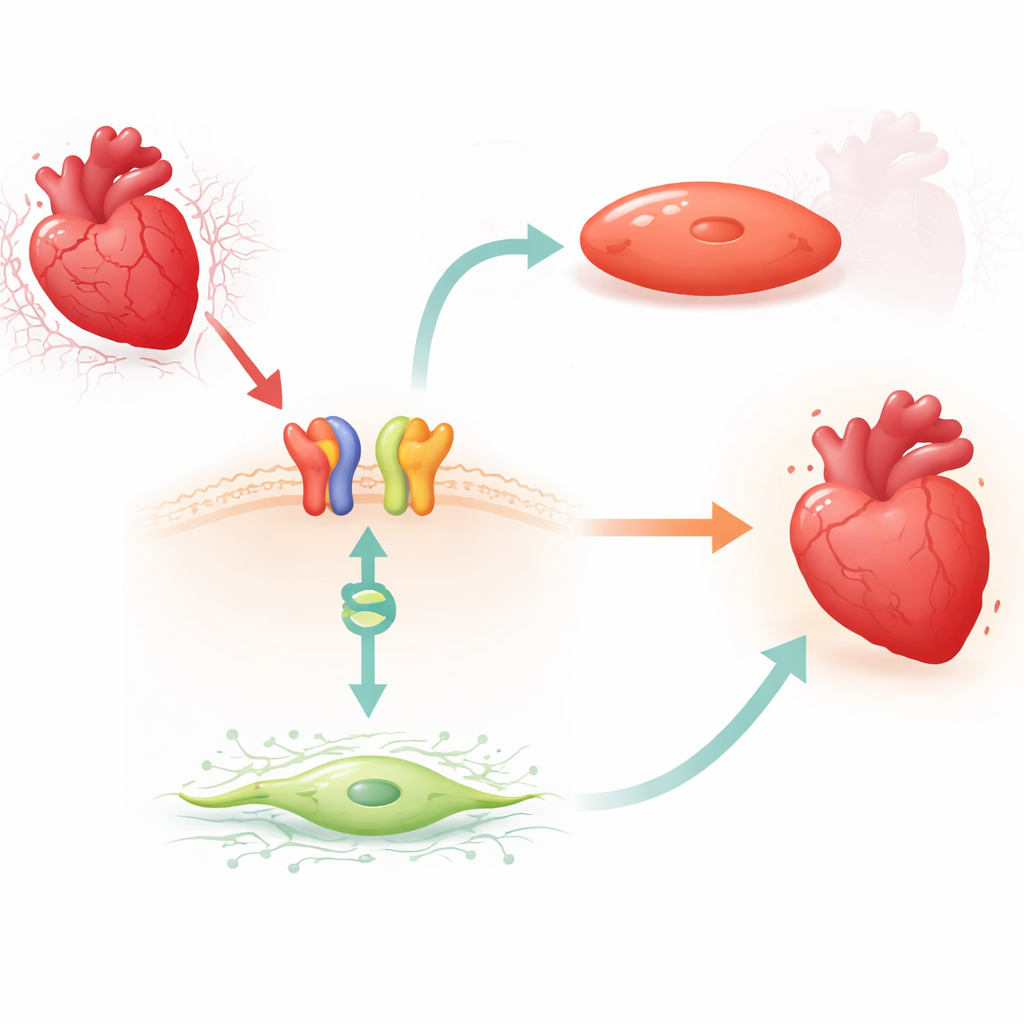
Yüzey sinyalinden gen anahtarına ilaçla tetiklenen bağ
Araştırmacılar, β1‑adrenerjik reseptörleri ve bir adaptör proteini olan β‑arrestin1 aracılığıyla koruyucu bir sinyal yolunu tetikleyebilen yaygın olarak kullanılan bir beta‑bloker olan carvedilole odaklandı. Farelerde kısa süreli carvedilol tedavisinin sol ventrikülde MIAT düzeylerini sürekli düşürdüğünü, ancak bunun yalnızca β1 reseptörleri ve β‑arrestin1 mevcut olduğunda gerçekleştiğini buldular. Benzer MIAT azalması, yetişkin insan kardiyak fibroblastlarında ve düşük oksijen‑yeniden oksijenasyonun laboratuvar modeline maruz bırakılan insan ve kemirgen kalp kası hücrelerinde de gözlendi. Bu sistemlerin tümünde stres MIAT’ı artırırken carvedilol bu yükselmeyi tersine çevirdi; bu da ilacın zararlı RNA üzerinde doğal bir fren mekanizmasını kullandığını düşündürüyor.
Zararlı RNA’yı susturan koruyucu protein
Daha derine inen ekip, hücre çekirdeğinde β‑arrestin1 ile ortaklık kurabilecek bir DNA‑bağlayıcı protein aradı. Daha önce diğer kalp yaralanmalarına karşı koruma ile ilişkilendirilmiş fakat bu bağlamda incelenmemiş bir transkripsiyon faktörü olan BACH2’ye odaklandılar. Biyokimyasal bağlanma testleri kullanarak BACH2’nin MIAT promotöründeki korunmuş dizilere bağlandığını gösterdiler; promotör MIAT üretimini yöneten kontrol bölgesidir. İnsan kalp fibroblastlarında ve kardiyomiyositlerde BACH2’yi artırmak MIAT düzeylerini düşürürken, BACH2’yi susturmak MIAT’ı yükseltti. Önemli olarak, ileri kalp yetmezliği olan hastaların kalpleri ve kalp krizi sonrası farelerden alınan kalpler aynı paterni gösterdi: BACH2 düzeyleri MIAT yüksek olduğunda düşüktü. Farelerde carvedilol tedavisi, yüzeydeki ilaç sinyalini bu nükleer gen anahtarına bağlayarak β1‑ve β‑arrestin1‑bağımlı biçimde BACH2 ekspresyonunu artırdı.
Kalp hücrelerini skarlaşma ve ölümden korumak
Ekip daha sonra BACH2’nin kardiyak destek ve kas hücrelerinde gerçekte ne yaptığını sordu. Kültürdeki insan kardiyak fibroblastlarında BACH2 kaybı fibroz belirteçlerini artırdı, hücre büyümesini ve hücre göçünü hızlandırdı—bunlar skar birikimini destekleyen davranışlar—oysa fazla BACH2 bu fibrotik özellikleri zayıflattı. İnsan ve fare kardiyomiyositlerinde BACH2’yi azaltmak daha fazla hücre ölümü ve ölümle ilişkili enzimlerin artmış aktivitesi ile birlikte doğal hayatta kalma proteinlerinin düşmesine yol açtı. BACH2 aşırı ifadesi ters etki göstererek stres altında hücre sağkalımını korudu. Birlikte, bu deneyler carvedilolün β1 reseptörlerini ve β‑arrestin1’i aktive ettiğini; bunların çekirdekte BACH2 ile işbirliği yaparak MIAT’ı azaltıp böylece skarlaşma ve hücre kaybını sınırladığı bir modeli destekliyor.
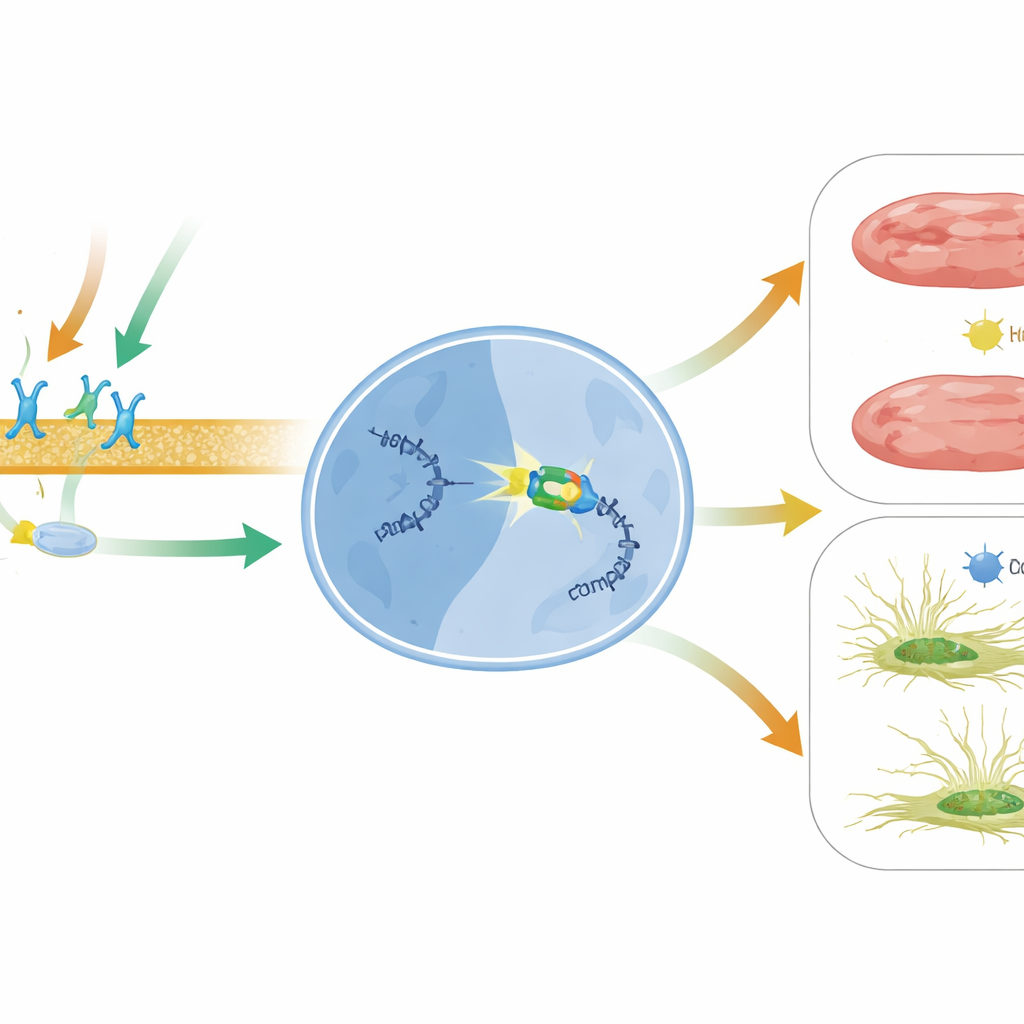
Gelecekteki kalp tedavileri için anlamı
Basitçe söylemek gerekirse, bu çalışma başarısız kalpte yeni bir koruyucu ekseni ortaya koyuyor: ilaca bağlı β1 reseptör ve β‑arrestin1 sinyali BACH2’yi açıyor; BACH2 ise skar oluşumunu ve hücre ölümünü teşvik eden zararlı MIAT mesajını kapatıyor. MIAT birçok insan kalp hastalığında yükseldiği ve hatta kalp hasarının potansiyel bir belirteci olarak kanda dolaştığı için, bu BACH2–MIAT yolunu hedeflemek mevcut tedavilere tamamlayıcı olabilir. BACH2 aktivitesini artıran stratejiler, carvedilol gibi ilaçlarla β‑arrestin1‑yanlı sinyallemeyi hassaslaştırma veya doğrudan MIAT’ı RNA‑temelli araçlarla susturma yaklaşımları bir gün hasarlı kalplerin sertleşmesini ve yetersizleşmesini engellemeye yardımcı olabilir.
Atıf: Moukette, B., Teoh, Jp., Hashmi, W.J. et al. BACH2 links β1-adrenergic receptor/β-arrestin1 signaling to MIAT to inhibit cardiac fibroblast activation and cardiomyocyte apoptosis. Cell Death Discov. 12, 127 (2026). https://doi.org/10.1038/s41420-026-02985-4
Anahtar kelimeler: kalp yetmezliği, kardiyak fibroz, uzun kodlamayan RNA, beta-bloker tedavisi, kardiyomiyosit apoptozu