Clear Sky Science · sv
BACH2 kopplar β1‑adrenerg receptor/β‑arrestin1‑signalering till MIAT för att hämma aktivering av hjärtfibroblaster och apoptos i kardiomyocyter
Varför denna hjärtstudie är viktig
Hjärtinfarkt och kronisk hjärtsvikt är fortfarande ledande dödsorsaker, delvis eftersom skadad hjärtmuskel ersätts av ärrvävnad och viktiga hjärtceller går förlorade. Denna studie avslöjar en tidigare okänd säkerhetsbrytare i hjärtceller som aktiveras av ett vanligt beta‑blockerande läkemedel och som i sin tur stänger av en skadlig RNA‑signal kopplad till ärrbildning och celldöd. Att förstå denna inbyggda skyddsmekanism kan peka ut mer precisa behandlingar som hjälper skadade hjärtan att fortsätta pumpa längre och bättre.
Ett skadligt budskap i hjärtsvikt
När en del av hjärtat blir utan blod tillfogas många fungerande muskelceller (kardiomyocyter) och ersätts av stel ärrvävnad som bildas av stödjeceller kallade fibroblaster. Tidigare forskning identifierade ett långt icke‑kodande RNA kallat MIAT som fungerar som ett toxiskt budskap: det ökar uttrycket av gener som främjar ärrbildning och programmerad celldöd. MIAT‑nivåerna ökar vid flera mänskliga hjärtsjukdomar och i olika djurmodeller för hjärtskada, medan blockering av MIAT hos möss förbättrar hjärtfunktionen efter infarkt. Fram till nu har dock kontrollen av MIAT och hur vanliga hjärtmediciner påverkar den varit okänd.
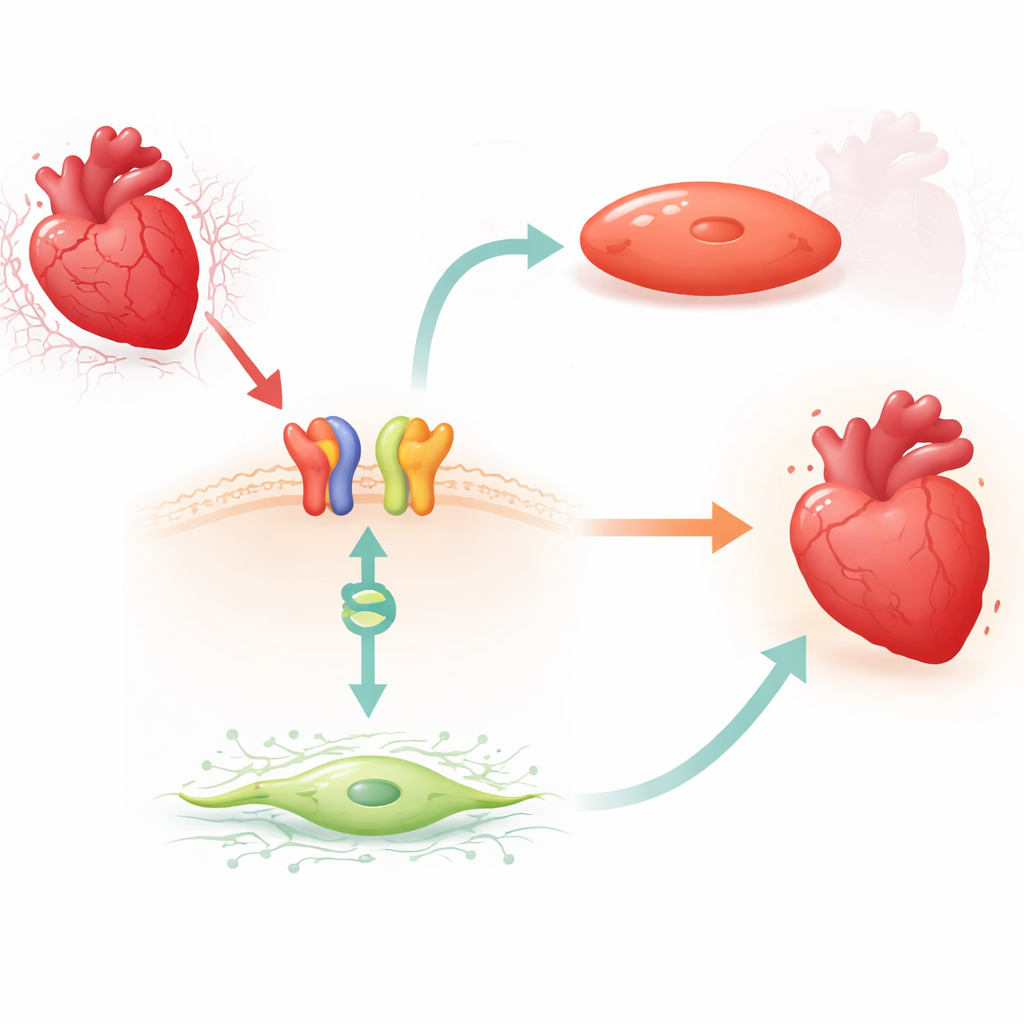
En läkemedelsaktiverad länk från ytsignal till genreglering
Forskarna fokuserade på carvedilol, ett mycket använt beta‑blockerande läkemedel som kan aktivera en skyddande signalväg via β1‑adrenerg receptor och ett adaptorprotein kallat β‑arrestin1. Hos möss fann de att kortvarig behandling med carvedilol konsekvent minskade MIAT‑nivåerna i vänster kammare, men bara när β1‑receptorer och β‑arrestin1 var närvarande. Liknande minskningar av MIAT observerades i vuxna humana hjärtfibroblaster och i humana och gnagarhjärtmuskelceller utsatta för en laborativ modell av syrebrist och återoksygenering. I dessa system ökade stress MIAT, medan carvedilol vände denna ökning, vilket tyder på att läkemedlet utnyttjar en naturlig broms på det skadliga RNA:t.
Vaktproteinet som tystar det skadliga RNA:t
För att gå djupare letade teamet efter ett DNA‑bindande protein som skulle kunna samarbeta med β‑arrestin1 i cellkärnan. De identifierade BACH2, en transkriptionsfaktor tidigare kopplad till skydd mot andra former av hjärtskada men inte studerad i detta sammanhang. Med biokemiska bindningstester visade de att BACH2 fäster vid bevarade regioner i MIAT‑promotorn, kontrollområdet som driver MIAT‑produktion. I humana hjärtfibroblaster och kardiomyocyter minskade MIAT‑nivåerna när BACH2 ökades, medan tystande av BACH2 höjde MIAT. Viktigt är att hjärtan från patienter med avancerad hjärtsvikt och från möss efter infarkt visade samma mönster: låga BACH2‑nivåer när MIAT var högt. Carvedilolbehandling hos möss ökade BACH2‑uttrycket på ett β1‑ och β‑arrestin1‑beroende sätt, vilket kopplar ytlig läkemedelssignal till denna nukleära genbrytare.
Skydd av hjärtceller mot ärrbildning och död
Teamet undersökte sedan vad BACH2 faktiskt gör med stödje‑ och muskelceller i hjärtat. I odlade humana hjärtfibroblaster ökade förlust av BACH2 markörer för fibros, ökade celltillväxt och förbättrad cellmigration—beteenden som gynnar ärrbildning—medan mer BACH2 dämpade dessa fibrotiska egenskaper. I humana och murina kardiomyocyter ledde minskat BACH2 till fler döende celler och högre aktivitet av dödsrelaterade enzymer, tillsammans med minskade nivåer av naturliga överlevnadsproteiner. Överuttryck av BACH2 gav motsatta effekter och bevarade cellöverlevnad under stress. Tillsammans stödjer dessa experiment en modell där carvedilol aktiverar β1‑receptorer och β‑arrestin1, vilka sedan samarbetar med BACH2 i kärnan för att sänka MIAT och därigenom begränsa ärrbildning och celldöd.
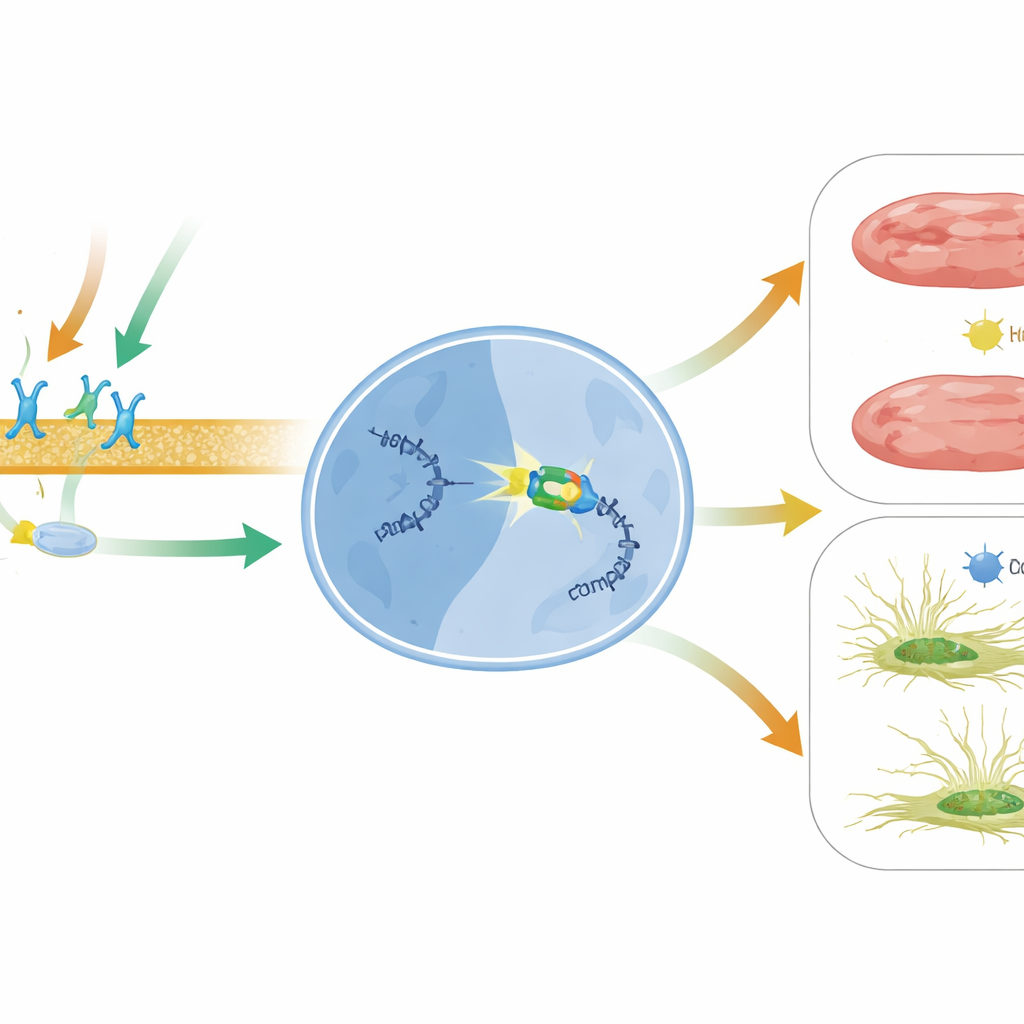
Vad detta kan innebära för framtida hjärtbehandlingar
Förenklat visar detta arbete en ny skyddsaxel i det sviktande hjärtat: läkemedelsutlösta β1‑receptor‑ och β‑arrestin1‑signaler slår på BACH2, som i sin tur stänger av det skadliga MIAT‑budskapet som driver ärrbildning och celldöd. Eftersom MIAT är förhöjt i flera mänskliga hjärtsjukdomar och till och med cirkulerar i blodet som en möjlig markör för hjärtskada, kan mål mot denna BACH2–MIAT‑väg komplettera befintliga behandlingar. Strategier som ökar BACH2‑aktivitet, finjusterar β‑arrestin1‑förskjuten signalering med läkemedel som carvedilol, eller direkt tystar MIAT med RNA‑baserade verktyg kan en dag hjälpa till att förhindra att skadade hjärtan blir stela och sviktar.
Citering: Moukette, B., Teoh, Jp., Hashmi, W.J. et al. BACH2 links β1-adrenergic receptor/β-arrestin1 signaling to MIAT to inhibit cardiac fibroblast activation and cardiomyocyte apoptosis. Cell Death Discov. 12, 127 (2026). https://doi.org/10.1038/s41420-026-02985-4
Nyckelord: hjärtsvikt, hjärtfibros, lång icke‑kodande RNA, beta‑blockerande behandling, kardiomyocytapoptos