Clear Sky Science · zh
成纤维细胞介导的KRAS激活在双阴性前列腺癌中的作用
这项前列腺癌研究为何重要
对许多男性而言,阻断激素的治疗可以让前列腺癌多年处于可控状态。然而有些肿瘤最终以一种隐蔽的形式复发,不再对激素药物响应,也不会在常规血液检测中显现。该研究探究了这些“双阴性”前列腺癌如何生存与扩散,揭示了癌细胞与其周围支持细胞之间的隐秘对话——并指向了一个未来药物可能利用的新薄弱环节。
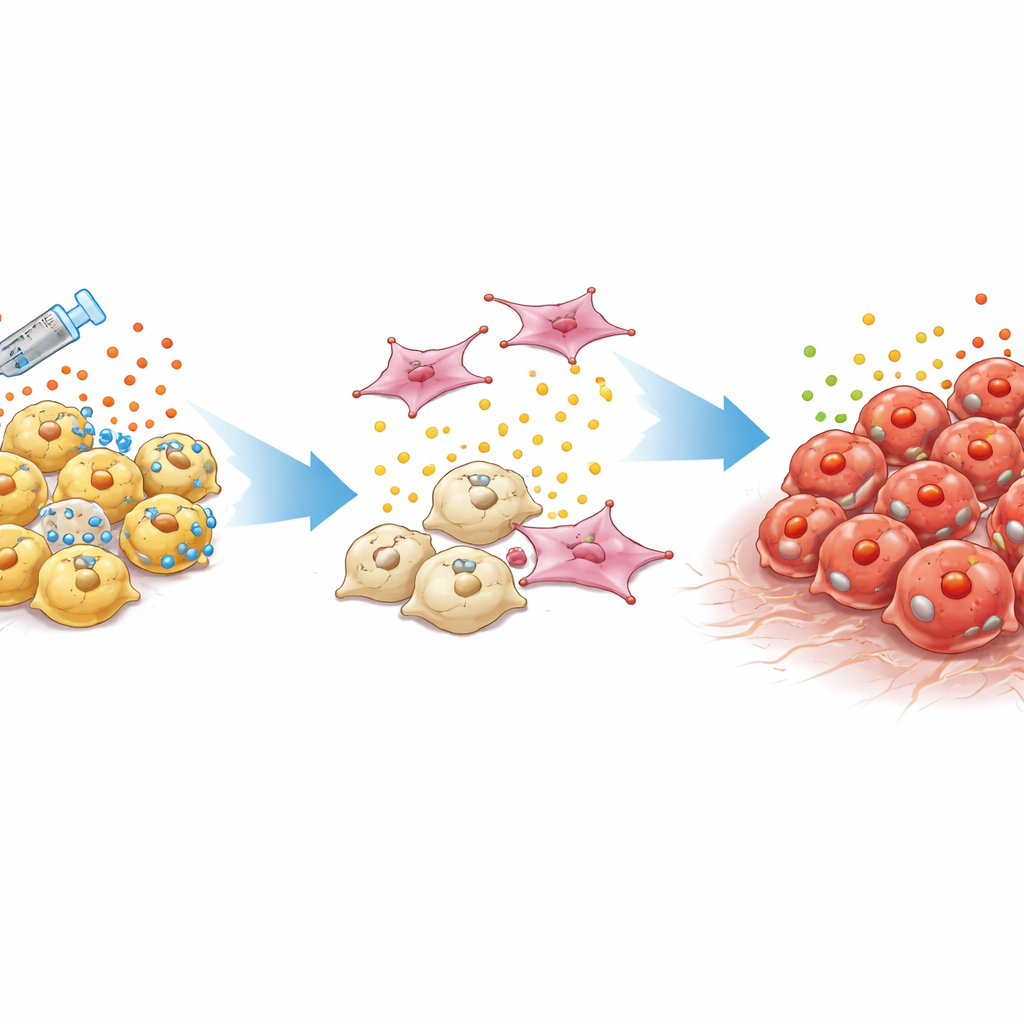
一种难以检测、难以治疗的肿瘤类型
常见的前列腺癌依赖男性激素通过一种称为雄激素受体的蛋白发挥作用。医生通过激素疗法和新型靶向药物抑制这一信号。然而,随着时间推移,部分肿瘤会演化为去势抗性前列腺癌,不再依赖该通路。其中一种尤其危险的亚型,被称为双阴性前列腺癌,既缺乏雄激素受体活性,也不具备类似神经内分泌细胞的特征。这些肿瘤常在局部复发或转移,尽管常规血液标志物水平很低,临床医生因此缺乏线索且没有经证实的有效治疗手段。
一种在激素被关闭时启动的生长引擎
研究者将注意力集中在KRAS上,这是一个在肺癌和结肠癌中因突变而驱动生长的著名分子开关。在前列腺癌中,此类突变并不常见,但患者的DNA分析提示KRAS可能参与双阴性病例。通过比较不同的前列腺癌细胞系,他们发现KRAS信号在依赖激素的细胞中作用甚微,但在细胞不再依赖雄激素信号时变得至关重要。在类DNPC细胞中,减少KRAS显著削弱了它们的增殖、迁移和侵袭能力,而对激素敏感的细胞几乎不受影响——这表明KRAS仅在后期的激素非依赖状态中成为关键动力。
邻近支持细胞如何喂养癌症开关
肿瘤不仅仅是失控的癌细胞;它们是包含成纤维细胞等细胞的群落——这些结缔组织细胞帮助塑造局部环境。研究团队发现,当前列腺癌细胞的雄激素信号被阻断时,癌细胞改变了其表面受体的类型,变得更容易响应一种称为FGF8的生长信号。与此同时,饥饿于激素的癌细胞向周围释放一种报警信号——趋化因子CCL2。晚期前列腺肿瘤中的类成纤维基质细胞携带CCL2受体。当CCL2到达这些基质细胞时,会打开它们内部的一条通路,增强它们产出并释放FGF8。随后,FGF8反馈到癌细胞,激活其改变后的受体,进而触发KRAS,驱动强烈的生长与生存信号。
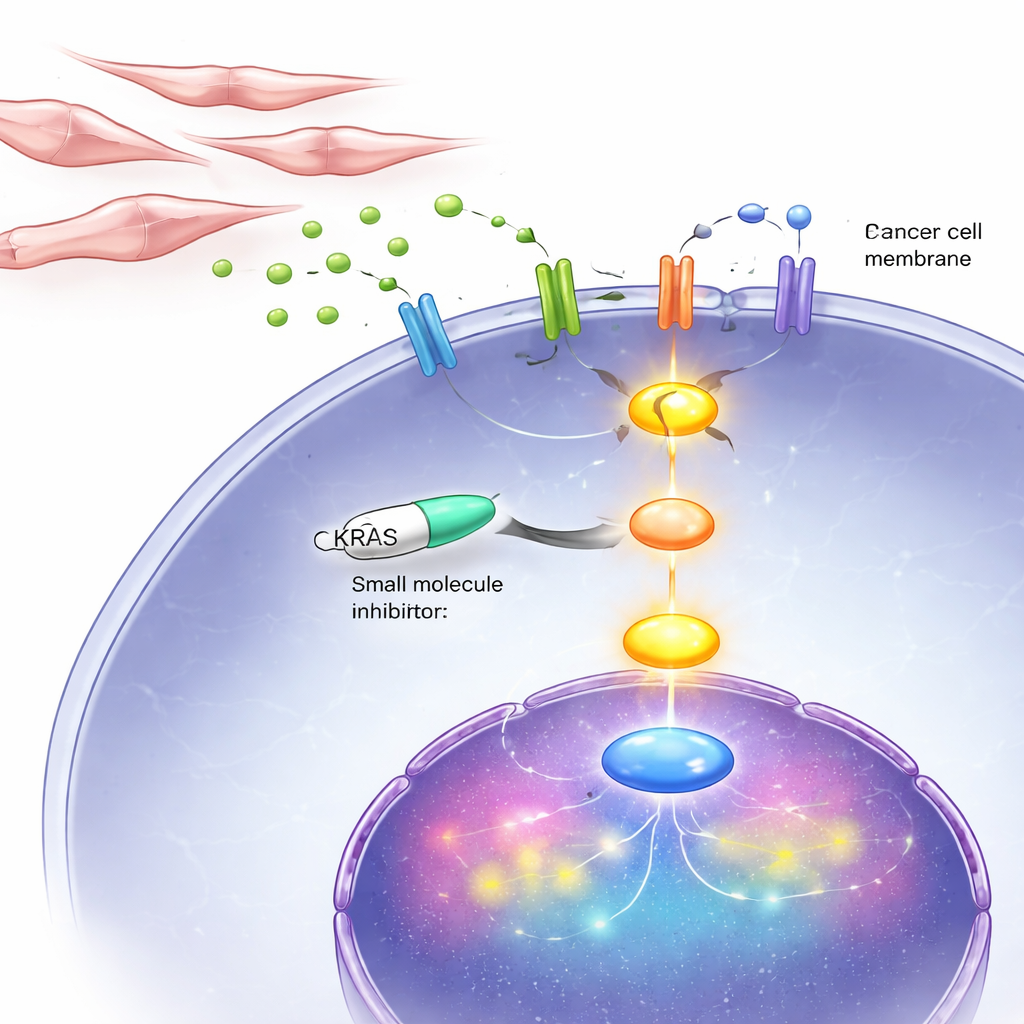
在细胞与小鼠体内阻断KRAS生命线
由于这一恶性循环最终汇聚于KRAS,研究者测试了一种药物BI-3406,该药干扰KRAS在细胞内的激活方式。在培养皿中,该抑制剂显著减缓了雄激素非依赖性前列腺癌细胞的生长与迁移,包括那些具有异常KRAS的细胞以及那些经由成纤维细胞信号激活正常KRAS的细胞。在植入类DNPC肿瘤的小鼠中,每日给予该抑制剂可使肿瘤缩小并降低细胞分裂标志物,同时增加程序性细胞死亡的迹象。重要的是,该药对依赖激素的癌细胞影响要小得多,这再次呼应了KRAS在后期双阴性阶段的特殊关键性。
这对未来治疗意味着什么
对普通读者而言,结论是:当激素治疗将前列腺癌逼入困境时,肿瘤可通过招募附近的成纤维细胞来获取另一种生长信号,最终激活KRAS逃脱控制。该研究详尽绘制了这一路径,并显示切断KRAS信号可以在模型中杀死这些耐药细胞。尽管在患者身上还需更多研究,尤其是需要安全阻断KRAS或其上游助因子的药物,但这些发现强调了一种新策略:针对CCL2–FGF8–KRAS链以治疗最顽固、激素非依赖的前列腺癌形式。
引用: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
关键词: 双阴性前列腺癌, 肿瘤微环境, KRAS信号, 成纤维细胞, 去势不敏感性癌症