Clear Sky Science · tr
Fibroblast kaynaklı KRAS aktivasyonu çift-negatif prostat kanserinde
Bu prostat kanseri çalışması neden önemli
Birçok erkek için hormon baskılayıcı tedaviler prostat kanserini yıllarca kontrol altında tutabilir. Ancak bazı tümörler sonunda hormon ilaçlarına yanıt vermeyen ve olağan kan testlerinde belirti vermeyen gizli bir formda geri döner. Bu çalışma, bu "çift-negatif" prostat kanserlerinin nasıl hayatta kaldığını ve yayıldığını araştırıyor; kanser hücreleri ile çevrelerindeki destek hücreleri arasındaki gizli konuşmayı ortaya koyuyor ve gelecekteki ilaçların hedefleyebileceği yeni bir zayıf noktaya işaret ediyor.
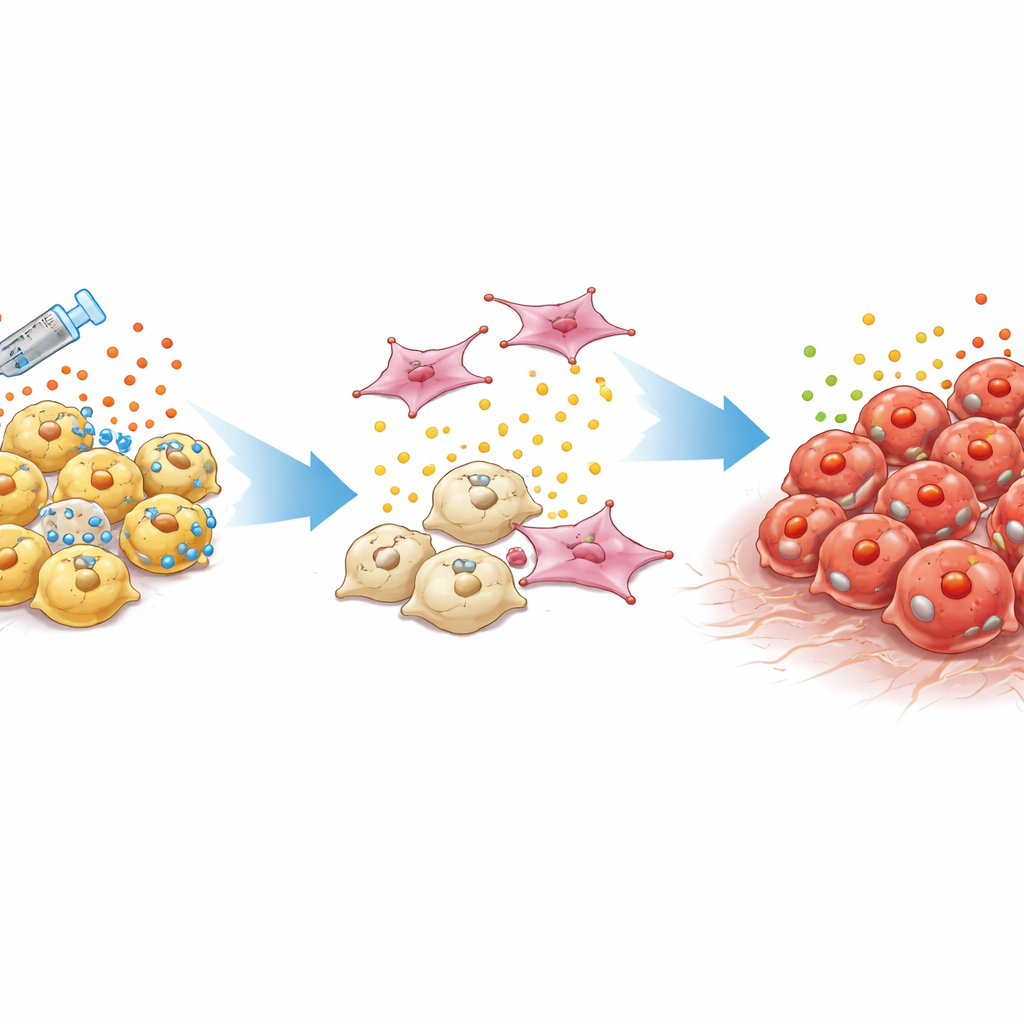
Bulması ve tedavisi zor bir tümör tipi
Standart prostat kanserleri, androjen reseptörü adı verilen bir protein aracılığıyla çalışan erkek hormonlarına bağımlıdır. Hekimler bu sinyali hormon tedavisi ve daha yeni hedefe yönelik ilaçlarla baskılar. Ancak zamanla bazı tümörler bu yoldan bağımsızlaşarak kastrasyon dirençli prostat kanserine dönüşür. Özellikle tehlikeli bir alt tip olan çift-negatif prostat kanseri, hem androjen reseptör aktivitesinden hem de sinir-benzeri “nöroendokrin” hücre özelliklerinden yoksundur. Bu tümörler genellikle düşük kan belirteçlerine rağmen yerel olarak tekrar büyür veya yayılır; klinisyenlere az ipucu bırakır ve kanıtlanmış bir tedavi seçeneği yoktur.
Hormonlar kapatıldığında devreye giren bir büyüme motoru
Araştırmacılar, akciğer ve kolon kanserlerinde mutasyonla etkinleştiğinde büyümeyi tetikleyen iyi bilinen moleküler bir anahtar olan KRAS’a odaklandı. Prostat kanserinde bu tür mutasyonlar nadirdir, fakat hasta DNA profillemesi KRAS’ın çift-negatif vakalarda rol alabileceğine işaret etti. Farklı prostat kanseri hücre hatlarını karşılaştırarak, KRAS sinyalinin hormon-bağımlı hücrelerde çok az etkisi olduğunu, ancak hücreler androjen sinyallerine artık bağımlı olmadığında bunun kritik hale geldiğini buldular. DNPC-benzeri hücrelerde KRAS’ı azaltmak, büyüme, hareket ve invazyon yeteneklerini keskin şekilde düşürürken; hormon-duyarlı hücreler kaybı neredeyse fark etmedi—bu da KRAS’ın ancak geç, hormon-bağımsız durumda kilit bir motor haline geldiğini düşündürüyor.
Yakındaki destek hücrelerin kanser anahtarını nasıl beslediği
Tümörler yalnızca asi kanser hücreleri değildir; fibroblastlar gibi yerel ortamı şekillendiren bağ dokusu hücrelerini de içeren bir topluluktur. Ekip, androjen sinyali baskılandığında prostat kanseri hücrelerinin yüzeylerinde sergiledikleri reseptör türlerini değiştirdiğini ve FGF8 adlı bir büyüme sinyaline daha duyarlı hale geldiklerini keşfetti. Aynı zamanda hormon yoksunu kanser hücreleri çevrelerine CCL2 adlı bir kimokin göndererek bir tür alarm sinyali salıyor. İleri prostat tümörlerindeki fibroblast-benzeri stromal hücreler CCL2 için reseptör taşır. CCL2 bu stromal hücrelere ulaştığında, onlar içinde FGF8 üretimini ve salgılanmasını artıran bir iç yolu açar. O FGF8 geri kanser hücrelerine döner, değişmiş reseptörlerini aktive eder ve bunun sonucunda KRAS’ı açarak güçlü büyüme ve hayatta kalma sinyallerini tetikler.
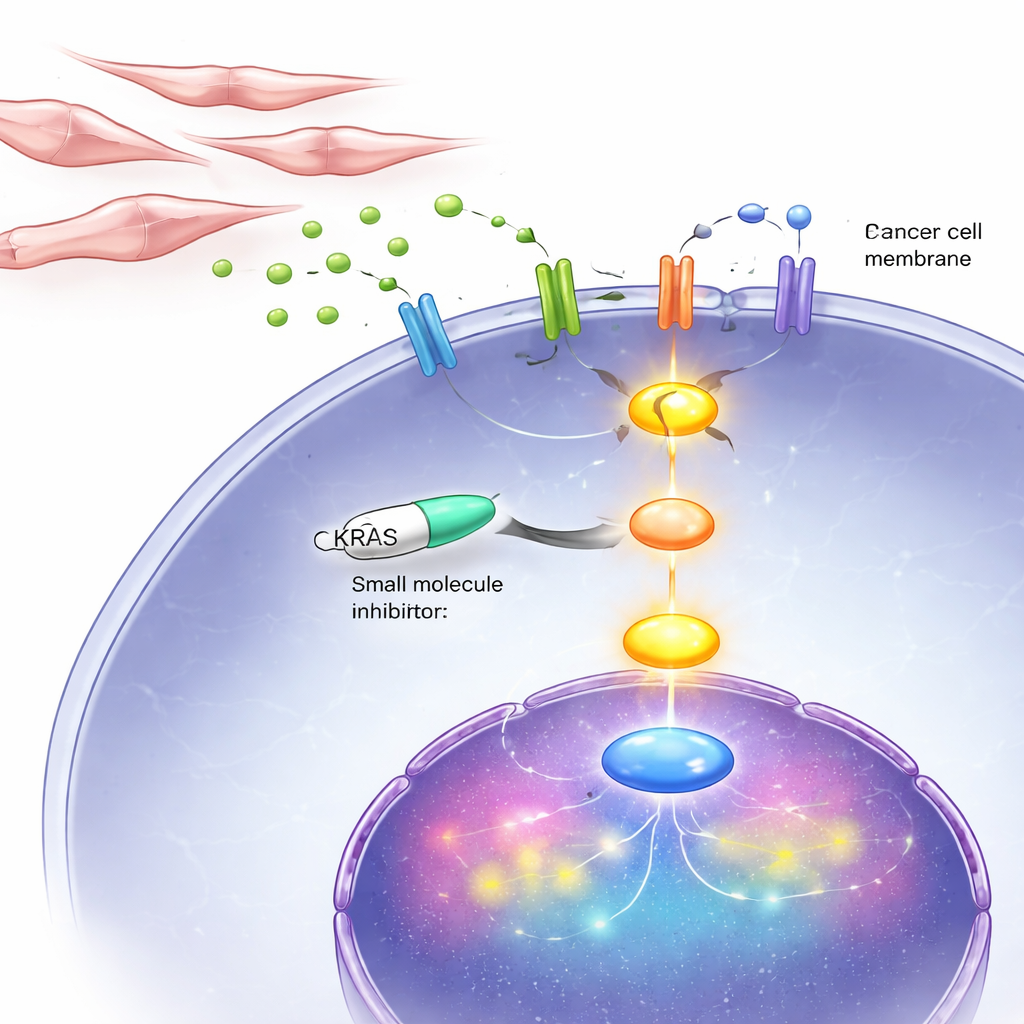
Hücrelerde ve farelerde KRAS yaşam hattını kesmek
Bu kötü döngü nihayetinde KRAS üzerinden aktığı için araştırmacılar, KRAS’ın hücre içinde nasıl açıldığını bozan BI-3406 adlı bir ilacı denediler. Laboratuvar kaplarında, bu inhibitör androjen-bağımsız prostat kanseri hücrelerinin, anormal KRAS’a sahip olanların da dahil olduğu ve fibroblastlardan gelen sinyallerle aktive olmuş normal KRAS’lı hücrelerin büyüme ve hareketini güçlü biçimde yavaşlattı. DNPC-benzeri tümörlerle implant edilen farelerde günlük uygulama, tümörleri küçülttü ve hücre bölünmesi belirteçlerini azalttı; aynı zamanda programlı hücre ölümü belirtilerini artırdı. Önemli olarak, ilaç hormon-bağımlı kanser hücreleri üzerinde çok daha az etkiye sahipti; bu da KRAS’ın özellikle geç, çift-negatif aşamada kritik olduğu fikrini destekliyor.
Gelecekteki tedavi için ne anlama geliyor
Halk için alınacak mesaj şu: hormon tedavisi prostat kanserini köşeye sıkıştırdığında, tümör yakındaki fibroblastları farklı bir büyüme sinyaliyle besleyerek kaçabilir ve bu sinyal nihayetinde KRAS’ı açar. Bu çalışma, o kaçış yolunu ayrıntılı şekilde haritalandırıyor ve KRAS sinyalini kesmenin modellerde bu dirençli hücreleri öldürebildiğini gösteriyor. Hastalarda, özellikle KRAS’ı ya da onun yukarı akışındaki yardımcıları güvenle bloke edebilen ilaçlarla daha fazla çalışma gerekse de, bulgular yeni bir stratefiye işaret ediyor: en inatçı, hormon-bağımsız prostat kanseri formlarını tedavi etmek için CCL2–FGF8–KRAS zincirini hedeflemek.
Atıf: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Anahtar kelimeler: çift-negatif prostat kanseri, tümör mikroçevresi, KRAS sinyalleşmesi, fibroblastlar, androjen-bağımsız kanser