Clear Sky Science · fr
Activation de KRAS médiée par des fibroblastes dans le cancer de la prostate double-négatif
Pourquoi cette étude sur le cancer de la prostate est importante
Pour de nombreux hommes, les traitements bloquant les hormones peuvent contenir le cancer de la prostate pendant des années. Pourtant, certains tumeurs réapparaissent finalement sous une forme furtive qui ne répond plus aux médicaments hormonaux et ne déclenche pas les tests sanguins habituels. Cette étude examine comment ces cancers de la prostate « double-négatifs » survivent et se propagent, révélant une conversation cachée entre les cellules cancéreuses et leurs cellules de soutien environnantes — et mettant en lumière une vulnérabilité nouvelle que de futurs médicaments pourraient exploiter.
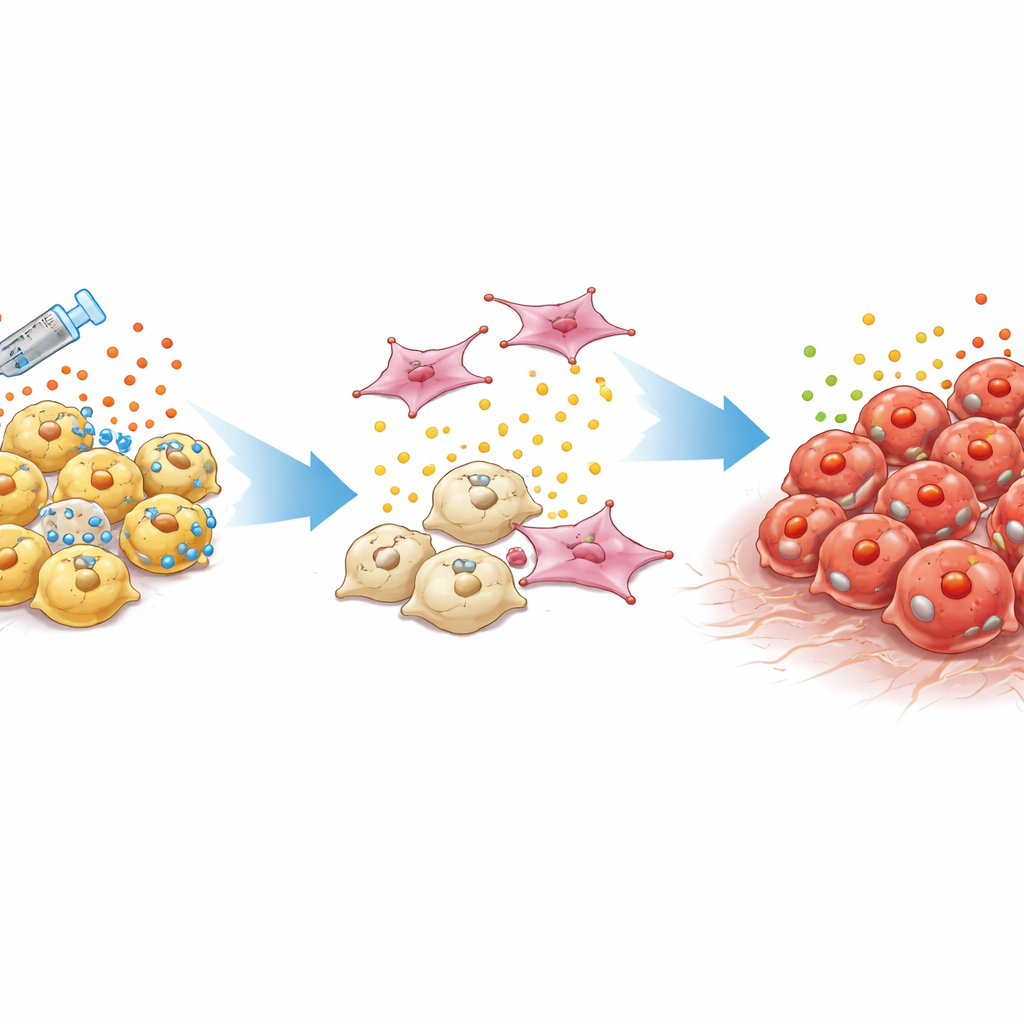
Un type de tumeur difficile à détecter et à traiter
Les cancers de la prostate standard dépendent des hormones masculines agissant via une protéine appelée récepteur des androgènes. Les médecins suppriment ce signal par hormonothérapie et par des médicaments ciblés plus récents. Avec le temps, toutefois, certaines tumeurs évoluent vers un cancer de la prostate résistant à la castration qui ne dépend plus de cette voie. Un sous-type particulièrement dangereux, appelé cancer de la prostate double-négatif, manque à la fois d’activité du récepteur des androgènes et des caractéristiques des cellules « neuroendocrines » de type nerveux. Ces tumeurs réapparaissent souvent localement ou se diffusent malgré de faibles niveaux des marqueurs habituels dans le sang, laissant les cliniciens avec peu d’indices et sans traitements éprouvés.
Un moteur de croissance qui s’allume quand les hormones sont éteintes
Les chercheurs se sont intéressés à KRAS, un interrupteur moléculaire bien connu qui stimule la croissance dans les cancers du poumon et du côlon lorsqu’il est muté. Dans le cancer de la prostate, de telles mutations sont rares, mais le profilage de l’ADN des patients suggérait que KRAS pourrait être impliqué dans les cas double-négatifs. En comparant différentes lignées cellulaires de cancer de la prostate, ils ont constaté que la signalisation KRAS avait très peu d’effet dans les cellules dépendantes des hormones mais devenait cruciale une fois que les cellules ne dépendaient plus des signaux androgènes. Dans les cellules de type DNPC, réduire KRAS diminuait fortement leur capacité à croître, à migrer et à envahir, tandis que les cellules sensibles aux hormones remarquaient à peine cette perte — ce qui suggère que KRAS devient un moteur clé seulement à l’état tardif et indépendant des hormones.
Comment les cellules de soutien voisines nourrissent l’interrupteur tumoral
Les tumeurs ne sont pas que des cellules cancéreuses rebelles ; ce sont des communautés qui incluent des fibroblastes — des cellules du tissu conjonctif qui aident à façonner l’environnement local. L’équipe a découvert que lorsque la signalisation androgénique est bloquée dans les cellules cancéreuses de la prostate, celles-ci changent le type de récepteurs qu’elles présentent à leur surface, devenant plus réceptives à un signal de croissance appelé FGF8. En même temps, les cellules cancéreuses privées d’hormones libèrent un signal de détresse, la chimiokine CCL2, dans leur voisinage. Les cellules stromales de type fibroblaste dans les tumeurs prostatiques avancées portent des récepteurs pour CCL2. Lorsque CCL2 atteint ces cellules stromales, il active une voie interne qui augmente leur production et libération de FGF8. Ce FGF8 revient ensuite vers les cellules cancéreuses, active leurs récepteurs modifiés et, à son tour, déclenche KRAS, entraînant des signaux puissants de croissance et de survie.
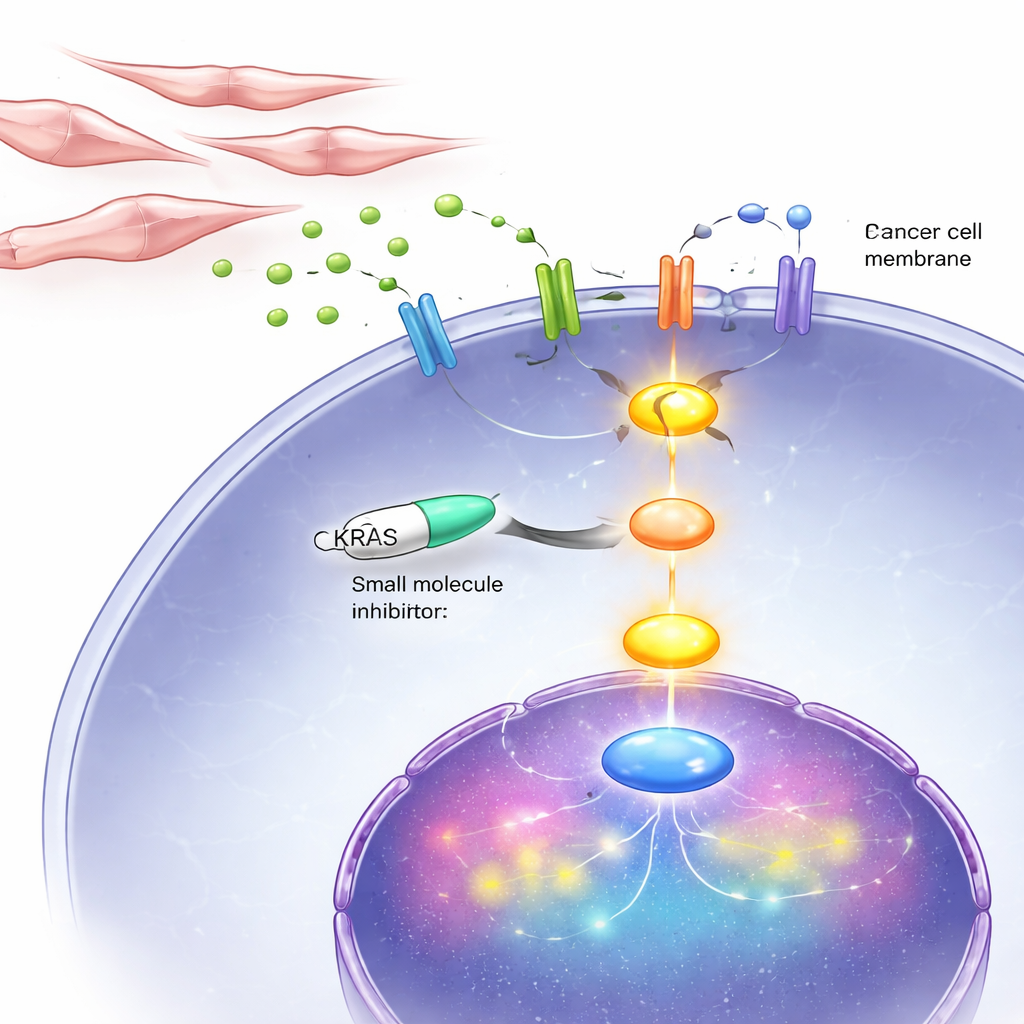
Bloquer la ligne de vie KRAS dans les cellules et chez la souris
Parce que ce cycle vicieux converge finalement sur KRAS, les chercheurs ont testé un médicament, BI-3406, qui interfère avec la façon dont KRAS est activé à l’intérieur des cellules. En culture, cet inhibiteur a fortement ralenti la croissance et la migration des cellules de cancer de la prostate indépendantes des androgènes, y compris celles avec un KRAS anormal et celles avec un KRAS normal activé par des signaux provenant des fibroblastes. Chez des souris implantées de tumeurs de type DNPC, un traitement quotidien par l’inhibiteur a réduit la taille des tumeurs et diminué les marqueurs de division cellulaire, tout en augmentant les signes d’apoptose. Fait important, le médicament a eu beaucoup moins d’effet sur les cellules cancéreuses dépendantes des hormones, ce qui renforce l’idée que KRAS est particulièrement critique au stade tardif double-négatif.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, la leçon est que lorsque l’hormonothérapie pousse le cancer de la prostate dans ses retranchements, la tumeur peut s’échapper en recrutant les fibroblastes voisins pour lui fournir un signal de croissance différent qui finit par activer KRAS. Cette étude cartographie en détail cette voie d’évasion et montre que couper la signalisation KRAS peut tuer ces cellules résistantes dans des modèles. Bien que davantage de travaux soient nécessaires chez les patients, en particulier avec des médicaments capables de bloquer KRAS ou ses activateurs en amont en toute sécurité, ces résultats soulignent une nouvelle stratégie : cibler la chaîne CCL2–FGF8–KRAS pour traiter les formes de la prostate les plus tenaces et indépendantes des hormones.
Citation: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Mots-clés: cancer de la prostate double-négatif, microenvironnement tumoral, signalisation KRAS, fibroblastes, cancer indépendant des androgènes