Clear Sky Science · ru
Активация KRAS, опосредованная фибробластами, при двукратно-негативном раке простаты
Почему это исследование рака простаты важно
Для многих мужчин гормоноблокирующая терапия способна удерживать рак простаты под контролем в течение лет. Тем не менее некоторые опухоли со временем возвращаются в скрытой форме, которая больше не реагирует на гормональные препараты и не проявляется в обычных анализах крови. В этом исследовании изучается, как эти «двукратно-негативные» опухоли выживают и распространяются, раскрывая скрытый диалог между раковыми клетками и окружающими их опорными клетками — и указывая на новую уязвимость, которой в будущем могут воспользоваться лекарства.
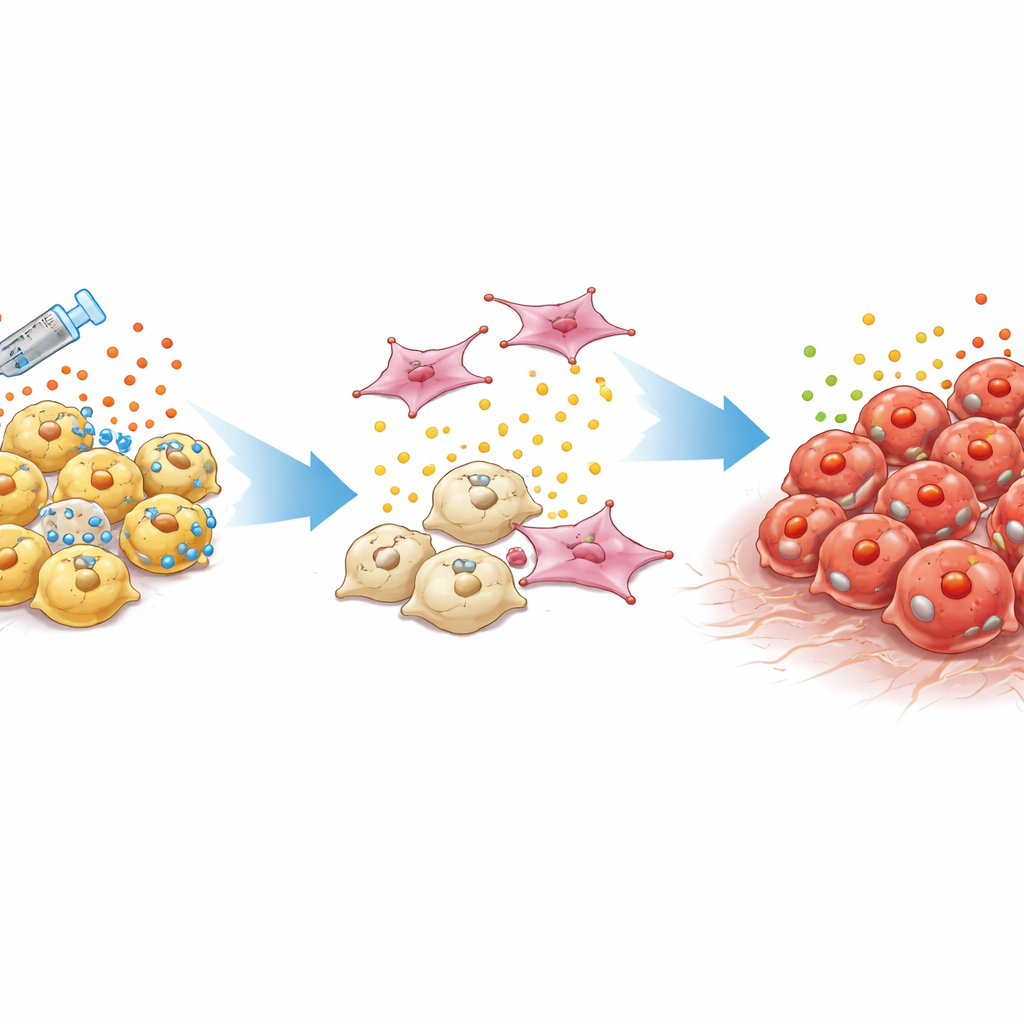
Труднообнаружимый и трудноизлечимый тип опухоли
Стандартные раки простаты зависят от мужских гормонов, действующих через белок, называемый андрогенным рецептором. Врачи подавляют этот сигнал с помощью гормональной терапии и новых таргетных препаратов. Со временем, однако, некоторые опухоли эволюционируют в кастрационно-резистентный рак простаты, который больше не опирается на этот путь. Особенно опасный подтип, называемый двукратно-негативным раком простаты, лишён как активности андрогенного рецептора, так и признаков нейроэндокринных клеток. Такие опухоли часто рецидивируют локально или дают метастазы, несмотря на низкие уровни обычных маркеров в крови, оставляя клиницистов без подсказок и без доказанных методов лечения.
Двигатель роста, который включается при выключении гормонов
Исследователи сосредоточились на KRAS — хорошо известном молекулярном переключателе, который при мутациях стимулирует рост при раках лёгких и толстой кишки. При раке простаты такие мутации редки, но профилирование ДНК пациентов намекало на участие KRAS в двукратно-негативных случаях. Сравнивая разные линии клеток рака простаты, они обнаружили, что сигнализация KRAS слабо проявлялась в гормонозависимых клетках, но становилась критически важной, как только клетки переставали полагаться на андрогенные сигналы. В клетках, похожих на DNPC, подавление KRAS резко снижало их способность к росту, подвижности и инвазии, тогда как гормоночувствительные клетки почти не реагировали на утрату — что свидетельствует о том, что KRAS превращается в ключевой двигатель только на поздней, гормон-независимой стадии.
Как соседние опорные клетки подпитывают переключатель рака
Опухоли — это не просто одиночные раковые клетки; это сообщества, включающие фибробласты — клетки соединительной ткани, формирующие местную среду. Команда обнаружила, что при блокаде андрогенной сигнализации раковые клетки простаты меняют наборы рецепторов на своей поверхности, становясь более восприимчивыми к ростовому сигналу FGF8. Одновременно гормон-обеднённые раковые клетки выделяют в окружение сигнал бедствия — хемокин CCL2. Стромальные клетки, похожие на фибробласты, в продвинутых опухолях простаты несут рецепторы для CCL2. Когда CCL2 достигает этих стромальных клеток, он включает внутриклеточный путь, который усиливает их синтез и секрецию FGF8. Этот FGF8 затем возвращается к раковым клеткам, активирует их изменённые рецепторы и, в свою очередь, запускает KRAS, стимулируя мощные сигналы роста и выживания.
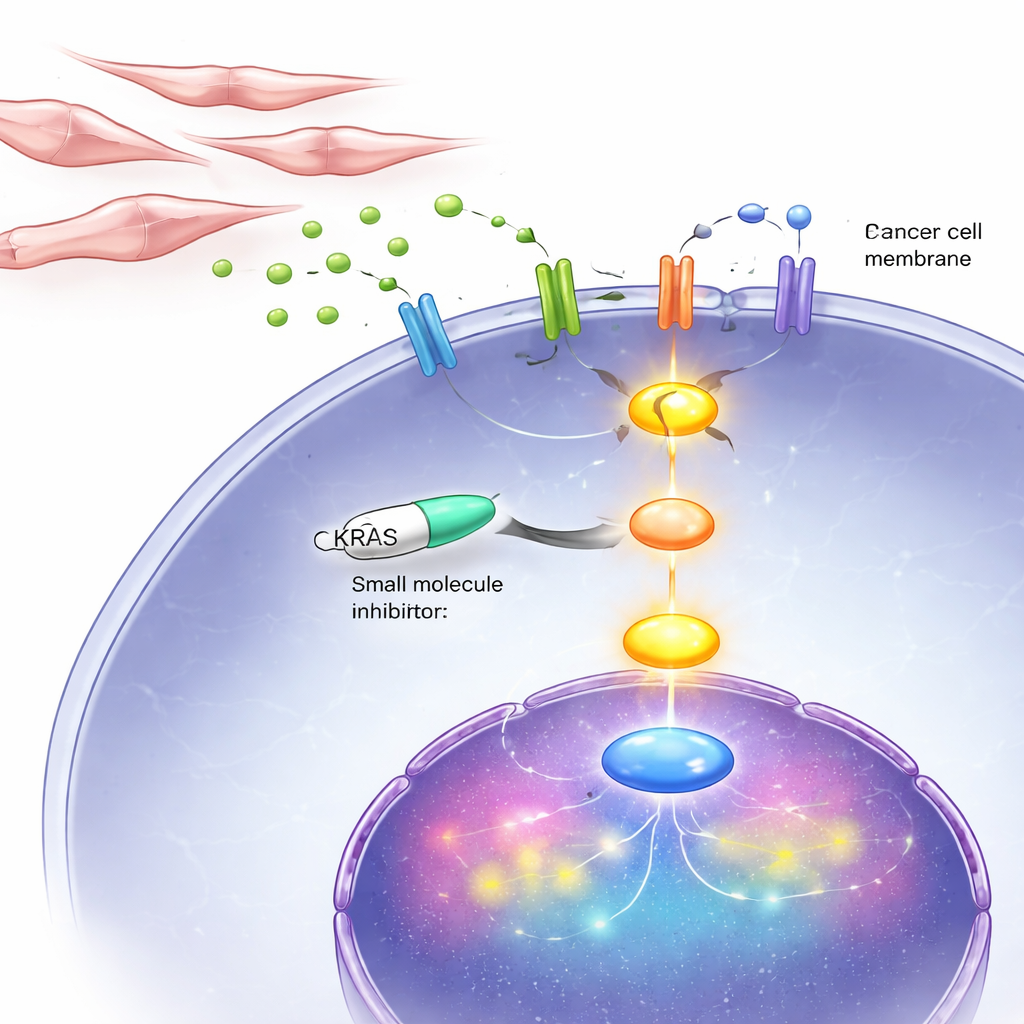
Блокирование «линии жизни» KRAS в клетках и у мышей
Поскольку этот порочный круг в конечном счёте проходит через KRAS, исследователи опробовали препарат BI-3406, который вмешивается в механизмы включения KRAS внутри клетки. В клеточных культурах этот ингибитор сильно замедлял рост и подвижность андроген-независимых клеток рака простаты, включая как клетки с аномальным KRAS, так и клетки с нормальным KRAS, активированным сигналами от фибробластов. У мышей с имплантированными опухолями, похожими на DNPC, ежедневное лечение ингибитором уменьшало объём опухолей и снижало маркеры деления клеток, одновременно усиливая признаки программируемой гибели. Важно, что препарат оказывал намного меньшее влияние на гормонозависимые раковые клетки, что подтверждает идею о том, что KRAS особенно важен на поздней, двукратно-негативной стадии.
Что это значит для будущего лечения
Для непрофессионала вывод таков: когда гормональная терапия загоняет рак простаты в угол, опухоль может уйти от неё, привлекая соседние фибробласты, которые снабжают её другим ростовым сигналом, в конечном счёте включая KRAS. Это исследование подробно картирует этот путь спасения и показывает, что прерывание сигнализации KRAS может уничтожить эти резистентные клетки в моделях. Хотя требуется дополнительная работа на пациентах, особенно с препаратами, которые безопасно блокируют KRAS или его вышестоящие помощники, результаты выделяют новую стратегию: нацеливание на цепочку CCL2–FGF8–KRAS для лечения самых стойких, гормон-независимых форм рака простаты.
Цитирование: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Ключевые слова: двукратно-негативный рак простаты, микроокружение опухоли, сигнализация KRAS, фибробласты, андроген-независимый рак