Clear Sky Science · de
Fibroblastvermittelte KRAS-Aktivierung beim doppelt-negativen Prostatakrebs
Warum diese Prostatakrebs-Studie wichtig ist
Für viele Männer halten Hormonblockaden Prostatakrebs über Jahre in Schach. Manche Tumoren kehren jedoch schließlich in einer stillen Form zurück, die nicht mehr auf Hormonmedikamente anspricht und bei üblichen Bluttests keine Signale mehr erzeugt. Diese Studie untersucht, wie diese „doppelt-negativen“ Prostatakarzinome überleben und sich ausbreiten, deckt ein verborgenes Gespräch zwischen Krebszellen und ihren umgebenden Stütz-Zellen auf und weist auf eine neue Schwachstelle hin, die künftige Medikamente ausnutzen könnten.
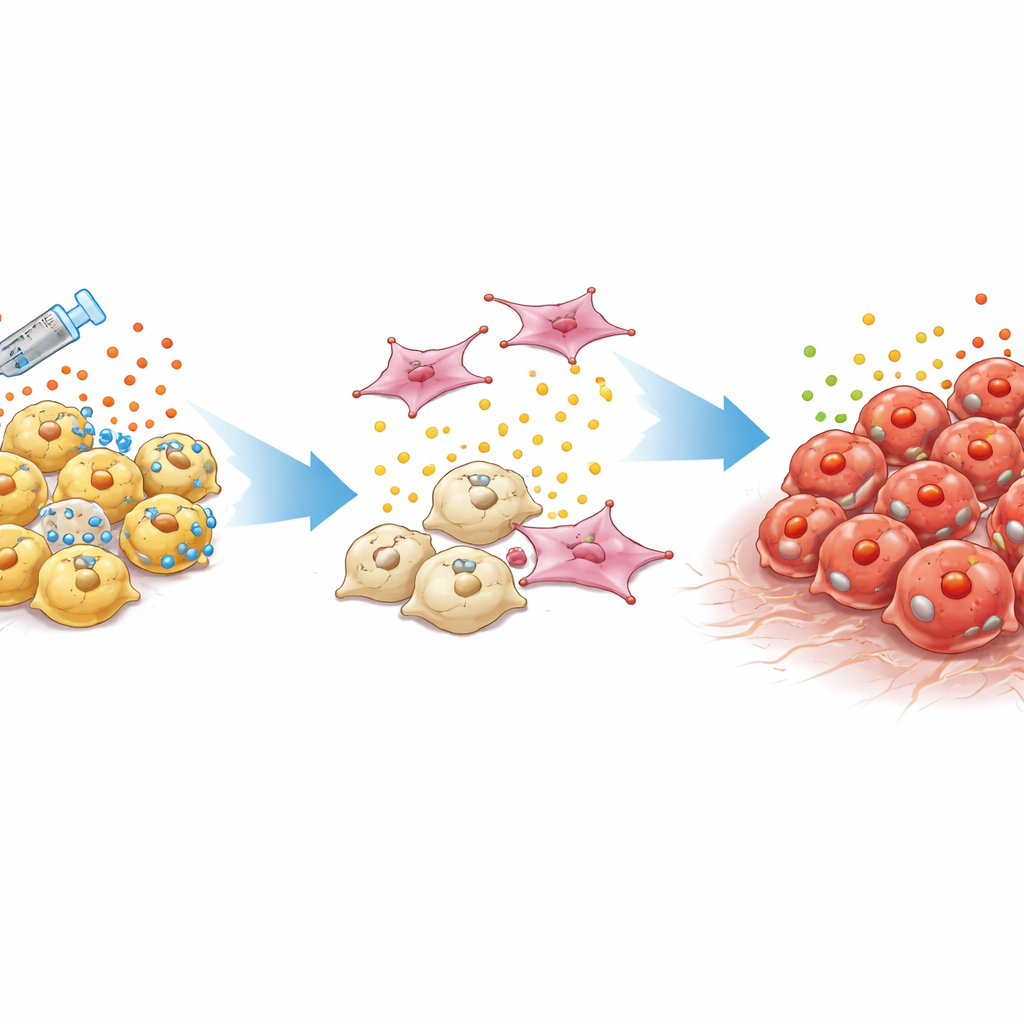
Ein schwer zu entdeckender, schwer zu behandelnder Tumortyp
Standard-Prostatakarzinome sind auf männliche Hormone angewiesen, die über ein Protein namens Androgenrezeptor wirken. Ärztinnen und Ärzte dämpfen dieses Signal mit Hormontherapie und neueren zielgerichteten Medikamenten. Mit der Zeit entwickeln sich jedoch einige Tumoren zu kastrationsresistentem Prostatakrebs, der nicht mehr auf diesen Weg angewiesen ist. Ein besonders gefährlicher Subtyp, der als doppelt-negativ bezeichnet wird, fehlt sowohl die Aktivität des Androgenrezeptors als auch Merkmale nervenähnlicher „neuroendokriner“ Zellen. Diese Tumoren wachsen oft lokal wieder oder streuen, obwohl die üblichen Marker im Blut niedrig sind, und hinterlassen Ärztinnen und Ärzten wenige Hinweise und keine etablierten Behandlungen.
Eine Wachstumsmotor, der anspringt, wenn Hormone abgeschaltet sind
Die Forschenden konzentrierten sich auf KRAS, einen bekannten molekularen Schalter, der bei Mutationen das Wachstum in Lungen‑ und Darmkrebs antreibt. Beim Prostatakrebs sind solche Mutationen selten, aber Genprofilmuster von Patientinnen und Patienten deuteten darauf hin, dass KRAS bei doppelt-negativen Fällen eine Rolle spielen könnte. Beim Vergleich verschiedener Prostatakrebszelllinien zeigte sich, dass die KRAS‑Signalgebung in hormonabhängigen Zellen kaum wirkte, aber entscheidend wurde, sobald die Zellen nicht mehr auf Androgensignale angewiesen waren. In DNPC‑ähnlichen Zellen führte eine Reduktion von KRAS zu einem starken Rückgang von Wachstum, Bewegung und Invasion, während hormon‑sensible Zellen den Verlust kaum bemerkten—was nahelegt, dass KRAS erst im späten, hormonunabhängigen Stadium zur zentralen Triebkraft wird.
Wie benachbarte Stütz-Zellen den Krebs-Schalter füttern
Tumoren sind nicht nur entartete Krebszellen; sie sind Gemeinschaften, zu denen auch Fibroblasten gehören—Bindegewebszellen, die das lokale Umfeld mitgestalten. Das Team stellte fest, dass bei Blockade der Androgensignalgebung Prostatakrebszellen die Art der Rezeptoren auf ihrer Oberfläche ändern und empfänglicher für ein Wachstumssignal namens FGF8 werden. Gleichzeitig geben die hormonentwöhnten Krebszellen ein Alarmsignal, die Chemokin CCL2, in ihre Umgebung ab. Fibroblast‑ähnliche stromale Zellen in fortgeschrittenen Prostatatumoren tragen Rezeptoren für CCL2. Wenn CCL2 diese Stromazellen erreicht, schaltet es einen internen Signalweg an, der ihre Produktion und Freisetzung von FGF8 erhöht. Dieses FGF8 gelangt dann zurück zu den Krebszellen, aktiviert deren veränderte Rezeptoren und schaltet wiederum KRAS ein, was starke Wachstums‑ und Überlebenssignale auslöst.
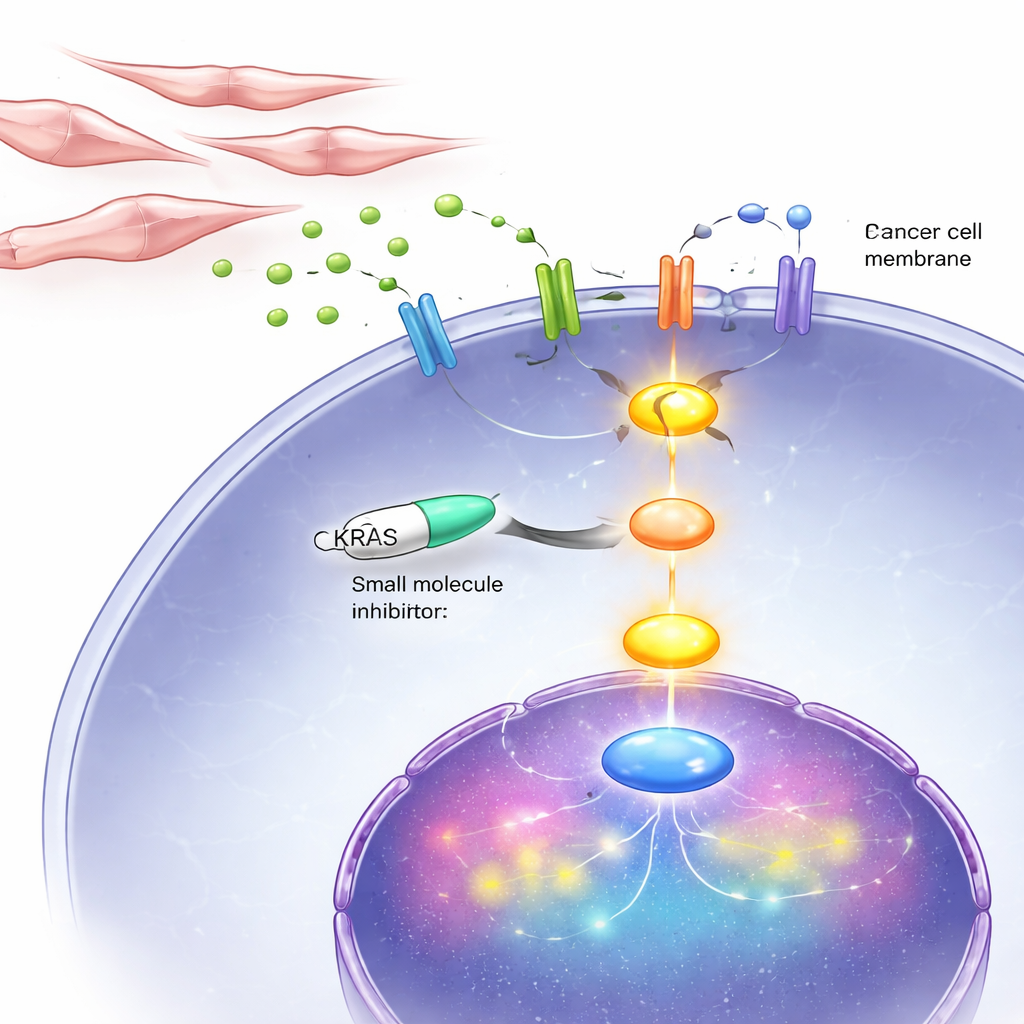
Die KRAS‑Lebensader in Zellen und Mäusen blockieren
Da dieser teuflische Kreis letztlich über KRAS läuft, testeten die Forschenden ein Medikament, BI‑3406, das die Aktivierung von KRAS in Zellen stört. In Zellkulturen verlangsamte dieser Inhibitor das Wachstum und die Bewegung androgenunabhängiger Prostatakrebszellen deutlich—einschließlich solcher mit mutiertem KRAS und solcher mit normalem KRAS, das durch Signale von Fibroblasten aktiviert wurde. Bei Mäusen mit implantierten DNPC‑ähnlichen Tumoren führte die tägliche Behandlung mit dem Inhibitor zu Tumorschrumpfung und zu weniger Markern für Zellteilung, während Hinweise auf programmierte Zellsterbeprozesse zunahmen. Wichtig ist, dass das Medikament auf hormonabhängige Krebszellen deutlich weniger Wirkung zeigte, was die Idee stützt, dass KRAS besonders kritisch im späten, doppelt-negativen Stadium ist.
Was das für zukünftige Therapien bedeutet
Für Laien lautet die Kernbotschaft: Wenn die Hormontherapie Prostatakrebs in die Enge treibt, kann der Tumor entkommen, indem er benachbarte Fibroblasten rekrutiert, die ihm ein alternatives Wachstumssignal liefern, das schließlich KRAS einschaltet. Diese Studie kartiert diese Fluchtroute detailliert und zeigt, dass das Abschneiden der KRAS‑Signalgebung resistente Zellen in Modellen töten kann. Zwar sind weitere Untersuchungen bei Patientinnen und Patienten nötig, insbesondere mit Wirkstoffen, die KRAS oder seine vorgelagerten Helfer sicher blockieren können, doch die Ergebnisse legen eine neue Strategie nahe: die Kette CCL2–FGF8–KRAS anzugreifen, um die hartnäckigsten, hormonunabhängigen Formen des Prostatakrebses zu behandeln.
Zitation: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Schlüsselwörter: doppelt-negativer Prostatakrebs, Tumormikroumgebung, KRAS-Signalgebung, Fibroblasten, androgenunabhängiger Krebs