Clear Sky Science · nl
Fibroblast-gemedieerde KRAS-activatie bij dubbel-negatieve prostaatkanker
Waarom deze prostaatkankerstudie ertoe doet
Voor veel mannen kunnen hormoonremmende behandelingen prostaatkanker jarenlang onder controle houden. Toch keren sommige tumoren uiteindelijk terug in een sluipende vorm die niet langer op hormoonmiddelen reageert en die de gebruikelijke bloedtests niet activeert. Deze studie onderzoekt hoe deze "dubbel-negatieve" prostaatkankers leven en zich verspreiden, onthult een verborgen gesprek tussen kankercellen en de omliggende steuncellen, en wijst op een nieuw kwetsbaar punt dat toekomstige geneesmiddelen mogelijk kunnen benutten.
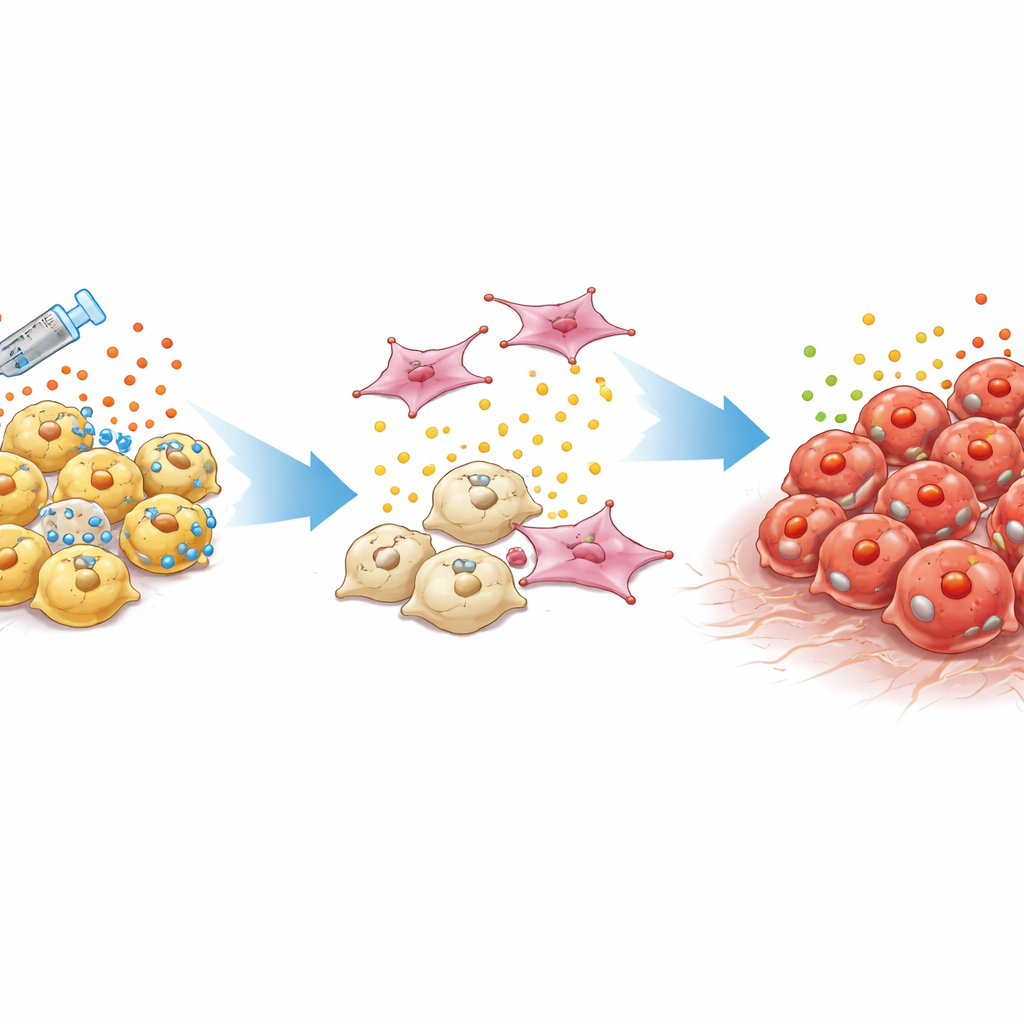
Een moeilijk te detecteren, moeilijk te behandelen tumortype
Standaard prostaatkankers zijn afhankelijk van mannelijke hormonen die werken via een eiwit genaamd de androgeenreceptor. Artsen onderdrukken dit signaal met hormoontherapie en nieuwere gerichte middelen. Na verloop van tijd evolueren sommige tumoren echter naar castratieresistente prostaatkanker die deze route niet meer nodig heeft. Een bijzonder gevaarlijke subtype, dubbel-negatieve prostaatkanker, ontbreekt zowel androgeenreceptoractiviteit als kenmerken van zenuwachtige “neuro-endocriene” cellen. Deze tumoren groeien vaak lokaal terug of verspreiden zich ondanks lage niveaus van de gebruikelijke markers in bloedtests, waardoor clinici weinig aanwijzingen en geen bewezen behandelingen hebben.
Een groeimotor die aanslaat wanneer hormonen zijn uitgeschakeld
De onderzoekers concentreerden zich op KRAS, een bekend moleculair schakelaartje dat groei aanjaagt in long- en darmkankers wanneer het gemuteerd is. Bij prostaatkanker zijn zulke mutaties zeldzaam, maar DNA-profielen van patiënten suggereerden dat KRAS betrokken kan zijn bij dubbel-negatieve gevallen. Door verschillende prostaatkankercellijnen te vergelijken, vonden ze dat KRAS-signaaloverdracht weinig deed in hormoonafhankelijke cellen maar cruciaal werd zodra cellen niet langer op androgeensignalen vertrouwden. In DNPC-achtige cellen verminderde het terugschakelen van KRAS hun vermogen om te groeien, te bewegen en in te dringen sterk, terwijl hormoongevoelige cellen het verlies nauwelijks merkten—wat suggereert dat KRAS alleen in de late, hormoononafhankelijke fase een sleutelrol speelt.
Hoe nabijgelegen steuncellen de kankerschakel voeden
Tumoren zijn niet alleen losgeslagen kankercellen; het zijn gemeenschappen die fibroblasten omvatten—bindweefselcellen die de lokale omgeving helpen vormgeven. Het team ontdekte dat wanneer androgeensignaal in prostaatkankercellen wordt geblokkeerd, de kankercellen het type receptoren op hun oppervlak veranderen en gevoeliger worden voor een groeisignaal genaamd FGF8. Tegelijk geven de hormoonuitgehongerde kankercellen een noodsignaal, de chemokine CCL2, af in hun omgeving. Fibroblastachtige stromale cellen in gevorderde prostaattumoren dragen receptoren voor CCL2. Wanneer CCL2 deze stromale cellen bereikt, zet het een interne route aan die hun productie en afgifte van FGF8 opvoert. Dat FGF8 keert vervolgens terug naar de kankercellen, activeert hun gewijzigde receptoren en schakelt op zijn beurt KRAS aan, wat krachtige groeivoorzieningen en overlevingssignalen aandrijft.
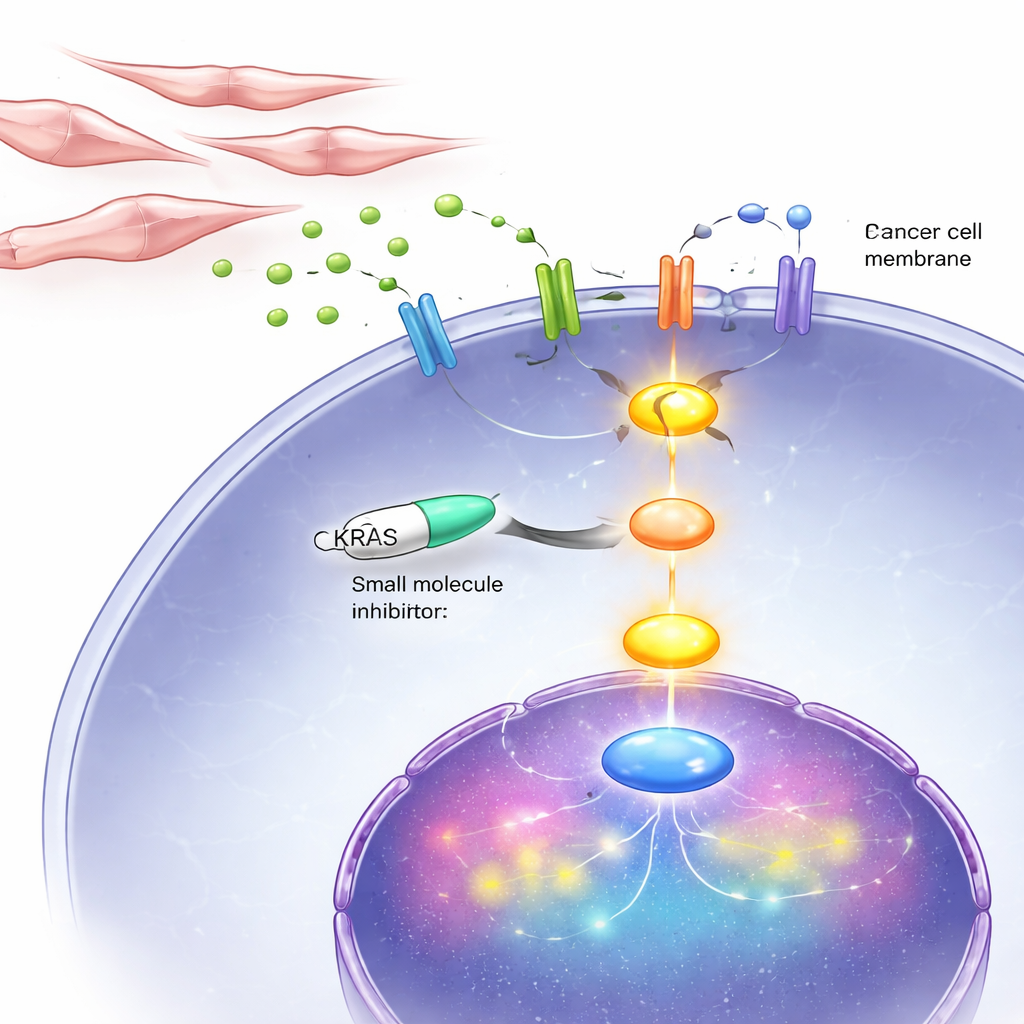
De KRAS-levenslijn blokkeren in cellen en muizen
Aangezien deze vicieuze cirkel uiteindelijk via KRAS loopt, testten de onderzoekers een middel, BI-3406, dat ingrijpt in hoe KRAS in cellen wordt aangezet. In laboratoriumschalen vertraagde deze remmer sterk de groei en beweging van androgenonafhankelijke prostaatkankercellen, inclusief die met abnormale KRAS en die met normale KRAS die door signalen van fibroblasten werden geactiveerd. Bij muizen met ingeplante DNPC-achtige tumoren kromp dagelijkse behandeling met de remmer de tumoren en verminderde markers voor celdeling, terwijl tekenen van geprogrammeerde celdood toenamen. Belangrijk is dat het middel veel minder effect had op hormoonafhankelijke kankercellen, wat het idee weerspiegelt dat KRAS vooral kritisch is in het late, dubbel-negatieve stadium.
Wat dit betekent voor toekomstige behandelingen
Voor een leek is de conclusie dat wanneer hormoontherapie prostaatkanker in het nauw brengt, de tumor kan ontsnappen door nabijgelegen fibroblasten te rekruteren die het een ander groeisignaal voeren dat uiteindelijk KRAS activeert. Deze studie brengt die ontsnappingsroute nauwgezet in kaart en laat zien dat het afsnijden van KRAS-signaaloverdracht deze resistente cellen in modellen kan doden. Hoewel er meer werk nodig is bij patiënten, met name met middelen die veilig KRAS of zijn upstream-helper(s) kunnen blokkeren, benadrukken de bevindingen een nieuwe strategie: het richten op de CCL2–FGF8–KRAS-keten om de hardnekkigste, hormoononafhankelijke vormen van prostaatkanker te behandelen.
Bronvermelding: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Trefwoorden: dubbel-negatieve prostaatkanker, tumormicro-omgeving, KRAS-signaaloverdracht, fibroblasten, androgenonafhankelijke kanker