Clear Sky Science · he
הפעלה של KRAS בתיווך פיברובלסטים בסרטן ערמונית דו-שלילי
מדוע המחקר הזה על סרטן הערמונית חשוב
בעבור גברים רבים, טיפולים החוסמים הורמונים יכולים לשלוט בסרטן הערמונית למשך שנים. עם זאת, חלק מהגידולים בסופו של דבר חוזרים בצורת שטה שאינה מגיבה יותר לתרופות הורמונליות ואינה מתגלה בבדיקות הדם הרגילות. המחקר חוקר כיצד סרטן ערמונית "דו-שלילי" שכזה שורד ומתפשט, וחושף שיחה נסתרת בין תאי הסרטן לתאי התמיכה שבסביבתם — ומצביע על נקודת תורפה חדשה שאולי ניתן יהיה לנצל בפיתוח תרופות עתידיות.
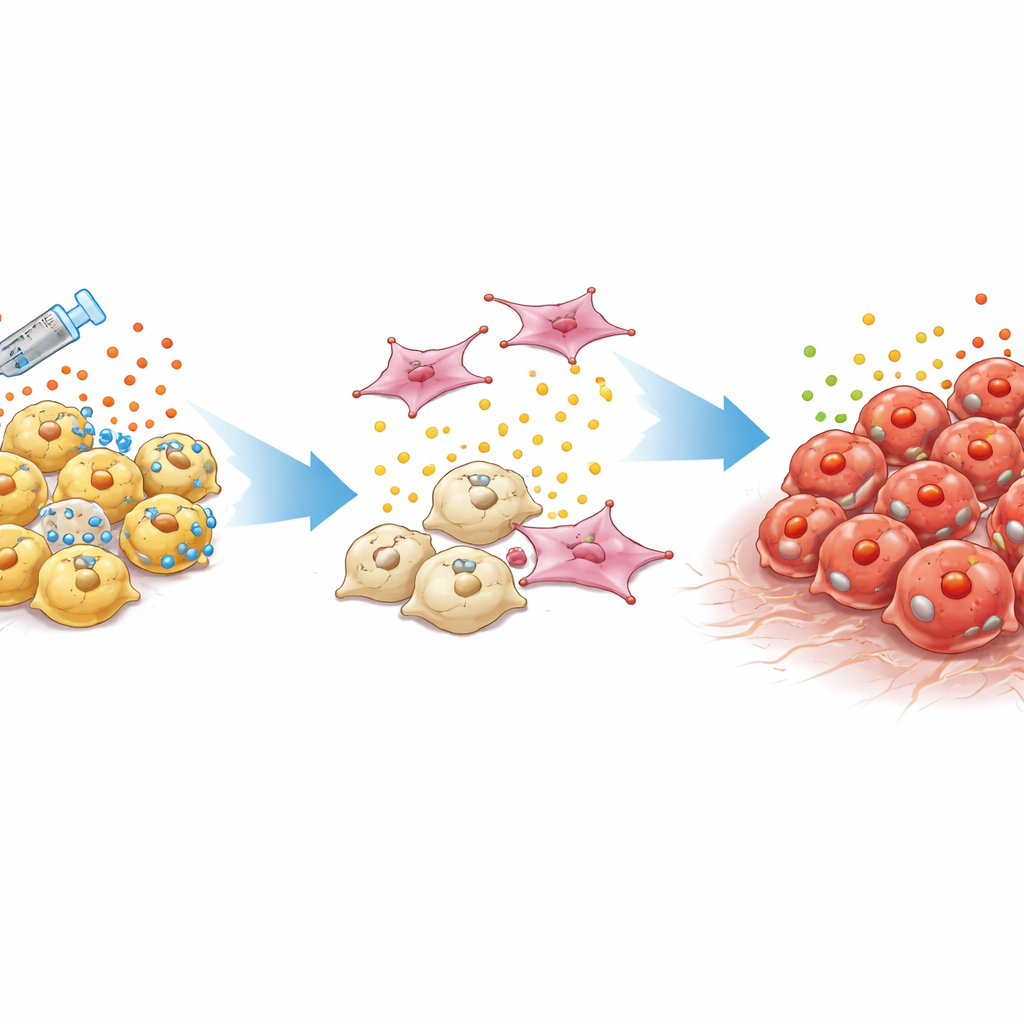
סוג גידול שקשה לאתרו ולטפל בו
סרטן הערמונית הסטנדרטי תלוי בהורמוני מין זכריים הפועלים דרך חלבון שנקרא קולטן אנדרוגן. רופאים מדכאים אותות אלה באמצעות טיפול הורמונלי ותרופות ממוקדות חדשות. עם הזמן, לעומת זאת, חלק מהגידולים מתפתחים לסרטן ערמונית עמיד לקסטראציה שאינו תלוי עוד במסלול זה. תת-סוג מסוכן במיוחד, שנקרא סרטן ערמונית דו-שלילי, חסר גם פעילות של קולטני אנדרוגן וגם תכונות של תאי "נוירואנדוקרין" דמויי עצב. גידולים אלה לעתים גדלים מחדש באופן מקומי או מתפשטים למרות רמות נמוכות של הסמנים הרגילים בבדיקות הדם, מה שמשאיר לרופאים מעט רמזים וללא טיפולים מבוססים.
מנוע גדילה שמיד נדלק כשהורמונים מושתקים
החוקרים התמקמו ב-KRAS, מתג מולקולרי ידוע שמניע גדילה בסרטן ריאה וסרטן המעי כשיש בו מוטציות. בסרטן הערמונית, מוטציות כאלה נדירות, אך מיפוי DNA של חולים רמז ש-KRAS עשוי להיות מעורב במקרים דו-שליליים. בהשוואה בין קווי תאי סרטן ערמונית שונים, הם מצאו שאותות KRAS כמעט אינם פעילים בתאים התלויים בהורמונים אך הופכים לשימושיים במיוחד כשהתאים כבר לא תלויים באותות אנדרוגן. בתאים בדמיון ל-DNPC, הקטנת פעילות KRAS חתכה באופן חדה את היכולת שלהם לגדול, לנוע ולחדור רקמות, בעוד שהתאים הרגישים להורמונים כמעט ולא הושפעו — דבר המרמז ש-KRAS הופך למנוע מרכזי רק בשלב המאוחר, הבלתי תלוי בהורמונים.
כיצד תאי התמיכה הקרובים מזינים את מתג הסרטן
גידולים אינם רק תאים סרטניים תוקפניים; הם קהילות שכוללות פיברובלסטים — תאי רקמת חיבור המסייעים לעיצוב הסביבה המקומית. הקבוצה גילתה שכאשר האות האנדרוגני נחסם בתאי סרטן הערמונית, תאי הסרטן משנים את סוגי הקולטנים שהם מציגים על פני השטח והופכים לרגישים יותר לאות גדילה בשם FGF8. במקביל, תאי הסרטן הרעבים להורמונים משחררים אות מצוקה — הכימוקין CCL2 — לסביבתם. תאי עיבוי דמויי פיברובלסט בגידולים מתקדמים נושאים קולטנים ל-CCL2. כאשר CCL2 מגיע לתאים stromal אלה, הוא מפעיל מסלול פנימי שמגביר את הייצור והשחרור שלהם של FGF8. אותו FGF8 חוזר לתאי הסרטן, מפעיל את הקולטנים המשונויים שלהם ובתמורה מדליק את KRAS, מה שמניע אותות חזקים של גדילה והישרדות.
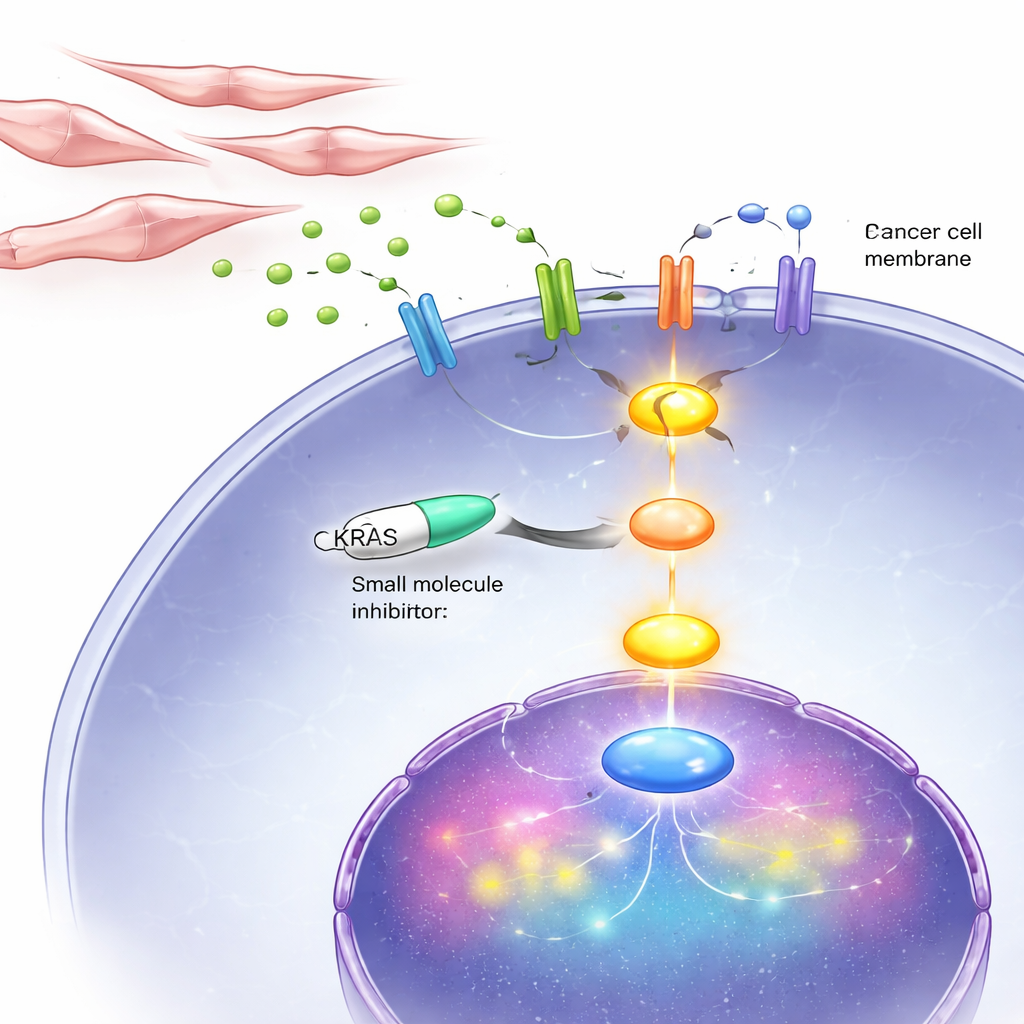
חסימת קו התמיכה של KRAS בתאים ובעכברים
מכיוון שהמעגל המזיק הזה מתרכז בסופו של דבר סביב KRAS, החוקרים בדקו תרופה, BI-3406, המעכבת את האופן שבו KRAS נדלק בתוך התאים. במעבדה, המעכב האט באופן משמעותי את הצמיחה והתנועה של תאי סרטן ערמונית בלתי תלויים באנדרוגן, כולל כאלה עם KRAS חריג ואלו עם KRAS תקין שהופעל על ידי אותות מהפיברובלסטים. בעכברים שקיבלו השתלה של גידולים בדמיון ל-DNPC, טיפול יומי באותו מעכב הקטן את נפח הגידולים והפחית סמנים של חלוקה תאית, בעוד שהוא הגביר סימנים של מוות תאי מתוכנת. חשוב לציין שהתרופה השפיעה הרבה פחות על תאים התלויים בהורמונים, דבר שמחזיר את הרעיון ש-KRAS קריטי במיוחד בשלב המאוחר, הדו-שלילי.
מה משמעות הממצא לטיפול עתידי
ללהבין בשפה פשוטה: כשהטיפול ההורמונלי דוחק את סרטן הערמונית לפינה, הגידול עלול להימלט על ידי גיוס פיברובלסטים סמוכים כדי להזין אותו באות גדילה שונה שבסופו של דבר מדליקה את KRAS. המחקר ממפה את נתיב המילוט הזה בפירוט ומראה שניתן להרוג תאים עמידים אלה במודלים על ידי חיתוך האותות דרך KRAS. בעוד שדרוש עוד מחקר בחולים, במיוחד עם תרופות שיכולות לחסום בבטחה את KRAS או את העוזרים שלו מעלה בזרם, הממצאים מדגישים אסטרטגיה חדשה: לכוון את שרשרת CCL2–FGF8–KRAS לטיפול בצורות הקשות והבלתי תלויות בהורמונים של סרטן הערמונית.
ציטוט: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
מילות מפתח: סרטן ערמונית דו-שלילי, מיקרו-סביבת הגידול, אותות KRAS, פיברובלסטים, סרטן בלתי תלוי באנדרוגן