Clear Sky Science · it
Attivazione di KRAS mediata dai fibroblasti nel cancro prostatico doppio-negativo
Perché questo studio sul cancro prostatico è importante
Per molti uomini, le terapie che bloccano gli ormoni possono mantenere il cancro prostatico sotto controllo per anni. Tuttavia, alcuni tumori alla fine ricompaiono in una forma insidiosa che non risponde più ai farmaci ormonali e non dà i soliti segnali nei test del sangue. Questo studio esplora come questi cancri “doppio-negativi” rimangono vivi e si diffondono, rivelando una conversazione nascosta tra le cellule tumorali e le cellule di supporto circostanti — e indicando un nuovo punto debole che farmaci futuri potrebbero sfruttare.
Un tipo di tumore difficile da rilevare e da trattare
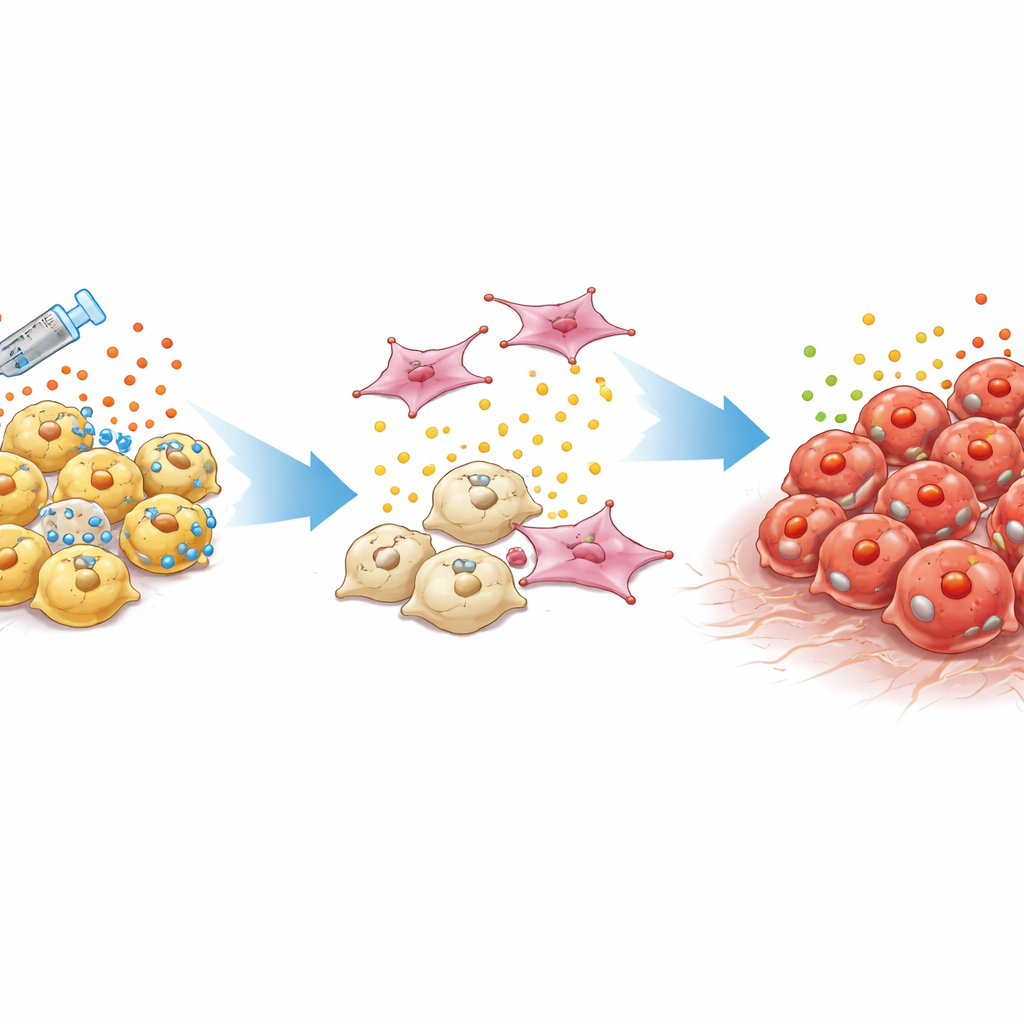
I normali carcinomi prostatici dipendono dagli ormoni maschili che agiscono attraverso una proteina chiamata recettore degli androgeni. I medici sopprimono questo segnale con la terapia ormonale e con farmaci mirati più recenti. Col tempo, però, alcuni tumori evolvono in cancro prostatico resistente alla castrazione che non si affida più a questa via. Un sottotipo particolarmente pericoloso, chiamato cancro prostatico doppio-negativo, è privo sia dell’attività del recettore degli androgeni sia delle caratteristiche delle cellule “neuroendocrine” simili a neuroni. Questi tumori spesso ricrescono localmente o si diffondono nonostante i bassi livelli dei marcatori abituali nei test del sangue, lasciando i clinici con pochi indizi e senza trattamenti consolidati.
Un motore di crescita che si accende quando gli ormoni vengono spenti
I ricercatori si sono concentrati su KRAS, un noto interruttore molecolare che guida la crescita in tumori polmonari e del colon quando è mutato. Nel cancro prostatico tali mutazioni sono rare, ma il profilo del DNA dei pazienti suggeriva che KRAS potesse essere coinvolto nei casi doppio-negativi. Confrontando diverse linee cellulari di cancro prostatico, hanno scoperto che la segnalazione KRAS aveva poco effetto nelle cellule dipendenti dagli ormoni ma diventava cruciale una volta che le cellule non dipendevano più dai segnali androgenici. Nelle cellule simili a DNPC, ridurre KRAS ha drasticamente ridotto la loro capacità di crescere, muoversi e invadere, mentre le cellule sensibili agli ormoni hanno risentito appena della perdita — il che suggerisce che KRAS diventa un motore chiave solo nello stadio tardivo, indipendente dagli ormoni.
Come le cellule di supporto vicine alimentano l’interruttore del cancro
I tumori non sono soltanto cellule tumorali canaglia; sono comunità che comprendono fibroblasti — cellule del tessuto connettivo che modellano l’ambiente locale. Il team ha scoperto che quando la segnalazione degli androgeni è bloccata nelle cellule tumorali prostatiche, queste cambiano il tipo di recettori che espongono sulla loro superficie, diventando più ricettive a un segnale di crescita chiamato FGF8. Allo stesso tempo, le cellule tumorali private di ormoni rilasciano un segnale di allarme, la chemochina CCL2, nell’ambiente circostante. Le cellule stromali di tipo fibroblastico nei tumori prostatici avanzati portano recettori per CCL2. Quando CCL2 raggiunge queste cellule stromali, attiva una via interna che aumenta la loro produzione e il rilascio di FGF8. Quell’FGF8 quindi ritorna alle cellule tumorali, attiva i loro recettori modificati e a sua volta accende KRAS, scatenando potenti segnali di crescita e sopravvivenza.
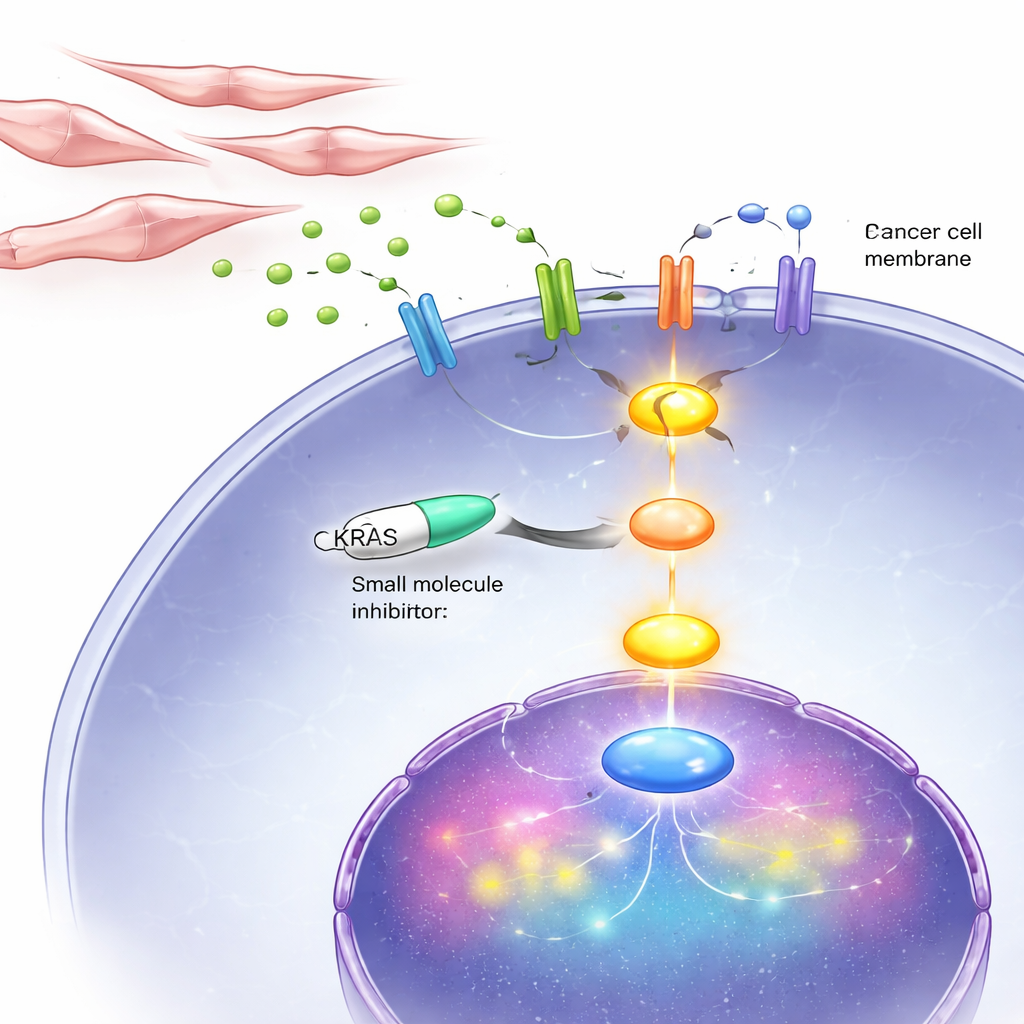
Bloccare la linea di vita KRAS in cellule e topi
Poiché questo circolo vizioso sfocia infine in KRAS, i ricercatori hanno testato un farmaco, BI-3406, che interferisce con il modo in cui KRAS viene attivato all’interno delle cellule. In colture cellulari, questo inibitore ha rallentato fortemente la crescita e il movimento delle cellule di cancro prostatico indipendenti dagli ormoni, incluse quelle con KRAS anomalo e quelle con KRAS normale attivato dai segnali dei fibroblasti. In topi impiantati con tumori simili a DNPC, il trattamento quotidiano con l’inibitore ha ridotto le dimensioni dei tumori e i marcatori della divisione cellulare, aumentando al contempo i segni di morte cellulare programmata. È importante che il farmaco abbia avuto molto meno impatto sulle cellule tumorali dipendenti dagli ormoni, ribadendo l’idea che KRAS è particolarmente critico nello stadio tardivo doppio-negativo.
Cosa significa per i trattamenti futuri
Per un lettore non specialistico, la conclusione è che quando la terapia ormonale mette il cancro prostatico all’angolo, il tumore può scappare reclutando i fibroblasti vicini per alimentarlo con un segnale di crescita diverso che alla fine accende KRAS. Questo studio mappa quel percorso di fuga in dettaglio e dimostra che tagliare la segnalazione KRAS può uccidere queste cellule resistenti nei modelli sperimentali. Pur essendo necessari ulteriori studi nei pazienti, in particolare con farmaci che possano bloccare in sicurezza KRAS o i suoi attivatori a monte, i risultati evidenziano una nuova strategia: mirare alla catena CCL2–FGF8–KRAS per trattare le forme più ostinate e indipendenti dagli ormoni del cancro prostatico.
Citazione: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Parole chiave: cancro prostatico doppio-negativo, microambiente tumorale, segnalizzazione KRAS, fibroblasti, cancro indipendente dagli ormoni