Clear Sky Science · pl
Aktywacja KRAS przez fibroblasty w podwójnie negatywnym raku prostaty
Dlaczego to badanie raka prostaty ma znaczenie
Dla wielu mężczyzn terapie blokujące hormony mogą utrzymywać raka prostaty pod kontrolą przez lata. Jednak niektóre guzy w końcu powracają w podstępnej postaci, która przestaje reagować na leki hormonalne i nie powoduje typowych zmian w badaniach krwi. To badanie bada, jak te „podwójnie negatywne” raki prostaty przeżywają i się rozprzestrzeniają, ujawniając ukrytą rozmowę między komórkami nowotworowymi a otaczającymi je komórkami wspierającymi — i wskazując nowe słabe miejsce, które mogą wykorzystać przyszłe leki.
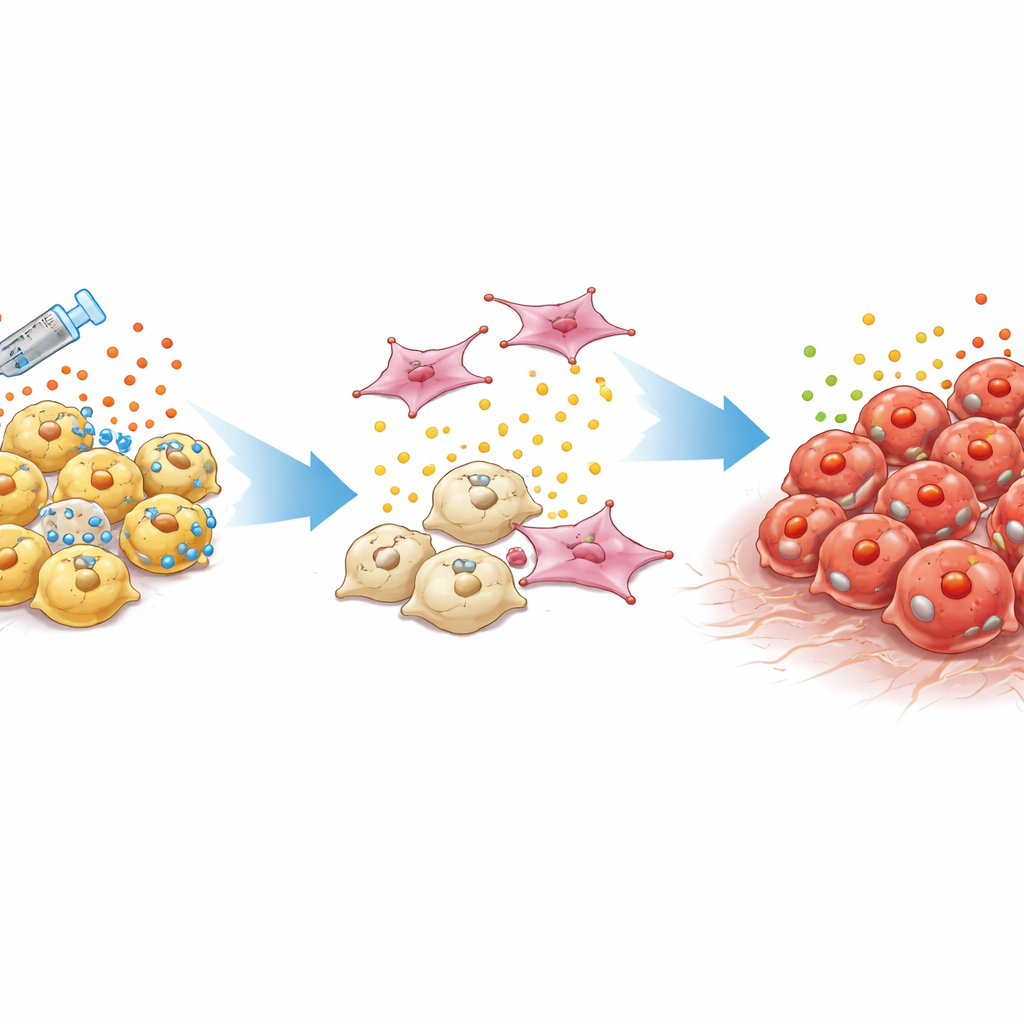
Trudny do wykrycia, trudny w leczeniu typ guza
Standardowe raki prostaty zależą od męskich hormonów działających przez białko zwane receptorem androgenowym. Lekarze tłumią ten sygnał terapią hormonalną i nowszymi lekami celowanymi. Z czasem jednak niektóre guzy przekształcają się w rak prostaty odporny na kastrację, który nie polega już na tej ścieżce. Szczególnie niebezpieczny podtyp, nazywany podwójnie negatywnym rakiem prostaty, nie wykazuje ani aktywności receptora androgenowego, ani cech komórek „neuroendokrynnych”. Te guzy często odrastają lokalnie lub dają przerzuty mimo niskich poziomów zwykłych markerów we krwi, pozostawiając klinicystów bez wyraźnych wskazówek i bez sprawdzonych terapii.
Silnik wzrostu, który włącza się, gdy hormony są zablokowane
Naukowcy skupili się na KRAS, dobrze znanym molekularnym przełączniku napędzającym wzrost w raku płuca i jelita grubego, gdy jest zmutowany. W raku prostaty takie mutacje są rzadkie, ale profilowanie DNA pacjentów sugerowało, że KRAS może mieć rolę w przypadkach podwójnie negatywnych. Porównując różne linie komórkowe raka prostaty, stwierdzili, że sygnalizacja KRAS odgrywała niewielką rolę w komórkach zależnych od hormonów, lecz stawała się kluczowa, gdy komórki przestały polegać na sygnałach androgenowych. W komórkach podobnych do DNPC obniżenie aktywności KRAS gwałtownie zmniejszało ich zdolność do wzrostu, migracji i inwazji, podczas gdy komórki wrażliwe na hormony prawie nie odczuwały tej utraty — co sugeruje, że KRAS staje się ważnym silnikiem dopiero w późnym, niezależnym od hormonów stadium.
Jak pobliskie komórki wspierające zasilają przełącznik nowotworu
Guzy to nie tylko złośliwe komórki nowotworowe; to społeczności, które obejmują fibroblasty — komórki tkanki łącznej kształtujące lokalne środowisko. Zespół odkrył, że gdy w komórkach raka prostaty blokowane jest sygnalizowanie androgenowe, komórki nowotworowe zmieniają rodzaj receptorów występujących na swojej powierzchni, stając się bardziej podatne na sygnał wzrostu zwany FGF8. Równocześnie komórki pozbawione hormonów uwalniają sygnał alarmowy — chemokinę CCL2 — do otoczenia. Komórki zrębu podobne do fibroblastów w zaawansowanych guzach prostaty mają receptory dla CCL2. Gdy CCL2 dociera do tych komórek zrębu, uruchamia wewnętrzną ścieżkę, która zwiększa ich produkcję i wydzielanie FGF8. Ten FGF8 wraca następnie do komórek nowotworowych, aktywuje ich zmienione receptory i w konsekwencji włącza KRAS, napędzając silne sygnały wzrostu i przeżycia.
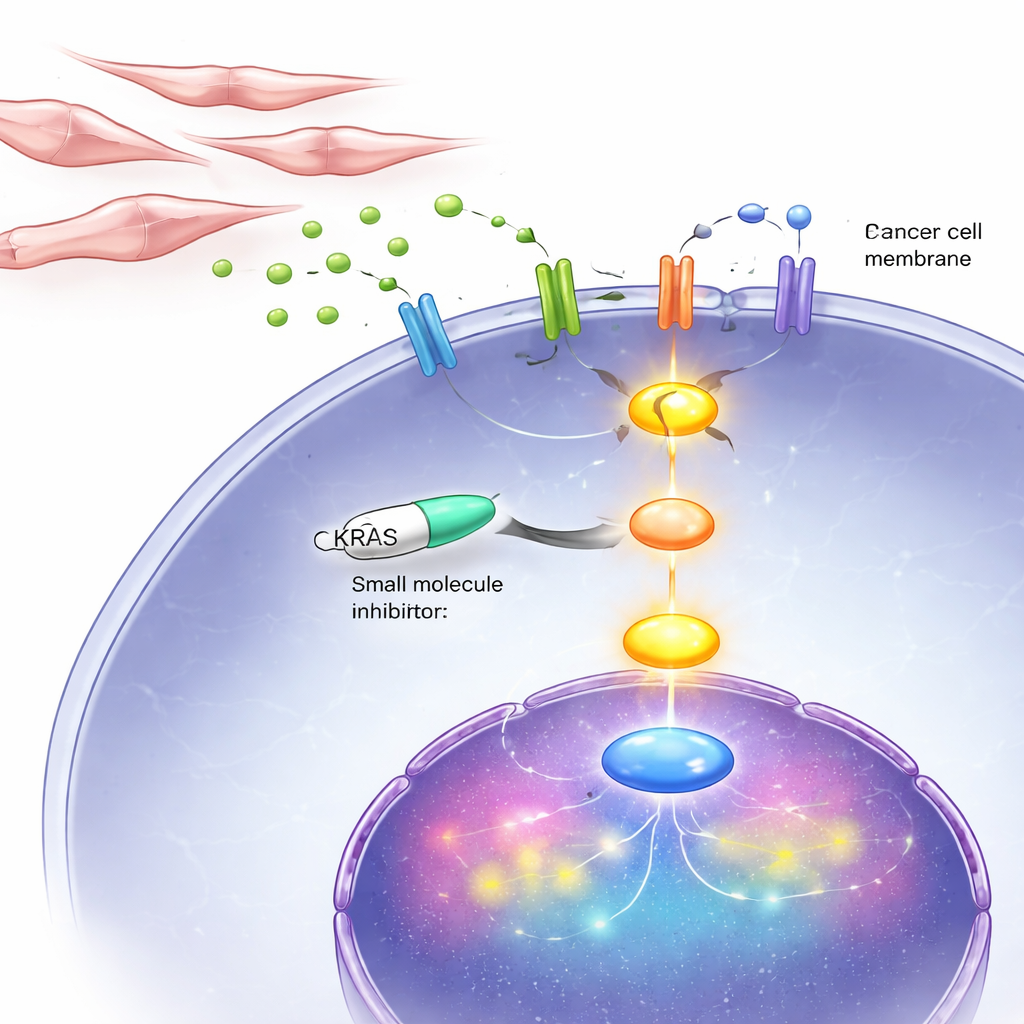
Blokowanie życiowej linii KRAS w komórkach i u myszy
Ponieważ ten błędny cykl ostatecznie przepływa przez KRAS, badacze przetestowali lek BI-3406, który zakłóca sposób aktywacji KRAS wewnątrz komórek. W hodowlach laboratoryjnych ten inhibitor silnie spowalniał wzrost i migrację komórek raka prostaty niezależnych od androgenów, w tym tych z nieprawidłowym KRAS oraz tych z prawidłowym KRAS aktywowanym przez sygnały z fibroblastów. U myszy wszczepionych guzami podobnymi do DNPC codzienne podawanie inhibitora zmniejszyło wielkość guzów i obniżyło markery podziału komórkowego, jednocześnie zwiększając oznaki zaprogramowanej śmierci komórek. Co istotne, lek miał znacznie mniejszy wpływ na komórki zależne od hormonów, co potwierdza ideę, że KRAS jest szczególnie krytyczny w późnym, podwójnie negatywnym stadium.
Co to oznacza dla przyszłego leczenia
Dla laika wniosek jest taki: gdy terapia hormonalna wypycha raka prostaty w róg, guz może uciec, rekrutując pobliskie fibroblasty, które dostarczają inny sygnał wzrostu, ostatecznie włączający KRAS. To badanie szczegółowo mapuje tę drogę ucieczki i pokazuje, że odcięcie sygnalizacji KRAS może zabić te odporne komórki w modelach. Choć potrzebne są dalsze badania u pacjentów, zwłaszcza nad lekami, które bezpiecznie zablokują KRAS lub jego pomocników upstream, wyniki wskazują nową strategię: celowanie w łańcuch CCL2–FGF8–KRAS w leczeniu najbardziej opornych, niezależnych od hormonów postaci raka prostaty.
Cytowanie: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Słowa kluczowe: podwójnie negatywny rak prostaty, mikrośrodowisko guza, sygnalizacja KRAS, fibroblasty, rak niezależny od androgenów