Clear Sky Science · pt
Ativação do KRAS mediada por fibroblastos no câncer de próstata duplo-negativo
Por que este estudo sobre câncer de próstata é importante
Para muitos homens, terapias que bloqueiam hormônios conseguem controlar o câncer de próstata por anos. Ainda assim, alguns tumores reaparecem numa forma sorrateira que não responde mais aos medicamentos hormonais e não dispara os testes sanguíneos usuais. Este estudo investiga como esses cânceres “duplo-negativos” permanecem vivos e se espalham, revelando uma conversa oculta entre as células cancerosas e as células de suporte ao redor — e apontando para uma nova vulnerabilidade que futuros medicamentos podem explorar.
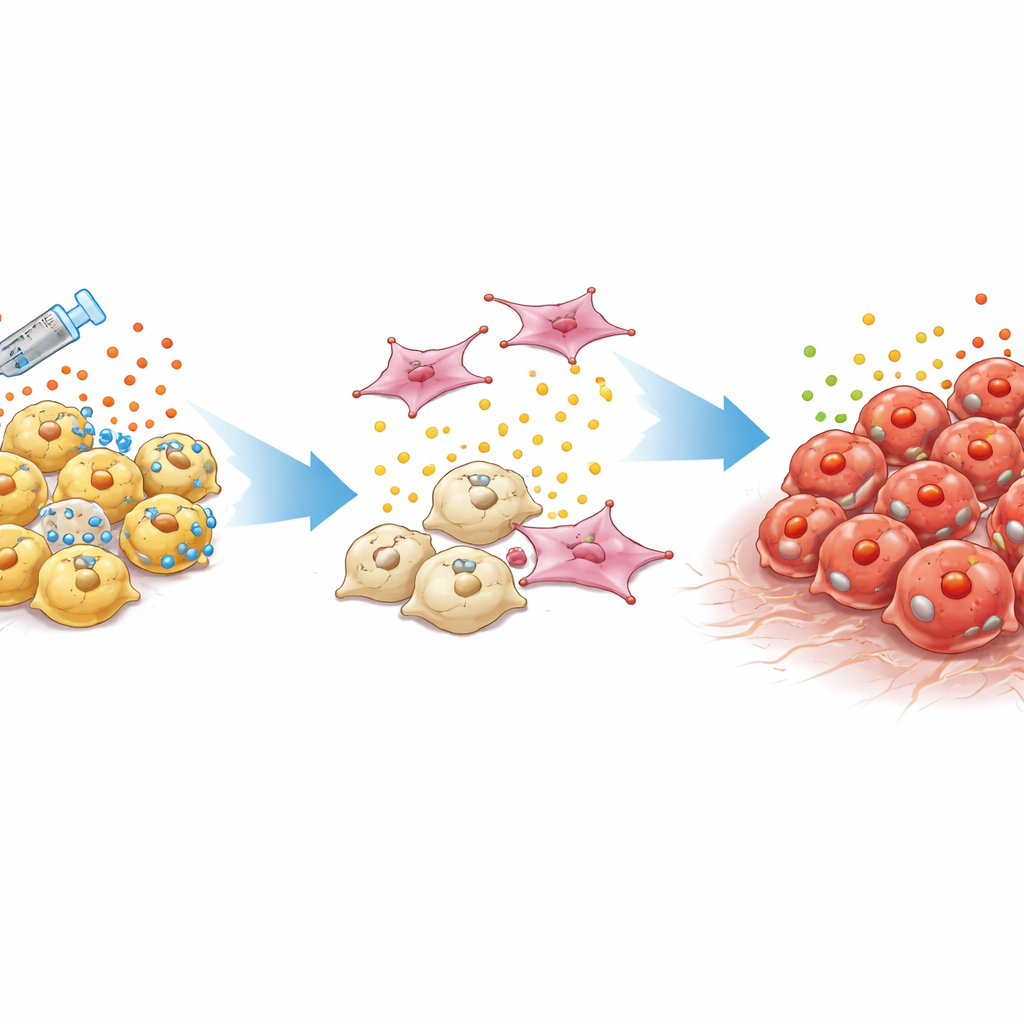
Um tipo de tumor difícil de detectar e de tratar
Os cânceres de próstata comuns dependem dos hormônios masculinos atuando por meio de uma proteína chamada receptor de andrógeno. Os médicos suprimem esse sinal com terapia hormonal e medicamentos mais recentes direcionados. Com o tempo, no entanto, alguns tumores evoluem para câncer de próstata resistente à castração que não depende mais dessa via. Um subtipo especialmente perigoso, chamado câncer de próstata duplo-negativo, carece tanto da atividade do receptor de andrógeno quanto das características de células “neuroendócrinas” semelhantes a neurônios. Esses tumores frequentemente recidivam localmente ou se espalham apesar de níveis baixos dos marcadores usuais em exames de sangue, deixando os clínicos com poucas pistas e sem tratamentos comprovados.
Um motor de crescimento que liga quando os hormônios são desligados
Os pesquisadores concentraram-se no KRAS, um comutador molecular bem conhecido que impulsiona o crescimento em cânceres de pulmão e cólon quando mutado. No câncer de próstata, tais mutações são raras, mas o perfil genético de pacientes sugeriu que o KRAS poderia estar envolvido em casos duplo-negativos. Ao comparar diferentes linhagens celulares de câncer de próstata, eles descobriram que a sinalização do KRAS era muito discreta em células dependentes de hormônio, mas tornou-se crucial quando as células não dependiam mais dos sinais de andrógeno. Em células semelhantes a DNPC, reduzir o KRAS cortou drasticamente sua capacidade de crescer, mover-se e invadir, enquanto as células sensíveis a hormônio mal perceberam a perda — sugerindo que o KRAS se torna um motor-chave apenas no estado tardio e independente de hormônio.
Como células de suporte próximas alimentam o interruptor do câncer
Os tumores não são apenas células cancerosas fora de controle; são comunidades que incluem fibroblastos — células do tecido conjuntivo que ajudam a moldar o ambiente local. A equipe descobriu que, quando a sinalização de andrógeno é bloqueada nas células de câncer de próstata, as células cancerosas mudam os tipos de receptores que exibem na superfície, tornando-se mais receptivas a um sinal de crescimento chamado FGF8. Ao mesmo tempo, as células privadas de hormônio liberam um sinal de alerta, a quimiocina CCL2, em seu entorno. Células estromais semelhantes a fibroblastos em tumores avançados de próstata carregam receptores para CCL2. Quando a CCL2 alcança essas células estromais, ela liga uma via interna que aumenta sua produção e liberação de FGF8. Esse FGF8 então retorna às células cancerosas, ativa seus receptores alterados e, por sua vez, aciona o KRAS, impulsionando sinais potentes de crescimento e sobrevivência.
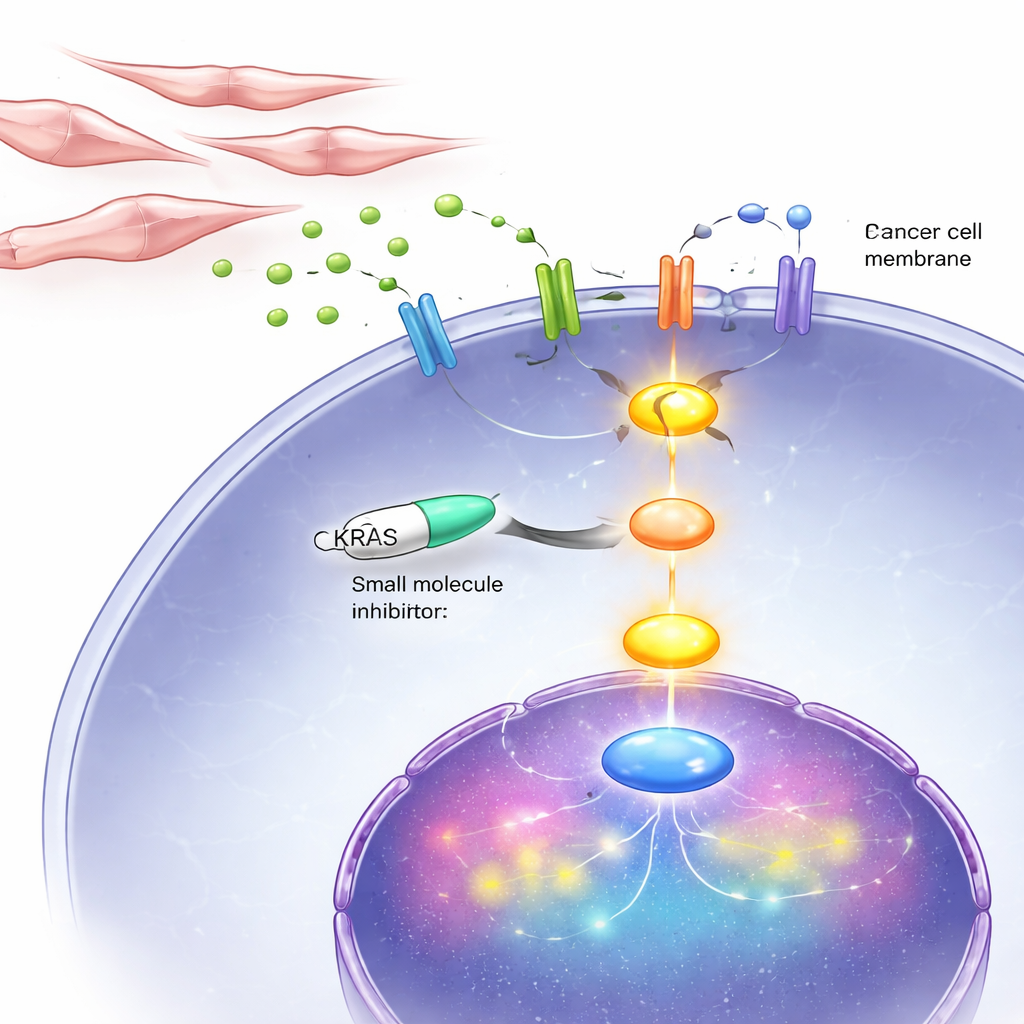
Bloqueando a linha vital do KRAS em células e em camundongos
Como esse ciclo vicioso finalmente converte-se pelo KRAS, os pesquisadores testaram um fármaco, BI-3406, que interfere na forma como o KRAS é ativado dentro das células. Em placas de cultura, esse inibidor desacelerou fortemente o crescimento e o movimento de células de câncer de próstata independentes de andrógeno, incluindo aquelas com KRAS anormal e aquelas com KRAS normal ativado por sinais de fibroblastos. Em camundongos implantados com tumores semelhantes a DNPC, o tratamento diário com o inibidor encolheu os tumores e reduziu marcadores de divisão celular, ao mesmo tempo que aumentou sinais de morte celular programada. Importante: o medicamento teve bem menos impacto em células cancerosas dependentes de hormônio, ecoando a ideia de que o KRAS é especialmente crítico na fase tardia e duplo-negativa.
O que isso significa para tratamentos futuros
Para um leigo, a conclusão é que, quando a terapia hormonal acorrenta o câncer de próstata, o tumor pode escapar recrutando fibroblastos próximos para lhe fornecer um sinal de crescimento distinto que acaba por ativar o KRAS. Este estudo mapeia essa rota de escape em detalhes e mostra que cortar a sinalização do KRAS pode matar essas células resistentes em modelos. Embora sejam necessários mais estudos em pacientes, especialmente com drogas que possam bloquear com segurança o KRAS ou seus auxiliares a montante, os achados destacam uma nova estratégia: mirar na cadeia CCL2–FGF8–KRAS para tratar as formas mais obstinadas e independentes de hormônio do câncer de próstata.
Citação: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Palavras-chave: câncer de próstata duplo-negativo, microambiente tumoral, sinalização KRAS, fibroblastos, câncer independente de andrógeno