Clear Sky Science · ar
تنشيط KRAS بواسطة الأرومات الليفية في سرطان البروستاتا العديم الثنائي
لماذا تهم هذه الدراسة عن سرطان البروستاتا
بالنسبة للعديد من الرجال، يمكن للعلاجات المانعة للهرمونات أن تحافظ على سرطان البروستاتا تحت السيطرة لسنوات. ومع ذلك، تعود بعض الأورام في نهاية المطاف بشكل خفي لم تعد تستجيب لأدوية الهرمونات ولا تُظهر علاماتها المعتادة في اختبارات الدم. تتعمق هذه الدراسة في كيفية بقاء هذه الأورام «العديمة الثنائية» حية وانتشارها، كاشفة عن حوار خفي بين خلايا السرطان والخلايا الداعمة المحيطة بها — ومشيرة إلى نقطة ضعف جديدة قد تستغلها الأدوية المستقبلية.
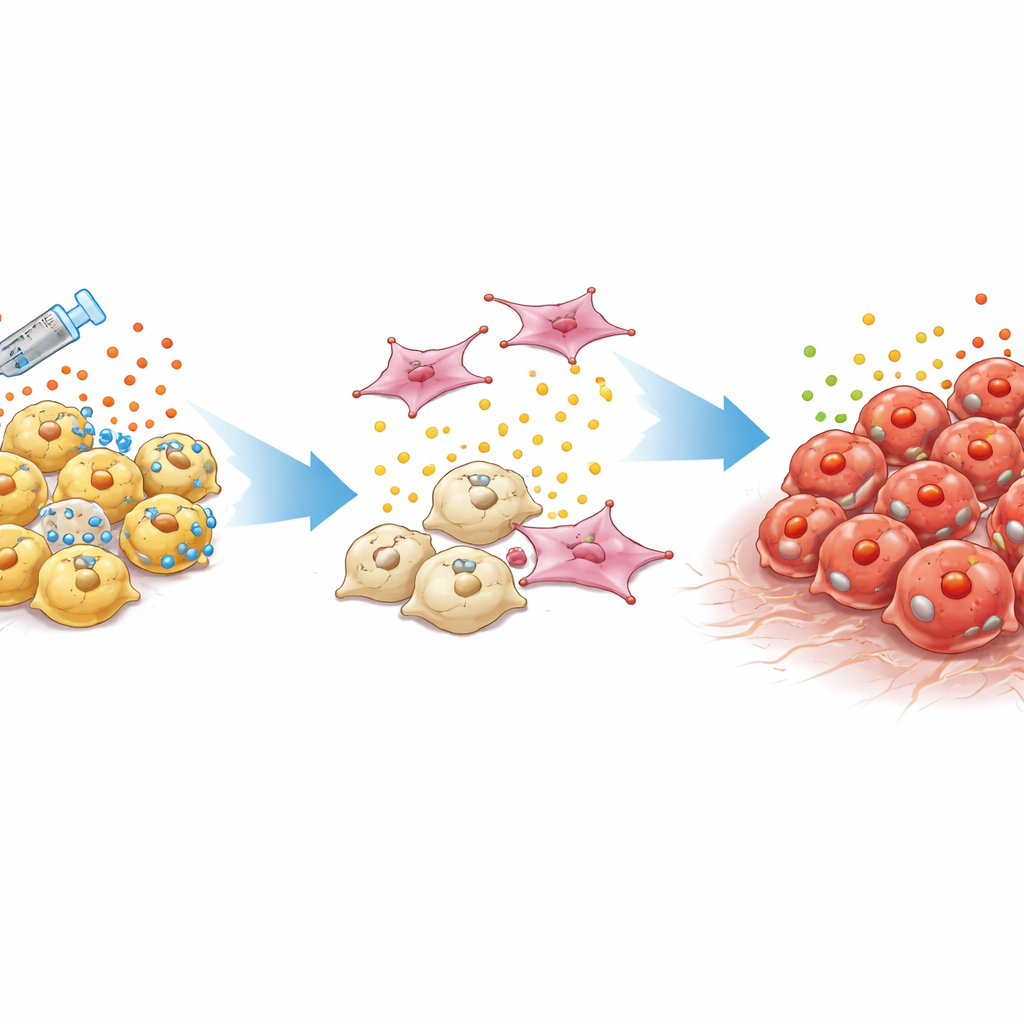
نوع ورم يصعب اكتشافه وعلاجه
تعتمد سرطانات البروستاتا التقليدية على هرمونات الذكورة التي تعمل عبر بروتين يسمى مستقبل الأندروجين. يكبت الأطباء هذا الإشارة بالعلاج الهرموني والأدوية المستهدفة الأحدث. مع مرور الوقت، تتطور بعض الأورام إلى سرطان البروستاتا المقاوم للخصي الذي لم يعد يعتمد على هذا المسار. فرع خطير بشكل خاص، يسمى سرطان البروستاتا العديم الثنائي، يفتقر إلى كل من نشاط مستقبل الأندروجين وسمات خلايا «الغدد الصم العصبية» الشبيهة بالأعصاب. غالبًا ما تنمو هذه الأورام مرة أخرى محليًا أو تنتشر رغم انخفاض مستويات العلامات المعتادة في اختبارات الدم، ما يترك الأطباء بقليل من الأدلة وبدون علاجات مثبتة.
محرك نمو يُشغل عند إيقاف الهرمونات
ركز الباحثون على KRAS، وهو مفتاح جزيئي معروف يدير النمو في سرطانات الرئة والقولون عند حدوث طفرات. في سرطان البروستاتا، نادرًا ما تُرى مثل هذه الطفرات، لكن تحليل الحمض النووي للمرضى ألمح إلى أن KRAS قد يكون له دور في حالات العديم الثنائي. بمقارنة خطوط خلايا سرطان البروستاتا المختلفة، وجدوا أن إشارة KRAS كانت ضئيلة في الخلايا المعتمدة على الهرمونات لكنها أصبحت حاسمة بمجرد أن توقفت الخلايا عن الاعتماد على إشارات الأندروجين. في الخلايا الشبيهة بالعديم الثنائي، أدى تقليل نشاط KRAS إلى خفض حاد في قدرتها على النمو والحركة والغزو، بينما كادت الخلايا الحساسة للهرمونات أن لا تتأثر بفقدانه — مما يوحي بأن KRAS يصبح محركًا رئيسيًا فقط في المرحلة المتأخرة غير المعتمدة على الهرمونات.
كيف تغذي الخلايا الداعمة المجاورة مفتاح السرطان
الأورام ليست مجرد خلايا سرطانية مارقة؛ إنها مجتمعات تشمل الأرومات الليفية — خلايا النسيج الضام التي تساعد في تشكيل البيئة المحلية. اكتشف الفريق أنه عندما يُحجب إشارة الأندروجين في خلايا سرطان البروستاتا، تغير خلايا السرطان أنواع المستقبلات التي تعرضها على سطحها، فأصبحت أكثر تقبلاً لإشارة نمو تسمى FGF8. في الوقت نفسه، تطلق خلايا السرطان المحرومة من الهرمون إشارة استغاثة، وهي الكيموكين CCL2، في محيطها. تحمل خلايا اللحمة الشبيهة بالأرومات الليفية في الأورام المتقدمة مستقبلات لـCCL2. عندما يصل CCL2 إلى هذه الخلايا اللحمة، يُشغّل مسارًا داخليًا يزيد من إنتاجها وإطلاقها لِـFGF8. ثم يعود هذا FGF8 إلى خلايا السرطان، ينشط مستقبلاتها المعدلة، وبالتالي يشغّل KRAS، مما يولد إشارات قوية للنمو والبقاء.
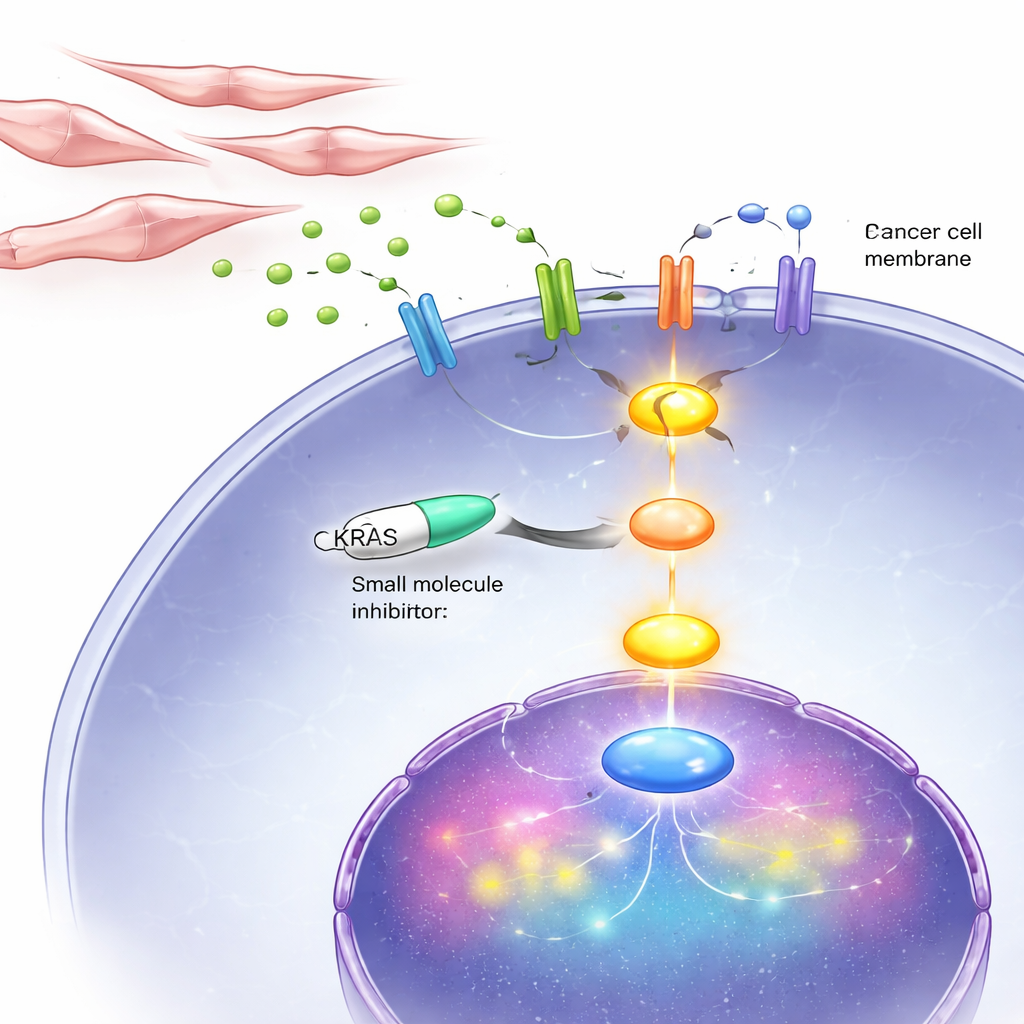
حجب شريان الحياة KRAS في الخلايا وفي الفئران
نظرًا لأن هذه الدورة الشريرة تصب في نهاية المطاف عبر KRAS، اختبر الباحثون دواءً، BI-3406، يتداخل مع كيفية تنشيط KRAS داخل الخلايا. في أطباق المختبر، أبطأ هذا المثبط بقوة نمو وحركة خلايا سرطان البروستاتا غير المعتمدة على الأندروجين، بما في ذلك تلك ذات KRAS الشاذ وتلك ذات KRAS الطبيعي المنشط بواسطة إشارات من الأرومات الليفية. في الفئران المصابة بأورام شبيهة بالعديم الثنائي، أدى العلاج اليومي بالمثبط إلى صغر حجم الأورام وتقليل علامات الانقسام الخلوي، مع زيادة دلائل الموت الخلوي المبرمج. ومن المهم أن الدواء كان له تأثير أقل بكثير على الخلايا السرطانية المعتمدة على الهرمونات، مما ينعكس الفكرة القائلة بأن KRAS له أهمية خاصة في المرحلة المتأخرة العديمية الثنائية.
ماذا يعني هذا للعلاج المستقبلي
لغير المتخصص، الخلاصة هي أن العلاج الهرموني عندما يدفع سرطان البروستاتا إلى الزاوية، يمكن للورم أن يهرب عبر تجنيد الأرومات الليفية المجاورة لتزويده بإشارة نمو مختلفة تنتهي بتشغيل KRAS. ترسم هذه الدراسة طريق الهروب هذا بتفصيل وتُظهر أن قطع إشارة KRAS يمكن أن يقتل هذه الخلايا المقاومة في النماذج المختبرية. بينما هناك حاجة إلى مزيد من العمل في المرضى، لا سيما بأدوية يمكنها حظر KRAS أو مساعديه الصاعدين بأمان، تبرز النتائج استراتيجية جديدة: استهداف سلسلة CCL2–FGF8–KRAS لعلاج أشد أشكال سرطان البروستاتا مقاومةً وغير المعتمدة على الهرمونات.
الاستشهاد: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
الكلمات المفتاحية: سرطان البروستاتا العديم الثنائي, البيئة الدقيقة للورم, إشارات KRAS, الأرومات الليفية, السرطان غير المعتمد على الأندروجين