Clear Sky Science · sv
Fibroblastmedierad KRAS-aktivering i dubbelnegativ prostatacancer
Varför den här studien om prostatacancer är viktig
För många män kan hormonblockerande behandlingar hålla prostatacancer i schack i åratal. Men vissa tumörer återkommer så småningom i en förklädd form som inte längre svarar på hormonläkemedel och som inte ger utslag i de vanliga blodproverna. Denna studie undersöker hur dessa "dubbelnegativa" prostatacancerformer överlever och sprider sig, och avslöjar en dold kommunikation mellan cancerceller och deras omgivande stödjeceller — samt pekar på en ny svag punkt som framtida läkemedel kan utnyttja.
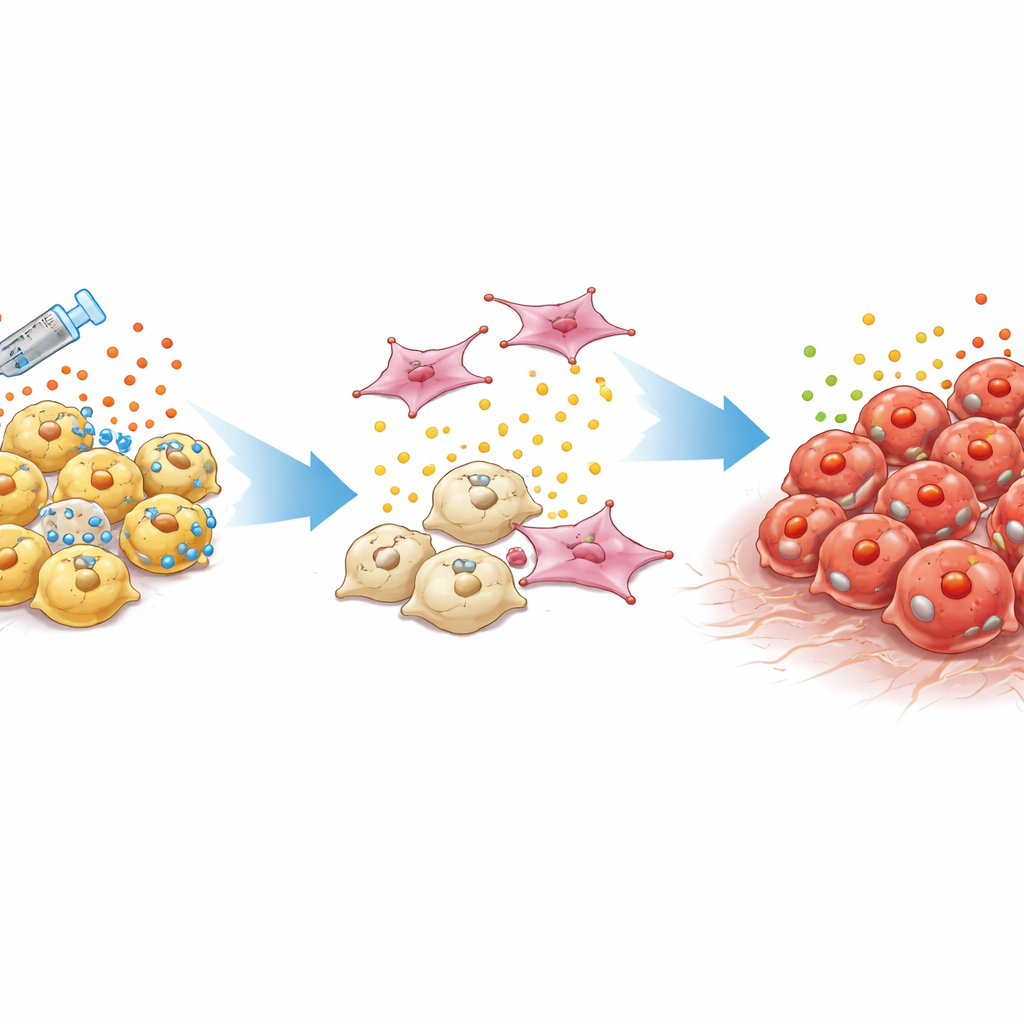
En svårupptäckt, svårbehandlad tumörtyp
Vanlig prostatacancer är beroende av manliga hormoner som verkar via ett protein som kallas androgenreceptorn. Läkare undertrycker denna signal med hormonbehandling och nyare riktade läkemedel. Med tiden utvecklas dock vissa tumörer till kastrationsresistent prostatacancer som inte längre är beroende av denna väg. En särskilt farlig undergrupp, kallad dubbelnegativ prostatacancer, saknar både androgenreceptoraktivitet och egenskaper hos nervliknande "neuroendokrina" celler. Dessa tumörer återkommer ofta lokalt eller sprider sig trots låga nivåer av de vanliga markörerna i blodet, vilket lämnar kliniker med få ledtrådar och inga etablerade behandlingar.
En tillväxtmotor som slås på när hormoner stängs av
Forskarna fokuserade på KRAS, en välkänd molekylär strömbrytare som driver tillväxt i lung- och tjocktarmscancer när den är muterad. I prostatacancer är sådana mutationer ovanliga, men patient-DNA-profilering antydde att KRAS kunde vara involverad i dubbelnegativa fall. Genom att jämföra olika prostatacancercellinjer fann de att KRAS-signalering gjorde mycket lite i hormonberoende celler men blev avgörande när cellerna inte längre var beroende av androgen signalering. I DNPC-liknande celler minskade reducering av KRAS deras förmåga att växa, röra sig och invaderas kraftigt, medan hormonkänsliga celler knappt märkte förlusten — vilket tyder på att KRAS blir en nyckelmotor först i det sena, hormonoberoende stadiet.
Hur närliggande stödjeceller matar cancerns brytare
Tumörer är inte bara avvikande cancerceller; de är samhällen som inkluderar fibroblaster — bindvävsceller som hjälper till att forma den lokala miljön. Teamet upptäckte att när androgen signalering blockeras i prostatacancerceller, ändrar cancercellerna vilka typer av receptorer de visar på sin yta och blir mer mottagliga för en tillväxtsignal kallad FGF8. Samtidigt släpper de hormonuttömda cancercellerna ut en nödsignal, kemokinen CCL2, i omgivningen. Fibroblastlika stromaceller i avancerade prostatatumörer bär receptorer för CCL2. När CCL2 når dessa stromaceller aktiverar den en intern väg som ökar deras produktion och frisättning av FGF8. Denna FGF8 återvänder sedan till cancercellerna, aktiverar deras omställda receptorer och i sin tur slår på KRAS, vilket driver starka tillväxt- och överlevnadssignaler.
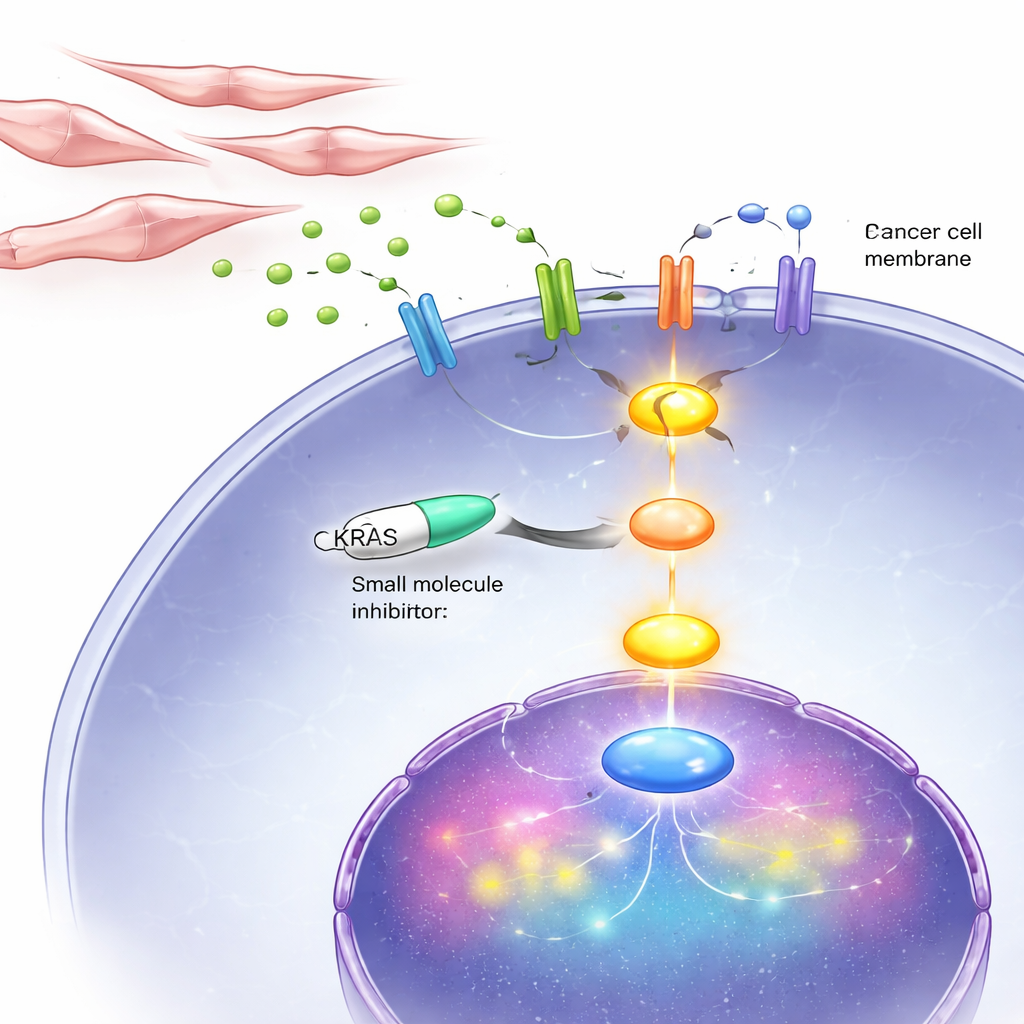
Blockera KRAS-livlinan i celler och i möss
Eftersom denna ondartade cykel slutligen kanaliseras genom KRAS testade forskarna ett läkemedel, BI-3406, som stör hur KRAS slås på inne i cellerna. I labbodlingar bromsade denna hämmare kraftigt tillväxten och rörligheten hos androgenoberoende prostatacancerceller, inklusive de med onormalt KRAS och de med normalt KRAS som aktiveras av signaler från fibroblaster. Hos möss som fått implantat med DNPC-liknande tumörer krympte tumörerna vid daglig behandling med hämmaren och markörer för celldelning minskade, samtidigt som tecken på programmerad celldöd ökade. Viktigt är att läkemedlet hade mycket mindre effekt på hormonberoende cancerceller, vilket bekräftar idén att KRAS är särskilt kritiskt i det sena, dubbelnegativa stadiet.
Vad detta innebär för framtida behandling
För en lekman är slutsatsen att när hormonbehandling tränger in prostatacancern i ett hörn kan tumören fly genom att rekrytera närliggande fibroblaster som matar den med en annan tillväxtsignal som i slutändan slår på KRAS. Studien kartlägger denna flyktväg i detalj och visar att avklippning av KRAS-signaleringen kan döda dessa resistenta celler i modeller. Även om mer arbete krävs hos patienter, särskilt med läkemedel som säkert kan blockera KRAS eller dess upstreamhjälpare, lyfter fynden fram en ny strategi: att rikta in sig på kedjan CCL2–FGF8–KRAS för att behandla de mest svårbehandlade, hormonoberoende formerna av prostatacancer.
Citering: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Nyckelord: dubbelnegativ prostatacancer, tumörmikromiljö, KRAS-signalering, fibroblaster, androgenoberoende cancer