Clear Sky Science · es
Activación de KRAS mediada por fibroblastos en el cáncer de próstata doble negativo
Por qué importa este estudio sobre el cáncer de próstata
Para muchos hombres, las terapias que bloquean las hormonas pueden mantener el cáncer de próstata bajo control durante años. Sin embargo, algunos tumores reaparecen con el tiempo en una forma sigilosa que ya no responde a los fármacos hormonales y no activa los marcadores habituales en sangre. Este estudio indaga cómo estos cánceres de próstata “doble negativos” sobreviven y se diseminan, revelando una conversación oculta entre las células cancerosas y las células de soporte a su alrededor —y señalando un punto débil nuevo que futuros fármacos podrían explotar.
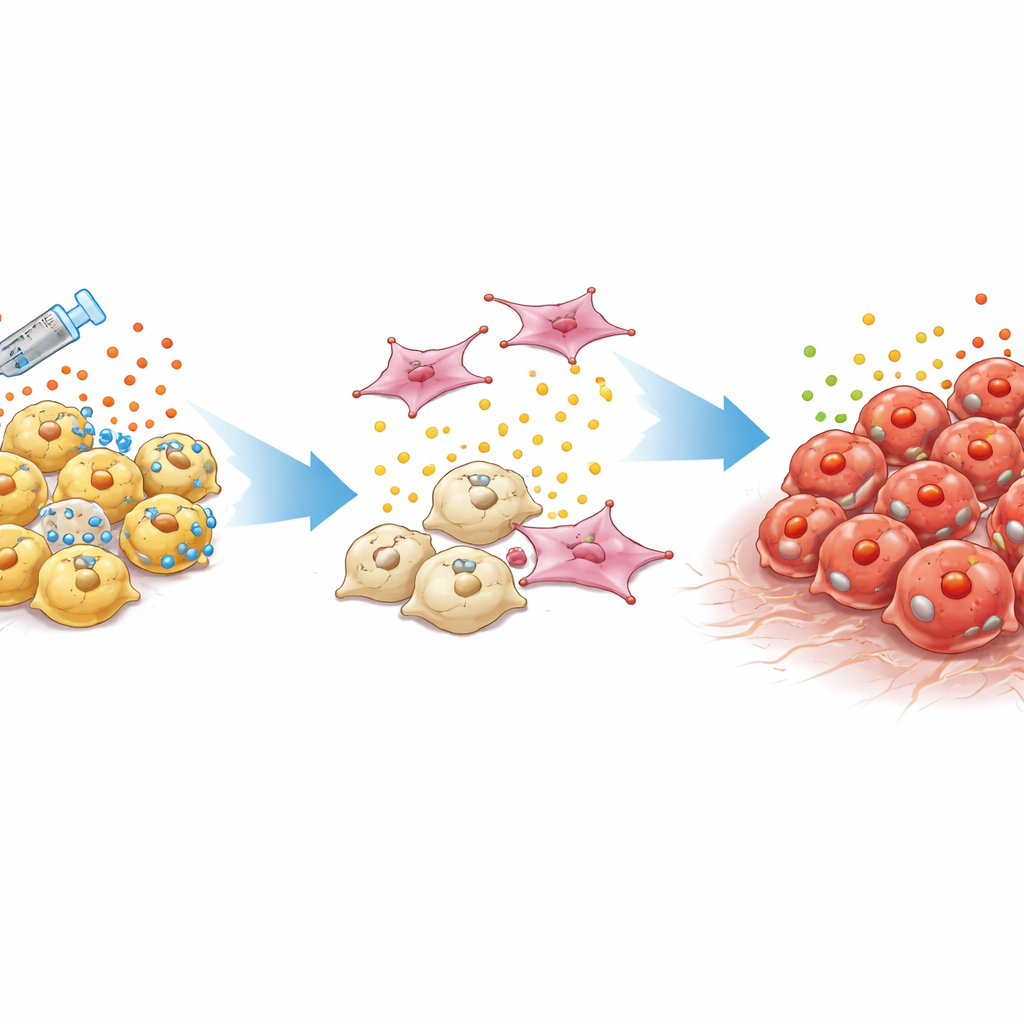
Un tipo de tumor difícil de detectar y de tratar
Los cánceres de próstata habituales dependen de las hormonas masculinas que actúan a través de una proteína llamada receptor de andrógenos. Los médicos suprimen esa señal con terapia hormonal y fármacos dirigidos más recientes. Con el tiempo, sin embargo, algunos tumores evolucionan a cáncer de próstata resistente a la castración que ya no depende de esta vía. Un subtipo especialmente peligroso, llamado cáncer de próstata doble negativo, carece tanto de actividad del receptor de andrógenos como de rasgos de las células “neuroendocrinas” similares a neuronas. Estos tumores a menudo vuelven a crecer localmente o se diseminan pese a los bajos niveles de los marcadores habituales en sangre, dejando a los clínicos con pocas pistas y sin tratamientos probados.
Un motor de crecimiento que se activa cuando las hormonas se apagan
Los investigadores se centraron en KRAS, un interruptor molecular bien conocido que impulsa el crecimiento en cánceres de pulmón y colon cuando está mutado. En el cáncer de próstata, tales mutaciones son raras, pero el perfil genético de pacientes sugería que KRAS podría estar implicado en los casos doble negativos. Al comparar distintas líneas celulares de cáncer de próstata, hallaron que la señalización de KRAS tenía poca función en células dependientes de hormonas, pero se volvía crucial una vez que las células dejaban de depender de señales de andrógenos. En células similares a DNPC, reducir KRAS cortó bruscamente su capacidad de crecer, moverse e invadir, mientras que las células sensibles a hormonas apenas notaban la pérdida —lo que sugiere que KRAS se convierte en un motor clave solo en el estado tardío e independiente de hormonas.
Cómo las células de soporte cercanas alimentan el interruptor canceroso
Los tumores no son solo células cancerosas descontroladas; son comunidades que incluyen fibroblastos —células del tejido conectivo que ayudan a moldear el entorno local. El equipo descubrió que cuando se bloquea la señalización de andrógenos en las células de cáncer de próstata, las células cancerosas cambian los tipos de receptores que muestran en su superficie, volviéndose más receptivas a una señal de crecimiento llamada FGF8. Al mismo tiempo, las células privadas de hormonas liberan una señal de alarma, la quimiocina CCL2, al entorno. Las células estromales de tipo fibroblasto en tumores de próstata avanzados llevan receptores para CCL2. Cuando CCL2 alcanza a estas células estromales, activa una vía interna que aumenta su producción y liberación de FGF8. Ese FGF8 vuelve entonces a las células cancerosas, activa sus receptores alterados y a su vez enciende KRAS, impulsando señales potentes de crecimiento y supervivencia.
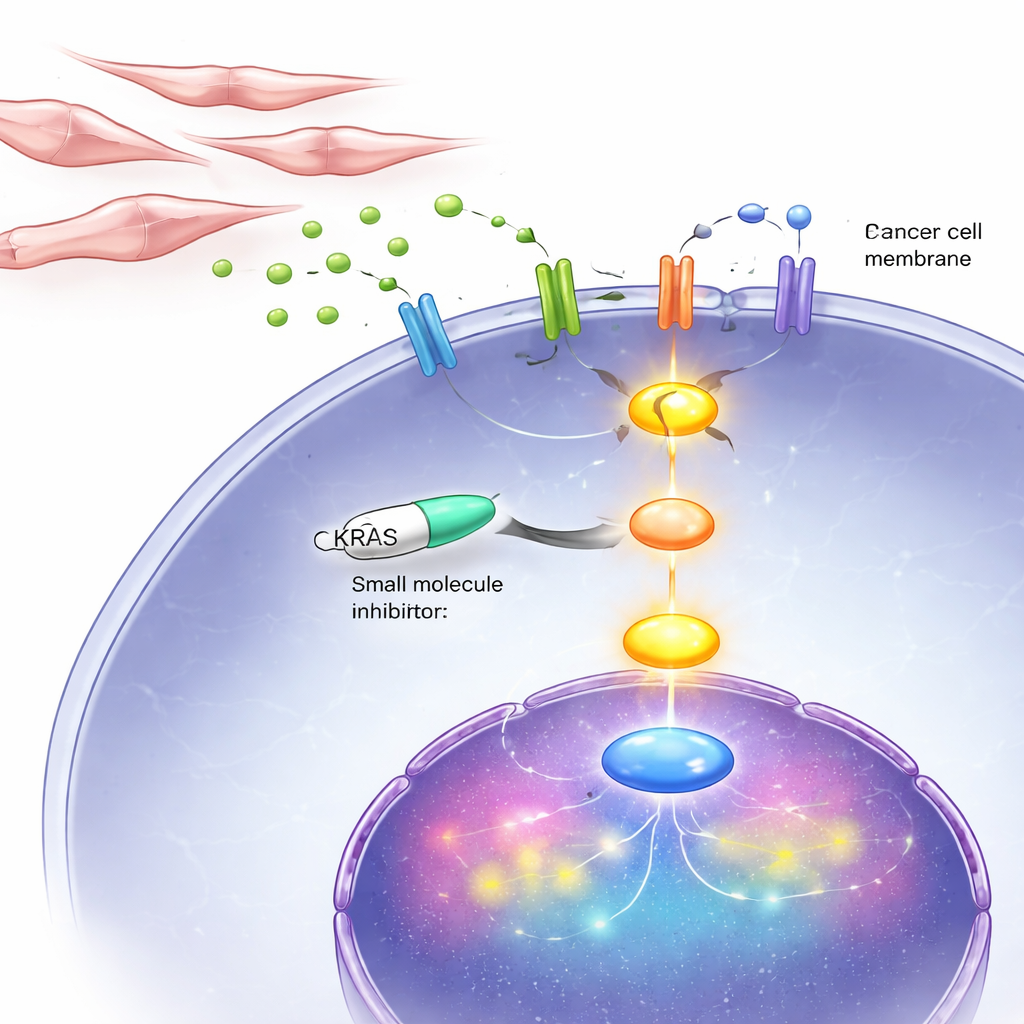
Bloquear la línea de vida de KRAS en células y en ratones
Puesto que este ciclo vicioso acaba canalizándose a través de KRAS, los investigadores probaron un fármaco, BI-3406, que interfiere con la forma en que KRAS se activa dentro de las células. En placas de laboratorio, este inhibidor ralentizó con fuerza el crecimiento y la movilidad de células de cáncer de próstata independientes de andrógenos, incluidas aquellas con KRAS anómalo y otras con KRAS normal activado por señales de fibroblastos. En ratones implantados con tumores similares a DNPC, el tratamiento diario con el inhibidor redujo el tamaño tumoral y los marcadores de división celular, al tiempo que aumentó los signos de muerte celular programada. De forma importante, el fármaco tuvo mucho menos impacto en células cancerosas dependientes de hormonas, lo que refuerza la idea de que KRAS es especialmente crítico en la fase tardía doble negativa.
Qué implica esto para tratamientos futuros
Para un lector general, la conclusión es que cuando la terapia hormonal empuja al cáncer de próstata a un rincón, el tumor puede escapar reclutando a fibroblastos cercanos para que le suministren una señal de crecimiento distinta que en última instancia activa KRAS. Este estudio cartografía esa ruta de escape con detalle y muestra que cortar la señalización de KRAS puede eliminar estas células resistentes en modelos. Aunque se necesita más trabajo en pacientes, especialmente con fármacos que puedan bloquear de forma segura a KRAS o a sus activadores en amont, los hallazgos subrayan una estrategia nueva: apuntar a la cadena CCL2–FGF8–KRAS para tratar las formas más resistentes e independientes de hormonas del cáncer de próstata.
Cita: Kamijima, T., Izumi, K., Hiratsuka, K. et al. Fibroblast-mediated KRAS activation in double-negative prostate cancer. Cell Death Dis 17, 403 (2026). https://doi.org/10.1038/s41419-026-08800-3
Palabras clave: cáncer de próstata doble negativo, microambiente tumoral, señalización KRAS, fibroblastos, cáncer independiente de andrógenos