Clear Sky Science · zh
TGF-β/SMAD4/14-3-3σ/TFEB 轴促进间充质-上皮转变并抑制结直肠癌中的自噬
这项研究为何与结肠癌相关
结直肠癌是导致癌症死亡的主要原因之一,因为肿瘤细胞常常从肠道扩散到远端器官。这项研究揭示了肠上皮细胞内部此前未被认识的一条保护回路,能够抑制这种扩散。通过绘制多种分子之间的相互作用,研究人员展示了肠道中的正常信号如何将癌细胞推回更有序的状态,并切断其一种生存伎俩——一种被称为自噬的自我清理过程。
肠道中的保护性信号
我们的肠道持续暴露于食物、细菌和机械性应力,因此肠上皮细胞依赖强有力的控制系统来维持生长与修复之间的平衡。一种重要信号称为 TGF‑β,通常在早期肿瘤发展中起制动作用。它通过名为 SMAD4 的蛋白发挥作用,SMAD4 进入细胞核并调控基因的开关。在结直肠癌中,SMAD4 常常缺失,缺失该蛋白的患者肿瘤更易发生转移且预后更差。作者旨在弄清 SMAD4 调控哪些特定基因,以解释其阻断侵袭与扩散的机制。
癌细胞内的一连串守护者
研究组发现 SMAD4 直接激活一个名为 14‑3‑3σ 的基因,该基因长期以来被认为是肿瘤抑制子。利用人类结直肠癌细胞系、来源于患者的体外迷你肿瘤和小鼠模型,他们证明激活 SMAD4 一致性地提升 14‑3‑3σ 水平,而去除 SMAD4 则阻止这一上调。他们在 14‑3‑3σ 的调控区定位到 SMAD4 的结合位点,并证实 SMAD4 在这些位点的物理占位,从而在人体和小鼠肠上皮细胞中确立了 14‑3‑3σ 作为直接靶基因的地位。在正常小鼠肠道中,14‑3‑3σ 在绒毛顶端尤为丰富,但当 Smad4 被删除时这种分布模式消失,强调了两者在组织分化过程中的紧密关联。
将癌细胞推回有序状态
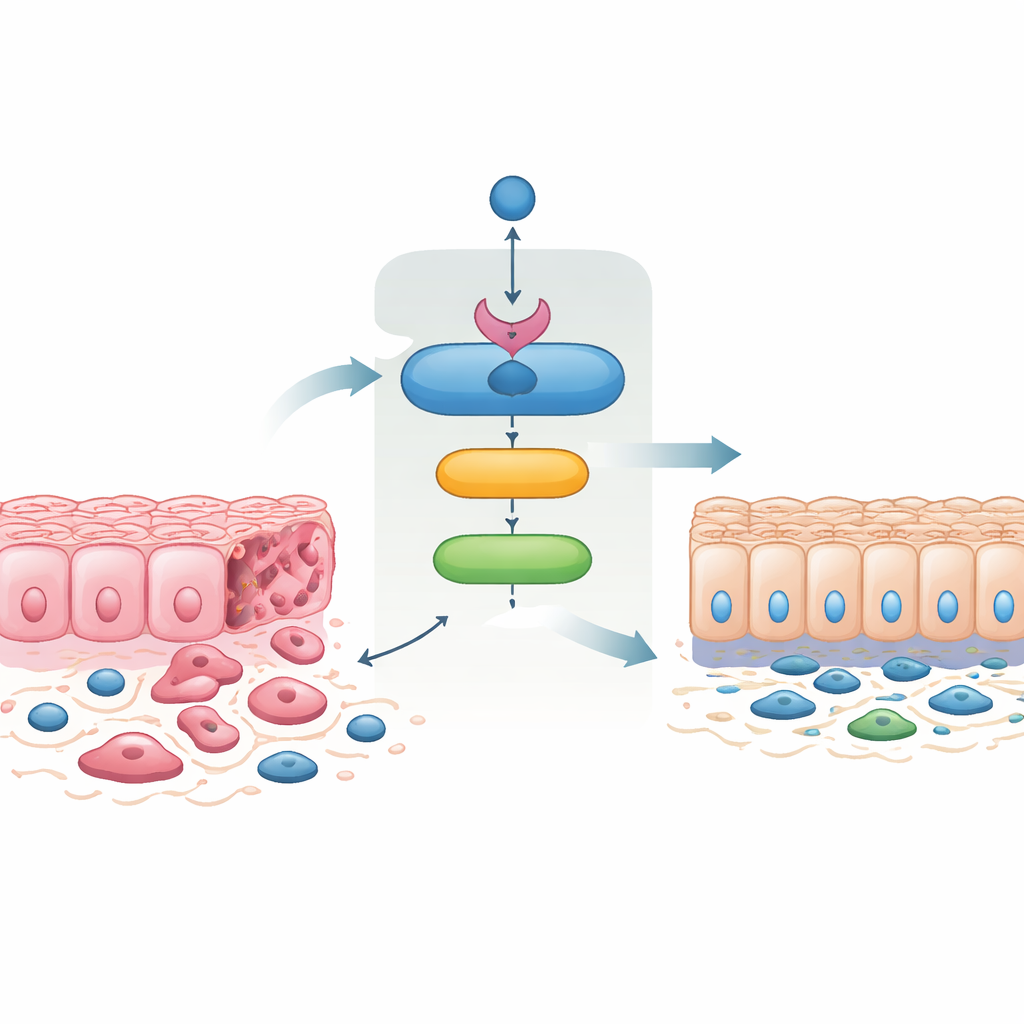
癌细胞常经历“上皮-间充质转化”(EMT),由紧密连接的片状上皮细胞变为更具移动性的梭形细胞,从而更容易侵袭并播散转移。相反过程称为间充质-上皮转变(MET),可恢复牢固的细胞间接触并减少侵袭性。当研究者将 SMAD4 重新导入那些通常缺失该蛋白的侵袭性结直肠癌细胞时,细胞表现出朝上皮表型的转变,恢复了位于膜上的细胞粘附蛋白,并失去了与迁移和侵袭相关的特征。恢复 SMAD4 的细胞迁移性降低,通过人工膜的侵袭减少,克隆形成能力也下降。值得注意的是,仅强制表达 14‑3‑3σ 即能产生非常相似的变化,而阻断 14‑3‑3σ 则在很大程度上消除了 SMAD4 的效应。这表明 14‑3‑3σ 并非旁观者,而是 SMAD4 驯服侵袭行为的关键介导者。
关闭一条生存通路
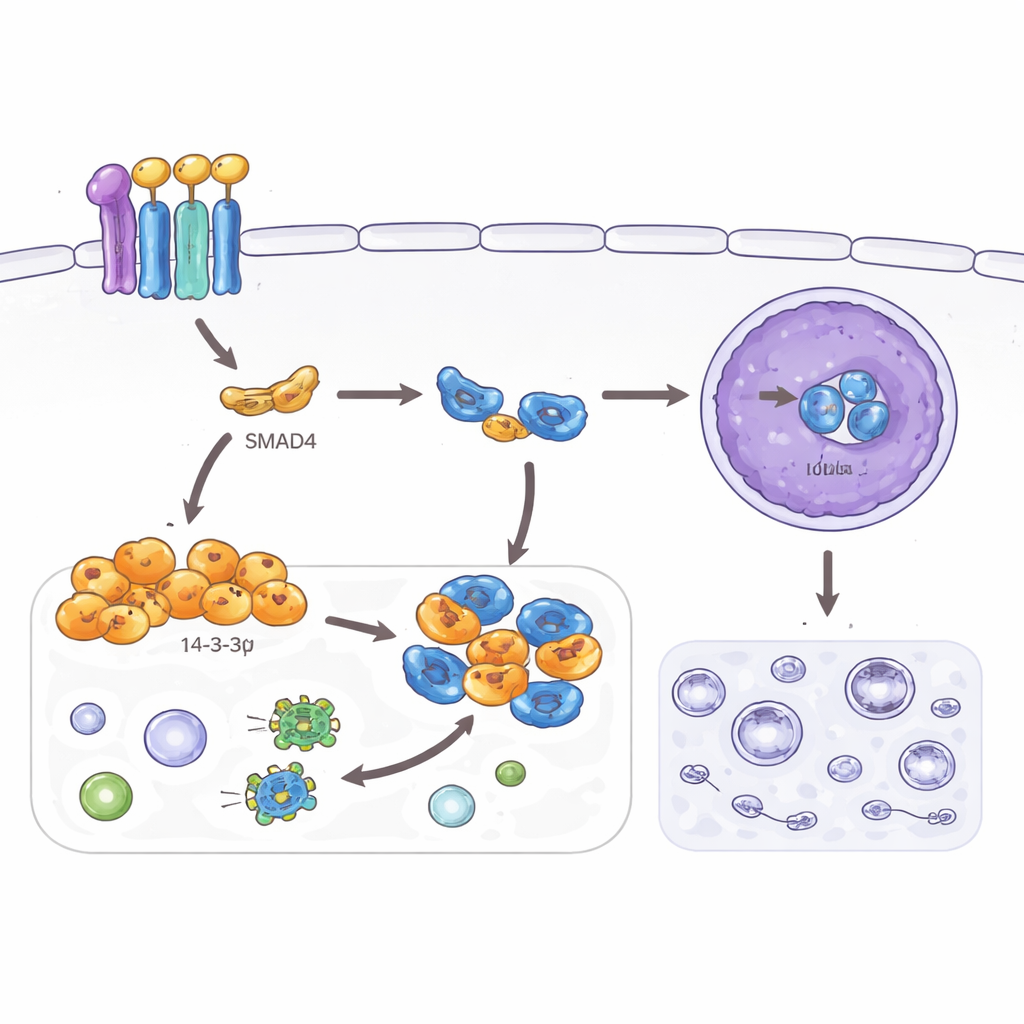
该研究还考察了自噬,这是一种通过分解细胞内部成分来帮助细胞在应激下生存的回收程序。虽然自噬在正常组织中有益,但增强的自噬可以帮助癌细胞应对恶劣环境和治疗。作者发现 SMAD4 和 14‑3‑3σ 都能降低结直肠癌细胞中自噬标志物,并减少显微镜下观察到的回收囊泡数量。他们将这一效应追溯到另一个蛋白 TFEB,它是自噬和溶酶体的主控因子。通常当 TFEB 进入细胞核时,它会激活许多与自噬相关的基因。在这里,SMAD4 诱导的 14‑3‑3σ 在细胞质中结合 TFEB,并阻止其进入细胞核,但这一束缚仅在 TFEB 的某一特定位点被化学标记时发生。当该位点发生突变时,14‑3‑3σ 无法再约束 TFEB,自噬恢复,且对侵袭性与细胞形态的抑制效应被削弱。
对患者的意义
综合来看,这些发现勾勒出肠道中一条线性保护轴:TGF‑β 激活 SMAD4,SMAD4 上调 14‑3‑3σ,14‑3‑3σ 将 TFEB 困于核外。该组合使结直肠癌细胞趋向更有序、移动性更低的状态,并抑制其自我清理机制,可能使其更难转移且对治疗更敏感。当 SMAD4 或 14‑3‑3σ 丢失时,TFEB 活性增强,可能同时促进细胞可塑性和应激耐受性。尽管仍需在活体动物和临床样本中做进一步研究,但此处揭示的通路指出了未来药物可以加固机体对抗转移性结直肠癌的内在防线的新分子靶点。
引用: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
关键词: 结直肠癌, 转移, 自噬, 上皮可塑性, TFEB