Clear Sky Science · pl
Oś TGF-β/SMAD4/14-3-3σ/TFEB promuje przejście mezenchymalno-epitelialne i hamuje autofagię w raku jelita grubego
Dlaczego to badanie ma znaczenie dla raka jelita
Rak jelita grubego jest jedną z głównych przyczyn zgonów z powodu nowotworów, ponieważ komórki nowotworowe często rozsiewają się z jelita do odległych narządów. To badanie ujawnia wcześniej niepoznany wewnętrzny układ zabezpieczający w komórkach jelita, który może ograniczać to rozsiewanie. Mapując, jak kilka cząsteczek ze sobą oddziałuje, autorzy pokazują, w jaki sposób normalne sygnały w jelicie mogą skierować komórki nowotworowe z powrotem ku bardziej uporządkowanemu stanowi i odciąć jedną z ich strategii przetrwania — samoczyszczący proces zwany autofagią.
Ochronne przesłanie w jelicie
Nasze jelita są stale narażone na pokarm, bakterie i stres mechaniczny, dlatego komórki jelitowe polegają na silnych układach kontroli, aby zachować równowagę między wzrostem a naprawą. Jeden z głównych sygnałów, zwany TGF-β, zwykle działa jak hamulec we wczesnym rozwoju nowotworu. Działa przez białko o nazwie SMAD4, które wnika do jądra komórkowego i włącza lub wyłącza geny. W raku jelita grubego SMAD4 jest często utracony, a pacjenci, których guzy nie zawierają tego białka, mają tendencję do większej liczby przerzutów i gorszych wyników. Autorzy postanowili ustalić, które konkretne geny kontrolowane przez SMAD4 mogą tłumaczyć jego zdolność do blokowania inwazji i rozsiewu.
Łańcuch strażników wewnątrz komórek nowotworowych
Zespół odkrył, że SMAD4 bezpośrednio aktywuje gen zwany 14-3-3σ, od dawna znany jako supresor nowotworowy. Wykorzystując linie komórkowe raka jelita grubego pochodzące od ludzi, mini-guzy pacjentów hodowane w laboratorium oraz modele mysie, pokazali, że włączenie SMAD4 konsekwentnie podnosi poziomy 14-3-3σ, podczas gdy usunięcie SMAD4 uniemożliwia ten wzrost. Zidentyfikowali miejsca dokowania dla SMAD4 w regionie kontrolnym 14-3-3σ i potwierdzili, że SMAD4 fizycznie zajmuje te miejsca, co zdecydowanie ustanawia 14-3-3σ jako bezpośredni cel zarówno w komórkach jelita ludzkiego, jak i mysiego. W normalnym jelicie myszy 14-3-3σ jest szczególnie obfite na szczytach kosmków jelitowych, lecz ten wzór znika po usunięciu Smad4, podkreślając ścisły związek obu podczas różnicowania tkanki.
Przywracanie komórkom nowotworowym porządku
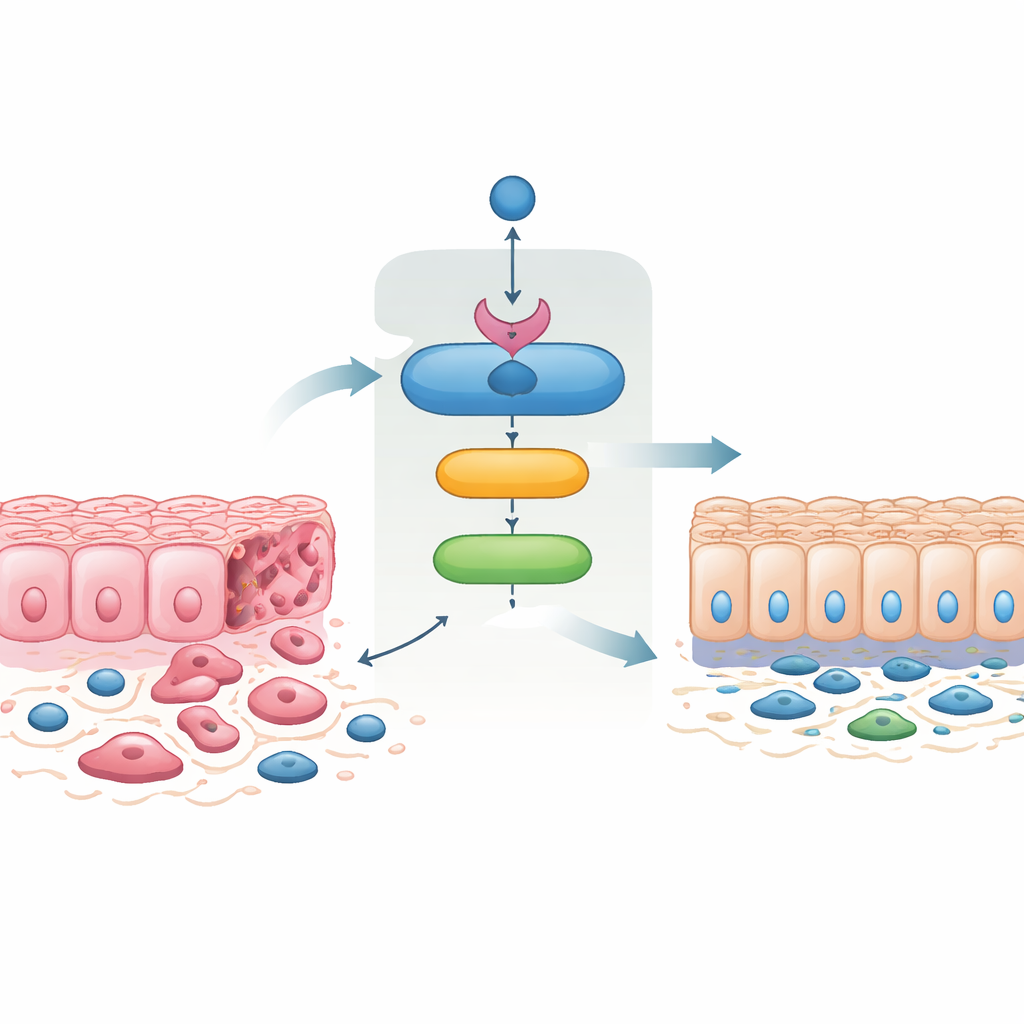
Komórki nowotworowe często przechodzą tzw. przejście nabłonkowo-mezenchymalne, zmieniając się z ściśle powiązanych, arkuszowych komórek w bardziej ruchome, wrzecionowate, które łatwiej inwazują i dają przerzuty. Odwrócenie tego procesu, przejście mezenchymalno-epitelialne, przywraca szczelne kontakty międzykomórkowe i zmniejsza inwazyjność. Kiedy badacze ponownie wprowadzili SMAD4 do agresywnych komórek raka jelita grubego, które zazwyczaj go nie mają, komórki przyjęły bardziej nabłonkowy wygląd, odzyskały błonowo związane białka adhezji i utraciły cechy związane z mobilnością i inwazją. Te komórki z przywróconym SMAD4 migrowały mniej, mniej inwadowały przez sztuczne membrany i tworzyły mniej kolonii. Co godne uwagi, wymuszone wytwarzanie wyłącznie 14-3-3σ dawało bardzo podobne zmiany, a blokada 14-3-3σ w dużej mierze znosiła efekty SMAD4. To pokazuje, że 14-3-3σ nie jest tylko obserwatorem, lecz kluczowym mediatorem zdolności SMAD4 do okiełznania zachowań inwazyjnych.
Wyłączanie ścieżki przetrwania
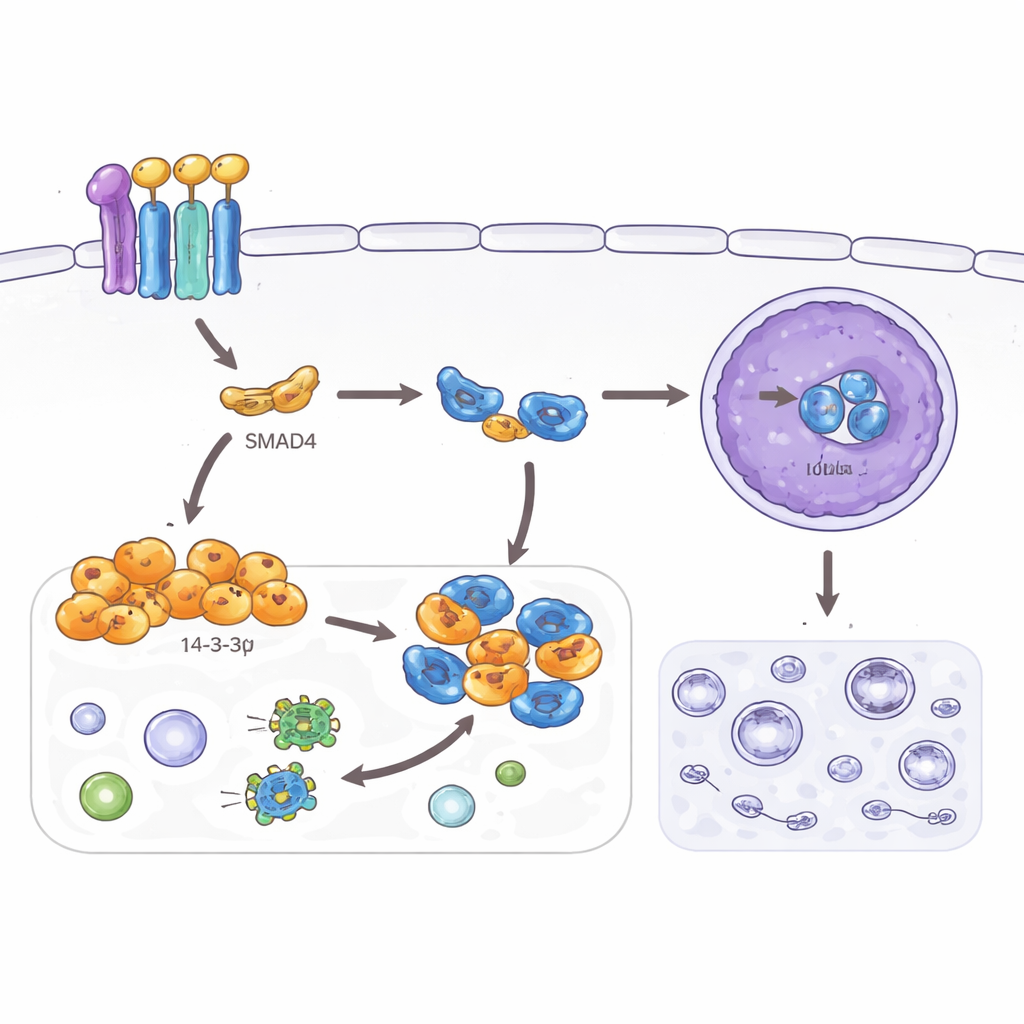
Badanie przeanalizowało również autofagię — program recyklingu, który pomaga komórkom przetrwać stres poprzez rozkładanie wewnętrznych składników. Chociaż użyteczna w tkankach normalnych, nasilona autofagia może pomagać komórkom nowotworowym radzić sobie w wrogim środowisku i przeciwko leczeniu. Autorzy stwierdzili, że SMAD4 i 14-3-3σ obniżają markery autofagii w komórkach raka jelita grubego i zmniejszają liczbę pęcherzyków recyklingowych widocznych w mikroskopie. To działanie przypisali innemu białku — TFEB, głównemu kontrolerowi autofagii i lizosomów. Zazwyczaj, gdy TFEB wchodzi do jądra, aktywuje wiele genów związanych z autofagią. Tutaj 14-3-3σ zależne od SMAD4 wiąże TFEB w pozajądrowej przestrzeni komórki i uniemożliwia mu dotarcie do jądra, lecz tylko wtedy, gdy określone miejsce na TFEB jest chemicznie oznakowane. Gdy to miejsce jest zmutowane, 14-3-3σ nie jest już w stanie zatrzymać TFEB, autofagia wraca, a efekty tłumiące inwazję i zmianę kształtu komórek słabną.
Co to oznacza dla pacjentów
Podsumowując, wyniki przedstawiają liniową ochronną oś w jelicie: TGF-β aktywuje SMAD4, SMAD4 włącza 14-3-3σ, a 14-3-3σ więzi TFEB poza jądrem. To połączenie popycha komórki raka jelita grubego w stronę bardziej uporządkowanego, mniej ruchomego stanu i tłumi ich mechanizm samoczyszczenia, co może zmniejszać ich zdolność do rozsiewu i zwiększać podatność na leczenie. Gdy SMAD4 lub 14-3-3σ są utracone, TFEB staje się bardziej aktywny, potencjalnie zwiększając zarówno plastyczność komórek, jak i odporność na stres. Chociaż potrzebne są dalsze badania na żywych organizmach i próbkach klinicznych, ujawniona tu ścieżka wskazuje nowe molekularne miejsca, w których przyszłe leki mogłyby wzmocnić naturalne mechanizmy obronne organizmu przeciwko przerzutowemu rakowi jelita grubego.
Cytowanie: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Słowa kluczowe: rak jelita grubego, przerzuty, autofagia, plastyczność nabłonkowa, TFEB