Clear Sky Science · sv
TGF-β/SMAD4/14-3-3σ/TFEB-axeln främjar mesenkymal‑epitelial övergång och hämmar autophagi vid kolorektal cancer
Varför denna studie är viktig för tjocktarmscancer
Kolorektal cancer är en av de ledande orsakerna till cancerdöd eftersom tumörceller ofta sprider sig från tarmen till avlägsna organ. Denna studie avslöjar en tidigare okänd skyddscircuit inne i tarmceller som kan bromsa denna spridning. Genom att kartlägga hur flera molekyler kommunicerar visar forskarna hur normala signaler i tarmen kan pressa cancerceller tillbaka mot ett mer ordnat tillstånd och stänga av ett av deras överlevnadstrick, en självstädande process kallad autophagi.
Ett skyddande budskap i tarmen
Våra tarmar utsätts ständigt för föda, bakterier och mekanisk stress, så cellerna i tarmen förlitar sig på kraftfulla kontrollsystem för att hålla tillväxt och reparation i balans. En huvudsignal, kallad TGF‑β, fungerar vanligtvis som en broms i tidig tumörutveckling. Den verkar via ett protein som heter SMAD4, vilket förflyttar sig in i cellkärnan och slår på eller av gener. I kolorektala cancerformer saknas ofta SMAD4, och patienter vars tumörer saknar detta protein har ofta fler metastaser och sämre överlevnad. Författarna ville förstå vilka specifika gener SMAD4 styr som kan förklara dess förmåga att blockera invasion och spridning.
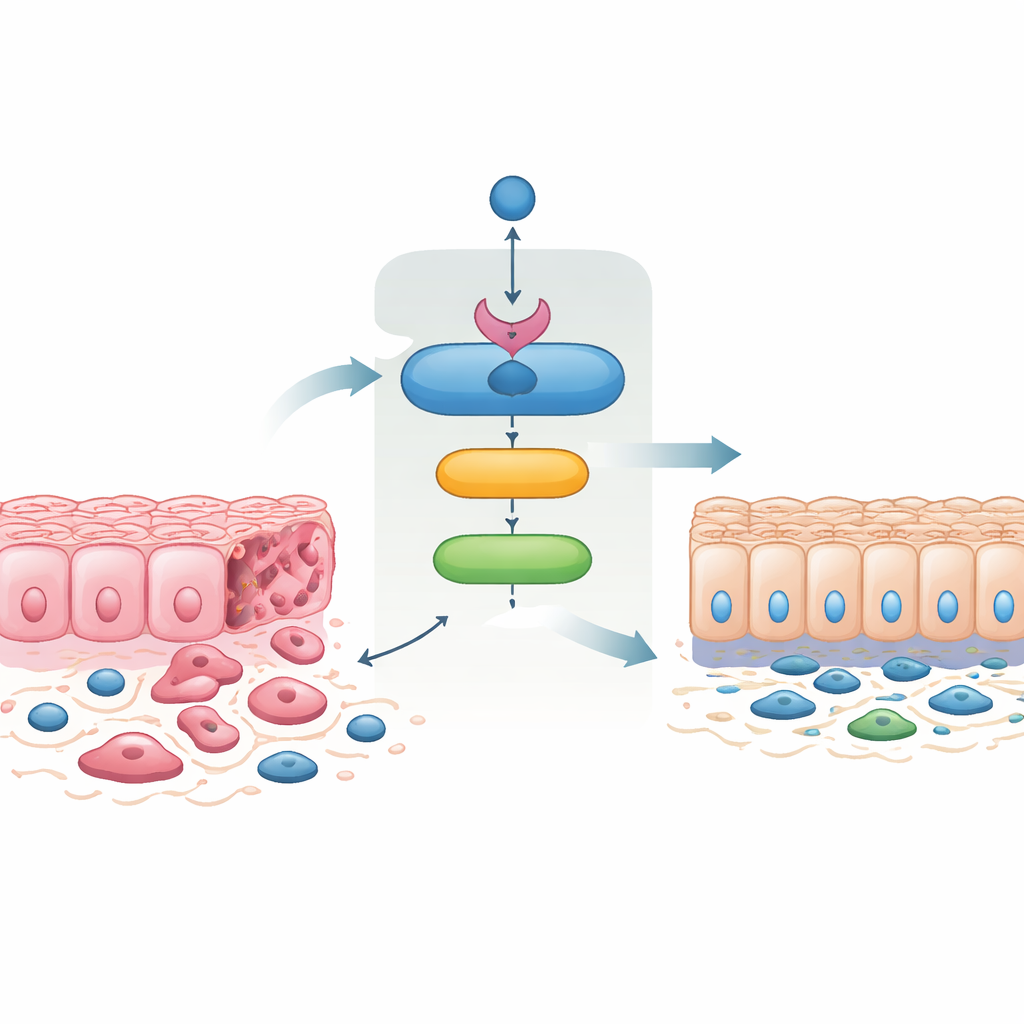
En kedja av väktare inne i cancerceller
Teamet upptäckte att SMAD4 direkt aktiverar en gen kallad 14‑3‑3σ, länge känd som en tumörsuppressor. Med hjälp av humana kolorektala cancercellinjer, patient‑härledda mini‑tumörer odlade i labbet och musemodeller visade de att aktivering av SMAD4 pålitligt ökar nivåerna av 14‑3‑3σ, medan borttagning av SMAD4 förhindrar denna ökning. De lokaliserade bindningsställen för SMAD4 i 14‑3‑3σ:s kontrollregion och bekräftade att SMAD4 fysiskt upptar dessa platser, vilket fastställer 14‑3‑3σ som ett direkt måL i både mänskliga och musintestin‑celler. I normal musintestinum är 14‑3‑3σ särskilt rikligt vid vili‑spetsarna, men detta mönster försvinner när Smad4 tas bort, vilket belyser hur tätt de två är kopplade under vävnadsdifferentiering.
Att driva cancerceller tillbaka mot ordning
Cancerceller genomgår ofta en "epitelial‑mesenkymal övergång", där de går från tätt sammanbundna, bladliknande celler till mer rörliga, spindelformade celler som lättare invaderar och bildar metastaser. Den omvända processen, mesenkymal‑epitelial övergång, återställer starka cell‑till‑cell‑kontakter och minskar invasivitet. När forskarna återinförde SMAD4 i aggressiva kolorektala cancerceller som normalt saknar det, skiftade cellerna mot ett epitelialt utseende, återfick membranbundna adhesionsproteiner och förlorade egenskaper kopplade till rörlighet och invasion. Dessa SMAD4‑återställda celler migrerade mindre, invaderade mindre genom konstgjorda membran och bildade färre kolonier. Anmärkningsvärt nog gav tvingad produktion av 14‑3‑3σ ensamt mycket liknande förändringar, och blockering av 14‑3‑3σ utsudda till stor del SMAD4:s effekter. Detta visar att 14‑3‑3σ inte bara är en åskådare utan en nyckelmedlare av SMAD4:s förmåga att tämja invasivt beteende.
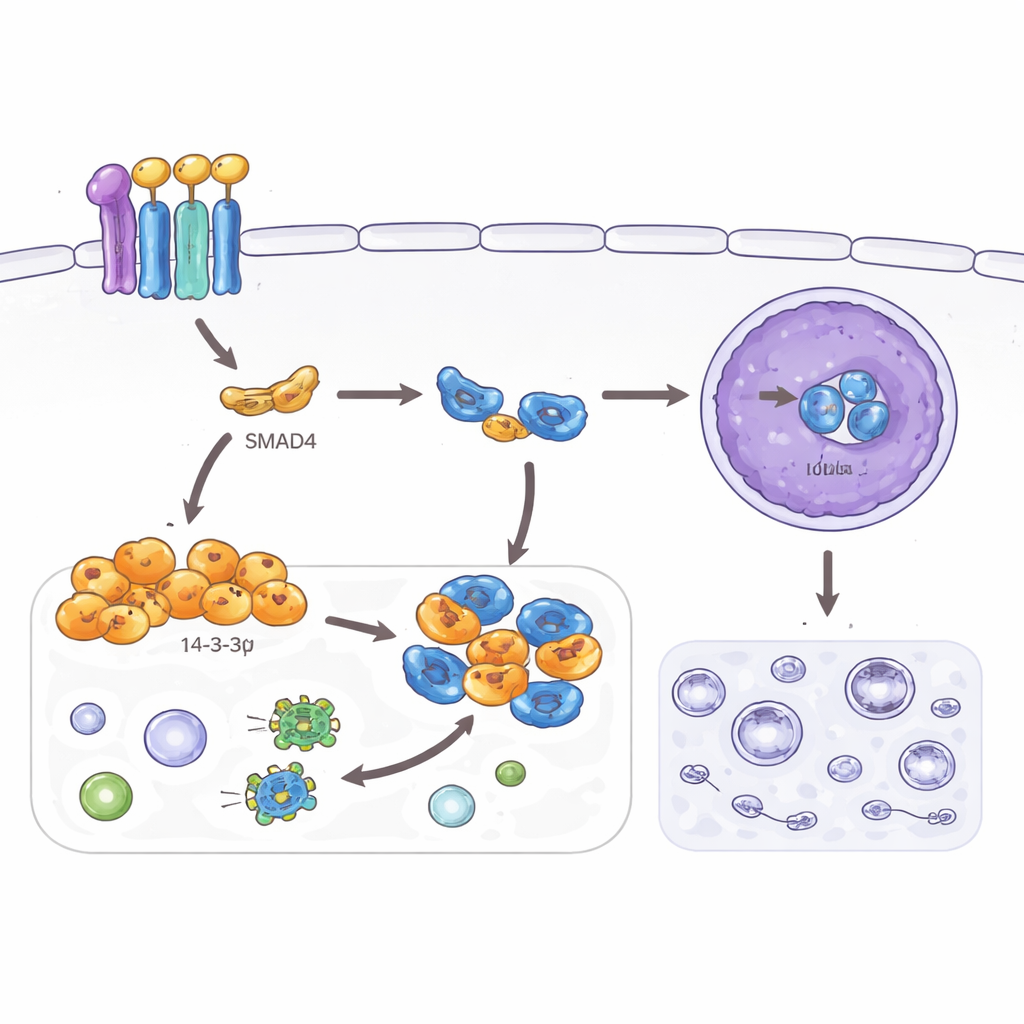
Att stänga av en överlevnadsbana
Studien undersökte också autophagi, ett återvinningsprogram som hjälper celler att överleva stress genom att bryta ner interna komponenter. Fastän användbar i normala vävnader kan förhöjd autophagi hjälpa cancerceller att klara fientliga miljöer och behandling. Författarna fann att både SMAD4 och 14‑3‑3σ sänker markörer för autophagi i kolorektala cancerceller och minskar antalet återvinningsvesiklar som observeras i mikroskopet. De spårade denna effekt till ett annat protein, TFEB, en huvudregulator för autophagi och lysosomer. Normalt, när TFEB går in i kärnan, aktiverar det många gener relaterade till autophagi. Här binder SMAD4‑driven 14‑3‑3σ TFEB i cellens yttre compartment och hindrar det från att nå kärnan, men endast när en specifik plats på TFEB har kemiskt märkts. När denna plats muteras kan 14‑3‑3σ inte längre hålla TFEB tillbaka, autophagin återupptas och de hämmande effekterna på invasion och cellform försvagas.
Vad detta betyder för patienter
Tillsammans skisserar fynden en linjär skyddsaxel i tarmen: TGF‑β aktiverar SMAD4, SMAD4 slår på 14‑3‑3σ, och 14‑3‑3σ fångar TFEB utanför kärnan. Denna kombination driver kolorektala cancerceller mot ett mer ordnat, mindre rörligt tillstånd och dämpar deras självstädande maskineri, vilket kan göra dem mindre benägna att sprida sig och mer sårbara för behandling. När SMAD4 eller 14‑3‑3σ går förlorade blir TFEB mer aktivt, vilket potentiellt ökar både cellplasticitet och stresstålighet. Även om ytterligare arbete i levande djur och kliniska prover behövs, lyfter den här avslöjade vägen fram nya molekylära punkter där framtida läkemedel kan förstärka kroppens egna försvar mot metastaserande kolorektal cancer.
Citering: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Nyckelord: kolorektal cancer, metastasering, autophagi, epitelial plasticitet, TFEB